Tecnologías disponibles para la colaboración
Neurociencia
Modelado de enfermedades neurológicas – fred gage Detalles"
Fred "Rusty" Gage es líder mundial en neurogénesis y presidente de la Sociedad Internacional para la Investigación de Células Madre. Ha desarrollado nuevos modelos celulares de enfermedades neurológicas (esquizofrenia, EM, autismo, Alzheimer, Parkinson) utilizando células madre pluripotentes inducidas por humanos (iPSC) derivadas de pacientes donantes y diferenciadas en tipos de células neuronales específicas. Estos modelos son útiles para estudiar los mecanismos de la enfermedad, identificar objetivos, detectar compuestos y estratificar pacientes. Son más predictivos de fenotipos de enfermedades que los modelos actuales. Gage también ha desarrollado un modelo de mielinización in vitro utilizando iPSCs para la detección de compuestos farmacológicos y para comprender mejor enfermedades como la esquizofrenia y el Parkinson.
Modelos animales de pérdida neuronal en enfermedades como el Parkinson – Martin Goulding Detalles"
Los mecanismos fundamentales que contribuyen a los déficits cognitivos y motores que acompañan a las enfermedades neurodegenerativas son poco conocidos, debido en gran parte a la naturaleza progresiva de estas enfermedades. El laboratorio de Goulding estudia los efectos inmediatos y posteriores de la pérdida de células neuronales, como los cambios continuos en las neuronas preservadas o en otros tipos de células que componen el circuito, y determina cómo se adaptan a la pérdida de un tipo de célula neuronal en particular. Mediante la ablación selectiva de tipos de células neuronales específicas, de una manera dependiente del tiempo y del espacio, se pueden realizar lesiones "quirúrgicas" y examinar los cambios resultantes con mucha mayor precisión. Esto permite una evaluación más precisa de los cambios celulares, sinápticos y fisiológicos concomitantes que ocurren en respuesta a la lesión inicial. Ha utilizado este enfoque para desarrollar un modelo de la enfermedad de Parkinson.
Nuevas dianas moleculares para el tratamiento de la esquizofrenia – Kuo Fen Lee Detalles"
Las disfunciones en los sistemas de glutamato, GABA y serotonina también se han implicado en la esquizofrenia. La mayoría de los estudios mecanicistas hasta ahora se han centrado en la modulación DA del circuito neural en la corteza prefrontal (PFC) o el cuerpo estriado, y los han relacionado con los fenotipos conductuales de la esquizofrenia. Sin embargo, se sabe poco sobre los circuitos reguladores aguas arriba de estas vías. Para comprender mejor cómo las neuronas colinérgicas ejercen sus funciones en distintas vías y cómo superar la dificultad de la selectividad del subtipo mAChR y los efectos secundarios periféricos, el grupo de Lee ha perfilado y caracterizado los genes que se expresan de manera única o selectiva en los subtipos de neuronas colinérgicas y que regulan de manera única la electrofisiología de Subtipos de mAChR. Actualmente, su laboratorio está investigando la organización y la función de una vía neuronal muy poco explorada pero potencialmente muy importante desde las neuronas colinérgicas MT a las DA, y busca posibles causas, así como objetivos moleculares y celulares para tratar la esquizofrenia.
Identificación de factores secretados por astrocitos para tratar los trastornos del espectro autista – nicolas allen Detalles"
Antecedentes y significado
Múltiples tipos de trastornos del espectro autista (TEA) dan lugar a defectos celulares similares en el cerebro en desarrollo, a pesar de que los TEA son causados por distintos conjuntos de mutaciones genéticas o surgen esporádicamente. Los fenotipos celulares incluyen muerte neuronal alterada, crecimiento reducido del árbol dendrítico neuronal y defectos en la formación y función de la sinapsis neuronal. Los fenotipos celulares similares presentes en múltiples TEA sugieren que pueden compartir defectos comunes en los mecanismos moleculares que regulan el desarrollo neuronal y aumentan el potencial de identificar vías comunes para la orientación terapéutica y el tratamiento de los TEA esporádicos. Muchas características de ASD no son células autónomas para las neuronas y pueden ser inducidas por astrocitos, el tipo de célula más abundante en el cerebro. Los astrocitos de modelos de ratón ASD inducen disfunción en las neuronas de tipo salvaje (WT), y los astrocitos WT pueden rescatar gran parte de la disfunción de las neuronas ASD (Fig. 1). Los astrocitos tienen funciones importantes en el desarrollo del cerebro al secretar factores que regulan la supervivencia neuronal, el crecimiento de dendritas, la formación de sinapsis y la función de la red neuronal. Nuestro laboratorio tiene una amplia experiencia en la identificación y caracterización de los factores secretados por astrocitos en el desarrollo normal del cerebro, y estamos aplicando este conocimiento para identificar alteraciones centrales en la secreción de astrocitos responsables de los defectos que se encuentran en múltiples tipos de ASD.
Hipótesis
Presumimos que múltiples formas de ASD comparten defectos comunes en la secreción de astrocitos de factores de apoyo neuronal, y que estos defectos afectan la maduración neuronal y constituyen un nuevo objetivo para la intervención terapéutica en múltiples formas de ASD.
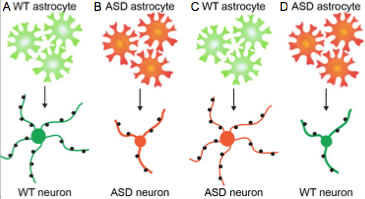 Figura 1. Los astrocitos contribuyen a la patología del TEA. A. Los astrocitos WT (verde) secretan factores que promueven el desarrollo de neuronas sanas (verde): la neurona tiene un cuerpo celular central grande, extiende muchos procesos dendríticos largos y delgados y recibe numerosas conexiones siápticas (negro). B. Cuando los astrocitos ASD (rojo) se cultivan con neuronas ASD (rojo), el desarrollo neuronal se ve afectado; la neurona tiene un cuerpo celular más pequeño, extiende menos procesos dendríticos que son gruesos y atrofiados, y recibe menos conexiones sinápticas. C. Los astrocitos WT liberan factores que son suficientes para rescatar el fenotipo de las neuronas ASD. D. Los astrocitos ASD liberan factores que son suficientes para impedir el desarrollo de las neuronas WT.
Para probar esta hipótesis tenemos:
1) Desarrolló un protocolo para purificar y cultivar astrocitos del cerebro de ratón postnatal, en condiciones libres de suero para prevenir la inducción de genes inflamatorios. 2) Determinó que las proteínas secretadas por estos astrocitos son suficientes para mantener la supervivencia neuronal y procesar el crecimiento in vitro 3) Usó espectrometría de masas para identificar el complemento completo de proteínas secretadas por astrocitos, una lista de ~ 2000 4) Usó secuenciación de ARN para identificar astrocitos- genes expresados, y si la expresión génica se correlaciona con el nivel de proteína. Ahora estamos aplicando estos métodos a los astrocitos de múltiples modelos de ASD, para identificar proteínas secretadas de manera diferencial que son candidatas para el impacto negativo de los astrocitos de ASD en las neuronas WT. Se evaluará la capacidad de estos candidatos para regular la supervivencia neuronal, el desarrollo de procesos neuronales y la formación de sinapsis mediante ensayos in vitro. Este análisis de la secreción de astrocitos, tanto en la salud como en los TEA, proporcionará el primer análisis completo del secretoma de los astrocitos e identificará objetivos novedosos para futuros objetivos terapéuticos en los TEA.
Figura 1. Los astrocitos contribuyen a la patología del TEA. A. Los astrocitos WT (verde) secretan factores que promueven el desarrollo de neuronas sanas (verde): la neurona tiene un cuerpo celular central grande, extiende muchos procesos dendríticos largos y delgados y recibe numerosas conexiones siápticas (negro). B. Cuando los astrocitos ASD (rojo) se cultivan con neuronas ASD (rojo), el desarrollo neuronal se ve afectado; la neurona tiene un cuerpo celular más pequeño, extiende menos procesos dendríticos que son gruesos y atrofiados, y recibe menos conexiones sinápticas. C. Los astrocitos WT liberan factores que son suficientes para rescatar el fenotipo de las neuronas ASD. D. Los astrocitos ASD liberan factores que son suficientes para impedir el desarrollo de las neuronas WT.
Para probar esta hipótesis tenemos:
1) Desarrolló un protocolo para purificar y cultivar astrocitos del cerebro de ratón postnatal, en condiciones libres de suero para prevenir la inducción de genes inflamatorios. 2) Determinó que las proteínas secretadas por estos astrocitos son suficientes para mantener la supervivencia neuronal y procesar el crecimiento in vitro 3) Usó espectrometría de masas para identificar el complemento completo de proteínas secretadas por astrocitos, una lista de ~ 2000 4) Usó secuenciación de ARN para identificar astrocitos- genes expresados, y si la expresión génica se correlaciona con el nivel de proteína. Ahora estamos aplicando estos métodos a los astrocitos de múltiples modelos de ASD, para identificar proteínas secretadas de manera diferencial que son candidatas para el impacto negativo de los astrocitos de ASD en las neuronas WT. Se evaluará la capacidad de estos candidatos para regular la supervivencia neuronal, el desarrollo de procesos neuronales y la formación de sinapsis mediante ensayos in vitro. Este análisis de la secreción de astrocitos, tanto en la salud como en los TEA, proporcionará el primer análisis completo del secretoma de los astrocitos e identificará objetivos novedosos para futuros objetivos terapéuticos en los TEA.
 Figura 1. Los astrocitos contribuyen a la patología del TEA. A. Los astrocitos WT (verde) secretan factores que promueven el desarrollo de neuronas sanas (verde): la neurona tiene un cuerpo celular central grande, extiende muchos procesos dendríticos largos y delgados y recibe numerosas conexiones siápticas (negro). B. Cuando los astrocitos ASD (rojo) se cultivan con neuronas ASD (rojo), el desarrollo neuronal se ve afectado; la neurona tiene un cuerpo celular más pequeño, extiende menos procesos dendríticos que son gruesos y atrofiados, y recibe menos conexiones sinápticas. C. Los astrocitos WT liberan factores que son suficientes para rescatar el fenotipo de las neuronas ASD. D. Los astrocitos ASD liberan factores que son suficientes para impedir el desarrollo de las neuronas WT.
Figura 1. Los astrocitos contribuyen a la patología del TEA. A. Los astrocitos WT (verde) secretan factores que promueven el desarrollo de neuronas sanas (verde): la neurona tiene un cuerpo celular central grande, extiende muchos procesos dendríticos largos y delgados y recibe numerosas conexiones siápticas (negro). B. Cuando los astrocitos ASD (rojo) se cultivan con neuronas ASD (rojo), el desarrollo neuronal se ve afectado; la neurona tiene un cuerpo celular más pequeño, extiende menos procesos dendríticos que son gruesos y atrofiados, y recibe menos conexiones sinápticas. C. Los astrocitos WT liberan factores que son suficientes para rescatar el fenotipo de las neuronas ASD. D. Los astrocitos ASD liberan factores que son suficientes para impedir el desarrollo de las neuronas WT.
Reparación de conexiones sinápticas después de lesiones como un accidente cerebrovascular – nicolas allen Detalles"
El laboratorio de Allen investiga las vías moleculares que conducen a las conexiones entre las neuronas, conocidas como sinapsis, en el cerebro en desarrollo. Su grupo se centra en las interacciones de señalización entre las neuronas y los astrocitos, una clase de células gliales en forma de estrella. La hipótesis es que los astrocitos juegan un papel crucial en dictar la formación y función de sinapsis a través de la liberación de proteínas específicas que determinan el tipo de sinapsis que se formará y la fuerza de esa sinapsis. Están explorando si estos hallazgos del desarrollo pueden usarse para abordar enfermedades como el accidente cerebrovascular, al promover la reparación de las conexiones sinápticas después de una lesión.
Regulación de Astrocitos de Sinapsis y Circuitos Neuronales – nicolas allen Detalles"
Las sinapsis son puntos esenciales de transferencia de información dentro de los circuitos neuronales, y la correcta formación y maduración de las sinapsis es necesaria para que el cerebro funcione durante toda la vida. Los astrocitos son el tipo de célula más abundante en el cerebro, y muchas sinapsis tienen un proceso de astrocito asociado con ellos. Estudios de referencia en el cerebro en desarrollo han demostrado que los astrocitos secretan señales que pueden inducir la formación de nuevas sinapsis, alterar la fuerza de las sinapsis o provocar la eliminación de las sinapsis existentes. Sin embargo, se desconoce la identidad de todas estas señales y su modo de acción específico. Nuestro laboratorio está trabajando para identificar cómo los astrocitos interactúan y regulan las sinapsis neuronales a lo largo de la vida: en el desarrollo de circuitos neuronales, en la plasticidad sináptica adulta y en la pérdida de sinapsis en el envejecimiento.
- Identificación y caracterización de señales secretadas por astrocitos que regulan el número y la fuerza de las sinapsis neuronales durante el desarrollo
- Determinar qué controla la liberación de factores sinaptogénicos de los astrocitos
- Identificar cómo las alteraciones en la secreción de proteínas de los astrocitos contribuyen al trastorno del espectro autista
- Investigar si los astrocitos en el cerebro adulto limitan la plasticidad sináptica e inhiben el aprendizaje
- Investigar si los astrocitos en el cerebro que envejece contribuyen a la pérdida de sinapsis relacionada con la edad
- Determinar si las señales secretadas por los astrocitos jóvenes se pueden usar para reparar las sinapsis después de una lesión
- Cultivos in vitro de neuronas purificadas y astrocitos purificados, aislados mediante inmunopanning, para identificar nuevas moléculas sinaptogénicas secretadas por astrocitos y diseccionar las vías de señalización que regulan en las neuronas
- RNAseq y espectrometría de masas para identificar el transcriptoma y el secretoma específicos de astrocitos, a lo largo del desarrollo tanto in vitro como in vivo
- Modelos de ratones knock-out específicos de astrocitos para determinar cómo los factores identificados regulan la formación y función de sinapsis y circuitos in vivo
- Enfoques como la electrofisiología para evaluar la fuerza y la plasticidad sináptica, la inmunohistoquímica para evaluar el número de sinapsis y los ensayos conductuales para evaluar el aprendizaje
Optogenética en el tratamiento de la enfermedad de Parkinson – Xin-jin Detalles"
Numerosos trastornos motores y mentales, desde la enfermedad de Parkinson hasta el trastorno obsesivo-compulsivo, se han relacionado con la disfunción de los circuitos de los ganglios basales. El laboratorio de Jin emplea una amplia gama de herramientas, que incluyen comportamiento cuantitativo, genética y optogenética, técnicas fisiológicas y ópticas in vivo para diseccionar los circuitos neuronales y los mecanismos moleculares que subyacen al aprendizaje y la selección de acciones en ratones que se comportan libremente.
Obtención de imágenes de tipos de células neuronales específicas en animales despiertos que se comportan – Axel Nimmerjhan Detalles"
>Las células gliales, el segundo tipo de célula principal en el cerebro, representan aproximadamente el noventa por ciento de las células del cerebro humano y más del cincuenta por ciento del volumen del cerebro. En los últimos años, ha quedado claro que las células gliales realizan contribuciones cruciales a la formación, operación y adaptación de los circuitos neuronales. El trabajo en el laboratorio de Nimmerjahn se centra en la innovación de herramientas microscópicas de luz que permitan el estudio de estas células eléctricamente no excitables y su interacción con otras células en el cerebro intacto de los mamíferos. Han creado herramientas para la tinción y la manipulación genética de tipos de células específicas, para obtener imágenes de la dinámica celular en mamíferos despiertos y en movimiento y para el análisis automatizado de datos de imágenes a gran escala. Este trabajo tiene amplias implicaciones para nuestra visión de las células gliales, la forma en que se procesa la información en el cerebro, la interpretación de las señales de imágenes cerebrales funcionales y el tratamiento de la enfermedad cerebral neurodegenerativa.
Modelo in vitro de mielinización y EM – fred gage Detalles"
Fred "Rusty" Gage es líder mundial en neurogénesis y presidente de la Sociedad Internacional para la Investigación de Células Madre. Ha desarrollado nuevos modelos celulares de enfermedades neurológicas (EM, autismo, Alzheimer, Parkinson) utilizando células madre pluripotentes inducidas por humanos (iPSC) derivadas de pacientes donantes y diferenciadas en tipos de células neuronales específicas. Ha demostrado que estos son útiles para estudiar los mecanismos de la enfermedad, identificar objetivos y detectar compuestos de prueba, y ser más predictivos de los fenotipos de la enfermedad que los modelos actuales. El Dr. Gage también ha desarrollado un modelo de mielinización in vitro usando iPSCs que se utilizará para la detección de compuestos farmacológicos y para comprender mejor enfermedades como la EM.
Resumen del modelo de mielinización:
La mielina es un material eléctricamente aislante que forma una capa de membrana, la vaina de mielina, alrededor del axón de una neurona. Es producido por oligodendrocitos en el sistema nervioso central y células de Schwann en el sistema nervioso periférico. La mielinización aumenta la velocidad de propagación del impulso por conducción saltatoria a través de porciones no aisladas del axón llamadas Nodos de Ranvier. La pérdida de la membrana de mielina, como ocurre en muchos trastornos neurológicos como la esclerosis múltiple, provoca la interrupción de la comunicación eléctrica entre las neuronas y déficits funcionales neuronales permanentes, incluida la pérdida del control motor y el deterioro cognitivo. La esclerosis múltiple por sí sola afecta a más de 400,000 personas en los Estados Unidos ya más de 2.1 millones de personas en todo el mundo. El proceso de mielinización se ha estudiado principalmente con células primarias aisladas, en tejidos post mortem o con modelos animales. Todos los enfoques están restringidos por la variabilidad entre individuos, por las diferencias intrínsecas entre modelos animales y humanos y por el número limitado de células y animales, lo que dificulta los experimentos a gran escala. Las células madre embrionarias (ESC) permiten una población relativamente uniforme de un gran número de células y las células madre pluripotentes inducidas (iPSC) ofrecen la oportunidad de comparar directamente células sanas y de pacientes. Hemos establecido un modelo de mielinización in vitro (en un plato) utilizando oligodendrocitos y neuronas derivados de ESC y iPSC. Nuestro ensayo contribuirá a la comprensión básica de la formación de mielina que conducirá a estrategias de tratamiento refinadas. Debido a la reproducibilidad y confiabilidad, nuestro ensayo propuesto estará disponible para la detección y adaptación de compuestos farmacológicos por parte de otros grupos de investigación para probar sus hipótesis. Actualmente, logramos una formación exitosa de mielina usando ESC de ratón y ya estamos adquiriendo conocimiento sobre la mecánica de la envoltura de mielina.
Oncología
Una pantalla basada en células para identificar compuestos terapéuticos para el cáncer de páncreas – ronald evans Detalles"El estroma desmoplásico es una característica definitoria del adenocarcinoma ductal pancreático (PDAC), la forma más común de cáncer de páncreas, y contribuye a la progresión del tumor y la resistencia a la terapia. Las células estrelladas pancreáticas (PSC) son el tipo de célula principal que causa la reacción desmoplásica. Las PSC quiescentes en un páncreas normal actúan como células de almacenamiento de lípidos con un secretoma limitado, mientras que las PSC activadas en el microambiente tumoral producen una amplia gama de proteínas secretadas implicadas en la progresión del cáncer. El Dr. Evans planteó la hipótesis de que la restauración del fenotipo inactivo de PSC interrumpirá la comunicación entre PSC y las células tumorales y afectará el crecimiento del tumor. Su laboratorio ha desarrollado una pantalla para identificar moléculas pequeñas que revierten las PSC a su fenotipo inactivo utilizando la acumulación de gotas de lípidos como un sello distintivo del estado inactivo.
Inhibidores de ULK1, en combinación con inhibidores de mTOR como terapia citotóxica contra el cáncer – Rubén Shaw Detalles"
La serina-treonina quinasa diana de rapamicina en mamíferos (mTOR) juega un papel importante en la regulación del crecimiento celular y el metabolismo. Dado que la vía mTOR está hiperactivada en una serie de cánceres, se ha propuesto que los inhibidores de mTOR tendrán una amplia aplicación terapéutica en muchos tipos de tumores, y la rapamicina y sus análogos (rapálogos), así como los inhibidores de mTOR competitivos con ATP, se están investigando activamente. perseguidos como candidatos terapéuticos. En 2012, el Instituto Nacional del Cáncer enumeró más de 200 ensayos clínicos que probaron la actividad anticancerígena de estos inhibidores, como monoterapia y como parte de terapias combinadas para muchos tipos de cáncer. Sin embargo, los inhibidores de mTOR como agentes únicos tienen una actividad modesta y se están desarrollando terapias combinadas con la idea de superar la resistencia a la inhibición de mTOR y aumentar la eficacia. Si bien el papel de mTOR en el crecimiento celular es bien conocido, su papel en la autofagia solo se ha identificado recientemente. La autofagia es el proceso celular mediante el cual las células descomponen las proteínas y los orgánulos intracelulares en condiciones de estrés, liberando intermediarios metabólicos y promoviendo la supervivencia celular. El trabajo del Dr. Shaw demostró recientemente que mTOR inactiva un complejo que controla el inicio de la autofagia, compuesto por una quinasa llamada ULK1 (Egan et al., Science 2011). Por lo tanto, la inhibición de mTOR conducirá a la activación de la autofagia, que es una vía importante que promueve la supervivencia celular. La propensión de los inhibidores de mTOR para promover la supervivencia de las células tumorales a través de la autofagia dependiente de ULK1 puede ayudar a explicar por qué los rapálogos son principalmente citostáticos y solo son efectivos como estabilizadores de la enfermedad en lugar de para la regresión. El Dr. Shaw ha postulado que la combinación de la inhibición de ULK1 con el tratamiento con rapamicina podría convertir el efecto citostático estándar de los inhibidores de mTOR en un efecto citotóxico, una vez que se elimine el beneficio de supervivencia de la autofagia iniciada por ULK1. Su laboratorio ha desarrollado una variedad de modelos de ratones inducibles y genéticamente modificados que brindan lecturas biológicas de los regímenes de tratamiento en entornos que predicen los subtipos de cáncer humano. También ha desarrollado una amplia gama de ensayos in vitro para probar hipótesis biológicas en todos los miembros de las vías relevantes y para detectar inhibidores de ULK1. Actualmente está desarrollando inhibidores de molécula pequeña con un colaborador.
Nuevas dianas para el cáncer de mama triple negativo – geoff wahl Detalles"
El trabajo de Geoff Wahl sobre el vínculo entre el desarrollo y el cáncer ha demostrado que los procesos invasivos y proliferativos de la mamogénesis se asemejan a las fases de progresión del cáncer. Los perfiles de expresión de células madre mamarias fetales aisladas (fMaSC) y estroma asociado exhiben sorprendentes similitudes con los perfiles de cáncer de mama triple negativo y Her2+. La expresión génica, el trasplante y los análisis in vitro revelaron mecanismos, incluidas las vías ErbB y FGF, que regulan el crecimiento de fMaSC. Estos y otros candidatos ofrecen potencialmente nuevos objetivos para el diagnóstico, el pronóstico y la terapia del cáncer.
Modelos de ratón de carcinoma de pulmón de células no pequeñas – Rubén Shaw Detalles"
Los modelos de Shaw se basan en un oncogén K-ras inducible expresado en el epitelio del ratón una vez que los ratones inhalan un adenovirus que expresa cre-recombinasa. Su laboratorio cruzó el modelo K-ras con un promotor ubicuo que impulsa la expresión de luciferasa condicional solo en células en las que Cre ha ingresado. De esta manera, derivan una señal de las células tumorales proporcional a la masa tumoral que surge espontáneamente in vivo en el entorno exacto del pulmón y de las lesiones genéticas exactas que se encuentran en el cáncer de pulmón de células no pequeñas (CPCNP) humano. Combinaron los ratones condicionales con luciferasa K-ras con ratones condicionalmente inactivados para el supresor de tumores p53, AMPK, o el supresor de tumores LKB1/STK11. Es importante destacar que K-ras, p53 y LKB1 son los tres genes mutados con mayor frecuencia en el NSCLC humano, y los ratones K-ras p53 (KP) y los ratones K-ras LKB1 (KL) desarrollan carcinomas agresivos constantes dentro de las 8 semanas posteriores a la inhalación de cre. -recombinasa que permite a los científicos probar rigurosamente las terapias en tiempo real en estos modelos.
Observaciones
Pantalla de alto rendimiento para moduladores de interacciones proteína-proteína (PPI) – geoff wahl Detalles"Existen muchos mitos en torno a las dificultades de desarrollar antagonistas de PPI. Como resultado, este enfoque está muy poco explotado, a pesar de que el extenso interactoma humano presenta oportunidades que eclipsan los objetivos farmacológicos actuales. El profesor Wahl y su equipo han desarrollado una plataforma de ensayo basada en células en un formato de alto rendimiento para detectar inhibidores y agonistas de las interacciones proteína-proteína. Esta nueva plataforma de detección combina un sistema de expresión de proteínas inducible con el ensayo de complementación de luciferasa bimolecular (BiLC), lo que permite la interrogación de PPI transitorios y dinámicos, la identificación de nuevos socios de interacción de proteínas intracelulares y la detección y caracterización de antagonistas y agonistas de PPI. . El ensayo se desarrolló inicialmente para detectar inhibidores de p53-MDM2/MDMX en el cáncer, pero es ampliamente aplicable a muchas interacciones proteína-proteína, incluidos los inhibidores de K-Ras.
Disfunción de la neurona motora en la ELA y la atrofia muscular espinal (SMA) – sam pff Detalles"
Un desafío importante en el estudio de SMA ha sido la falta de sistemas modelo apropiados. El Dr. Pfaff ha desarrollado un nuevo modelo de AME basado en células madre embrionarias que fenocopia la patología de la AME humana y puede usarse para estudiar la base de la enfermedad y detectar compuestos que podrían aumentar la supervivencia de las neuronas motoras. A través de estos estudios, ha identificado un nuevo factor de transcripción y una vía asociada que podría generar nuevas vías para la intervención terapéutica en la AME.


