副总统、首席科学官
教授
分子与细胞生物学实验室
唐纳德和达琳·希利主席

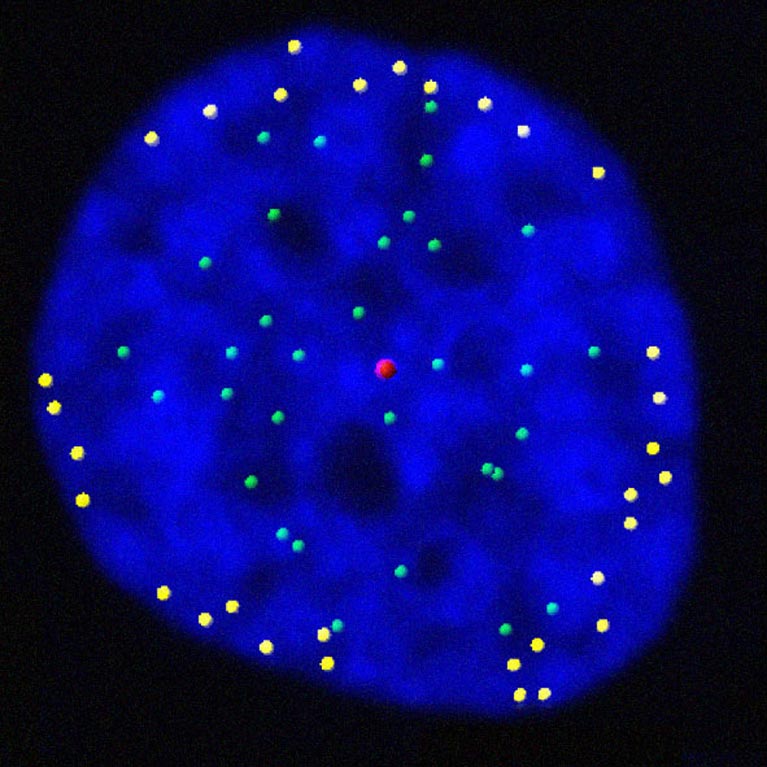
就像每一次复印复印件都会比原始版本稍微模糊一些一样,细胞每一次复制其遗传物质时,染色体末端的细节都会丢失一些。这些被称为端粒的末端最终会被侵蚀,使重要的基因暴露在磨损中,从而阻止细胞生长或导致其死亡。端粒调节重要的增殖边界并限制细胞的生长潜力——从而抑制癌症的形成。.
然而,在许多癌细胞中,端粒会不断地重建,从而赋予细胞永生。类似地,细胞修复DNA损伤的能力会随着年龄的增长而下降,导致突变累积和与年龄相关的疾病。如果科学家能够确定如何阻止这种端粒延长并改善衰老过程中的DNA修复,他们也许能够促使癌细胞死亡或使其更容易受到药物治疗。另一方面,保持端粒完整和改善DNA修复可以治疗早衰综合征。但首先,研究人员需要了解正常端粒功能的复杂细节以及DNA修复的调控机制。.
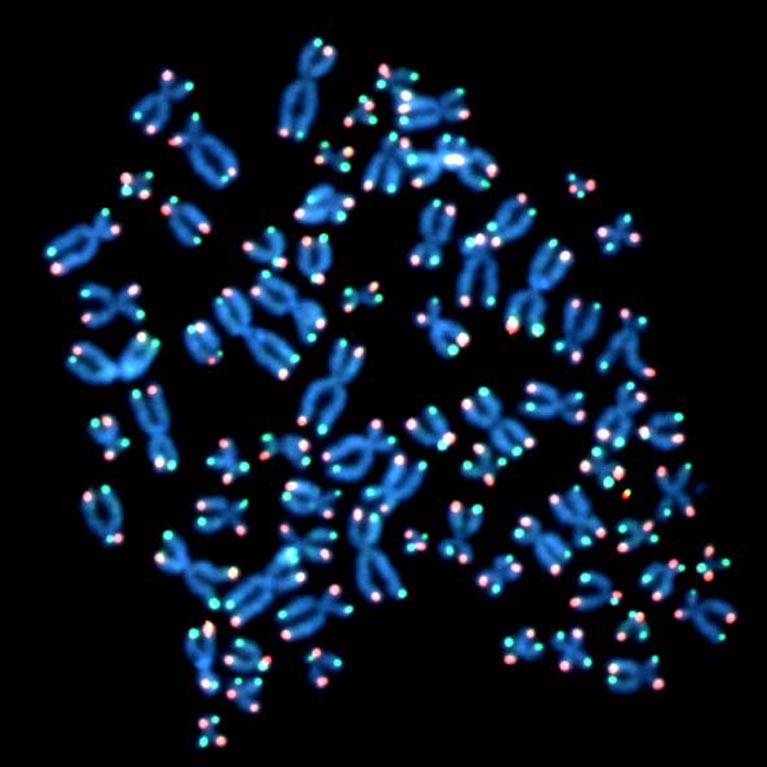
Jan Karlseder研究端粒在细胞增殖周期中的作用——从细胞开始复制其遗传物质到分裂成两个新细胞时,以及在细胞的整个生命周期中——从年轻细胞通过细胞分裂出现到年老细胞永久“退休”(衰老)或死亡时。.
细胞分裂的限制(例如端粒缩短所设定的限制)对于限制不受控制的细胞分裂以及从而预防癌症的形成至关重要。阻止原发性人类细胞癌变的两个基本限制是:复制衰老(一种细胞停止分裂的细胞衰退形式)和危象(一种导致细胞死亡的状态)。尽管这些界限已经存在了几十年,但细胞如何衰老以及当细胞继续分裂而应该衰老时会发生什么仍然不清楚。.
通过发现和清晰地定义调控原生人细胞(例如从活组织检查中提取的细胞)细胞分裂的机制,Karlseder实验室揭示了癌症形成的早期阶段的新通路,这可能带来潜在的干预措施。.
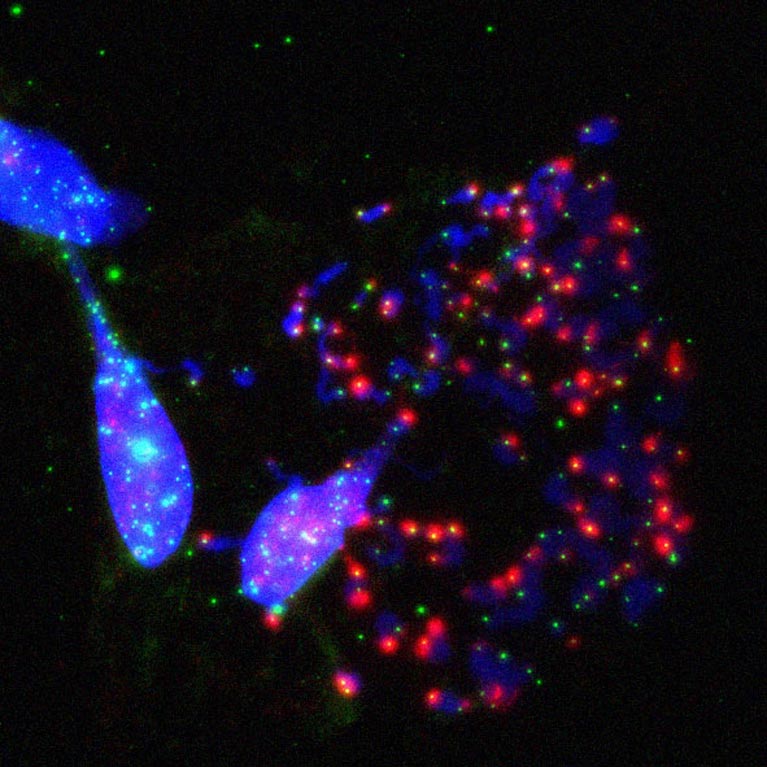
Karlseder实验室发现,危机下的细胞死亡是由细胞回收机制——巨自噬 maquinaria 执行的,这揭示了一条新颖的抗肿瘤通路。.
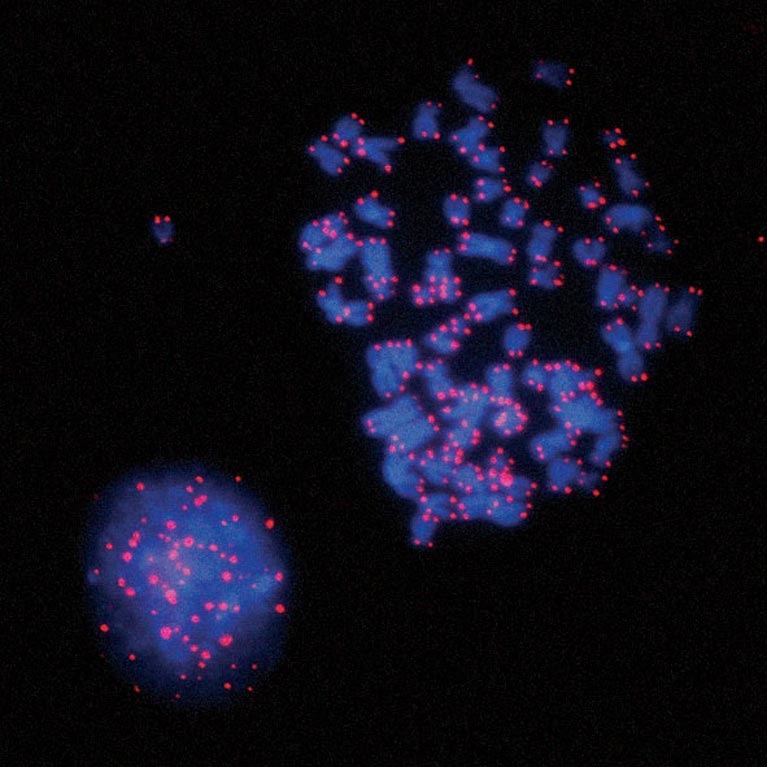
在衰老旁路发生后,端粒进一步缩短,直到染色体融合。Karlseder及其团队发现,这些融合的端粒会激活一个细胞检查点(纺锤体组装),导致有丝分裂停止。在此过程中,损伤信号被放大,并在单个细胞周期内导致细胞死亡。.
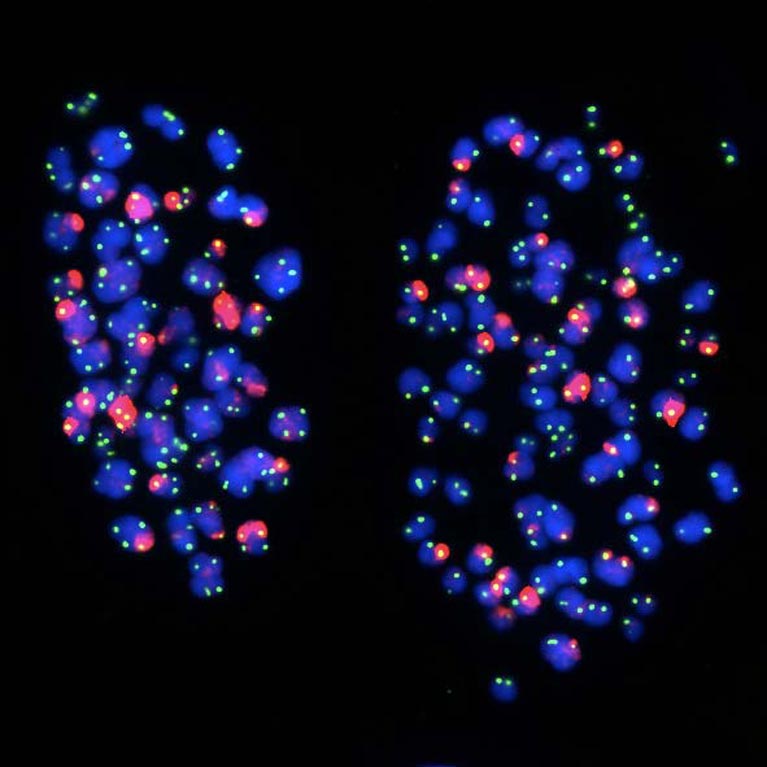
他的实验室发现,端粒在复制后会移动到细胞核的外边缘。这些发现揭示了我们的基因是如何被调控的,以及在细胞分裂过程中基因表达程序是如何改变的,这是理解衰老和由基因突变(如癌症)引起的疾病的重要一步。.
理学士,生物学,因斯布鲁克大学,奥地利
维也纳大学 博士,分子生物学
博士后研究员,洛克菲勒大学,纽约