
9 Julio 2025
Los científicos de Salk descubren un circuito neuronal clave en ratones que le da al dolor su impacto emocional, abriendo nuevas puertas para el tratamiento de la fibromialgia, la migraña y el trastorno de estrés postraumático (TEPT).
LA JOLLA—El dolor no es solo una sensación física, sino que también conlleva una carga emocional. Esa angustia y ansiedad pueden convertir una lesión pasajera en sufrimiento a largo plazo.
Los investigadores del Instituto Salk han identificado un circuito cerebral que da al dolor físico su tono emocional, revelando un nuevo objetivo potencial para el tratamiento de afecciones de dolor crónico y afectivo como la fibromialgia, la migraña y el trastorno de estrés postraumático (TEPT).
Publicado el 9 de julio de 2025 en Actas de la Academia Nacional de Ciencias, el estudio identifica un grupo de neuronas en un área central del cerebro llamada tálamo que parece mediar en el estado emocional o afectivo El lado del dolor en ratones. Esta nueva vía desafía la comprensión tradicional sobre cómo se procesa el dolor en el cerebro y el cuerpo.

“Durante décadas, la opinión predominante fue que el cerebro procesa los aspectos sensoriales y emocionales del dolor a través de vías separadas”, dice el autor principal. cantado han, profesor asociado y titular de la Cátedra de Desarrollo del Fondo Pionero en Salk. «Sin embargo, se ha debatido si la vía sensorial del dolor también podría contribuir al aspecto emocional del dolor. Nuestro estudio proporciona evidencia sólida de que una rama de la vía sensorial del dolor media directamente la experiencia afectiva del dolor».
La sensación física del dolor es lo que te permite detectarlo de inmediato, evaluar su intensidad e identificar su origen. La parte afectiva del dolor es lo que lo hace tan desagradable. Esta incomodidad emocional te motiva a actuar y te ayuda a aprender a asociar los sentimientos negativos con la situación para que puedas evitarla en el futuro.
Esta es una distinción crucial. La mayoría de las personas comienzan a percibir el dolor con las mismas intensidades de estímulo, lo que significa que todos procesamos el lado sensorial del dolor de manera bastante similar. En comparación, nuestra capacidad para... tolerar El dolor varía enormemente. La intensidad con la que sufrimos o nos sentimos amenazados por el dolor depende de nuestro procesamiento afectivo, y si este se vuelve demasiado sensible o se prolonga demasiado, puede provocar un trastorno del dolor. Por ello, es importante comprender qué partes del cerebro controlan estas diferentes dimensiones del dolor.
Se pensaba que el dolor sensorial estaba mediado por el tracto espinotalámico, una vía que envía señales de dolor desde la médula espinal al tálamo, que luego las transmite a áreas de procesamiento sensorial en todo el cerebro.
Generalmente se pensaba que el dolor afectivo estaba mediado por una segunda vía llamada tracto espinoparabranquial, que envía información del dolor desde la médula espinal al tronco encefálico.
Sin embargo, estudios previos con métodos de investigación más antiguos han sugerido que el circuito del dolor podría ser más complejo. Este prolongado debate inspiró a Han y a su equipo a replantear la cuestión con herramientas de investigación modernas.
Utilizando técnicas avanzadas para manipular la actividad de neuronas específicas, los investigadores descubrieron una nueva vía espinotalámica en ratones. En este circuito, las señales de dolor se envían desde la médula espinal a una parte diferente del tálamo, que tiene conexiones con la amígdala, el centro de procesamiento emocional del cerebro. Este grupo particular de neuronas en el tálamo puede identificarse por su expresión de CGRP (péptido relacionado con el gen de la calcitonina), un neuropéptido descubierto originalmente en el profesor... ronald evans' laboratorio en Salk.
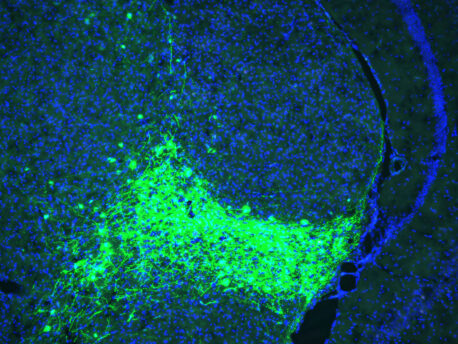
Cuando los investigadores desactivaron (silenciaron genéticamente) estas neuronas CGRP, los ratones siguieron reaccionando a estímulos de dolor leve, como calor o presión, lo que indica que su procesamiento sensorial estaba intacto. Sin embargo, no parecieron asociar sentimientos negativos persistentes con estas situaciones, y no mostraron ningún comportamiento aprendido de miedo o evitación en ensayos posteriores. Por otro lado, cuando estas mismas neuronas se activaron optogenéticamente, los ratones mostraron signos claros de angustia y aprendieron a evitar esa zona, incluso sin estímulos de dolor.
“El procesamiento del dolor no se trata solo de que los nervios lo detecten; se trata de que el cerebro decida qué tan importante es ese dolor”, afirma el primer autor, Sukjae Kang, investigador asociado sénior en el laboratorio de Han. “Comprender la biología subyacente a estos dos procesos distintos nos ayudará a encontrar tratamientos para los tipos de dolor que no responden a los fármacos tradicionales”.
Muchas afecciones de dolor crónico, como la fibromialgia y la migraña, implican experiencias de dolor prolongadas, intensas y desagradables, a menudo sin una causa física o lesión evidente. Algunos pacientes también reportan una sensibilidad extrema a estímulos comunes como la luz, el sonido o el tacto, que otros no percibirían como dolorosos.
Han afirma que la sobreactivación de la vía espinotalámica del CGRP podría contribuir a estas afecciones al provocar que el cerebro malinterprete o reaccione exageradamente a las entradas sensoriales. De hecho, el análisis transcriptómico de las neuronas del CGRP mostró que expresan muchos de los genes asociados con la migraña y otros trastornos del dolor.
Cabe destacar que varios bloqueadores del CGRP ya se utilizan para tratar las migrañas. Este estudio podría ayudar a explicar la eficacia de estos medicamentos y podría inspirar nuevos tratamientos no adictivos para los trastornos de dolor afectivo.
Han también ve una posible relevancia para afecciones psiquiátricas que implican una mayor percepción de amenazas, como el TEPT. La creciente evidencia de su laboratorio sugiere que la vía afectiva del dolor CGRP actúa como parte del sistema de alarma más amplio del cerebro, detectando y respondiendo no solo al dolor, sino también a una amplia gama de sensaciones desagradables. La inhibición de esta vía con bloqueadores del CGRP podría ofrecer un nuevo enfoque para aliviar el miedo, la evitación y la hipervigilancia en los trastornos relacionados con el trauma.
Es importante destacar que la relación entre la vía CGRP y el dolor psicológico asociado con experiencias sociales como el duelo, la soledad y la angustia sigue sin estar clara y requiere más estudios.
“Nuestro descubrimiento de la vía del dolor afectivo CGRP nos da una explicación a nivel molecular y de circuito para la diferencia entre detector dolor físico y sufrimiento "De ello", dice Han. "Estamos entusiasmados por seguir explorando esta vía y posibilitando futuras terapias que puedan reducir este sufrimiento".
Otros autores incluyen a Shijia Liu, Jong-Hyun Kim, Dong-Il Kim, Tae Gyu Oh, Jiahang Peng, Mao Ye, Kuo-Fen Lee, Ronald M. Evans y Martyn Goulding de Salk.
El trabajo fue apoyado por los Institutos Nacionales de Salud Mental (subvención BRAINS 1R01MH116203) y la Fundación Simons (premio Puente a la Independencia SFARI #388708).
DOI: https://doi.org/10.1073/pnas.2505889122
REVISTA
Actas de la Academia Nacional de Ciencias
AUTORES
Sukjae J. Kang, Shijia Liu, Jong-Hyun Kim, Dong-Il Kim, Tae Gyu Oh, Jiahang Peng, Mao Ye, Kuo-Fen Lee, Ronald M. Evans, Martyn Goulding, Sung Han
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
El Instituto Salk es un instituto de investigación independiente y sin fines de lucro fundado en 1960 por Jonas Salk, creador de la primera vacuna segura y eficaz contra la polio. Su misión es impulsar una investigación fundamental, colaborativa y arriesgada que aborde los desafíos más urgentes de la sociedad, como el cáncer, el Alzheimer y la vulnerabilidad agrícola. Esta ciencia fundamental sustenta todos los esfuerzos translacionales, generando conocimientos que facilitan el desarrollo de nuevos medicamentos e innovaciones en todo el mundo.