
25 Agosto 2010
LA JOLLA, CA—Un nuovo meccanismo utilizzato dall'adenovirus per eludere il programma suicida della cellula potrebbe contribuire notevolmente a spiegare come i geni soppressori dei tumori vengono silenziati nelle cellule tumorali e aprire la strada a un nuovo tipo di terapia mirata contro il cancro, riferiscono i ricercatori del Salk Institute for Biological Studies nel numero del 26 agosto 2010 di Nature.
Quando una cellula è sotto stress, il soppressore tumorale p53 entra in azione, attivando un esercito di "soldati" che innescano un meccanismo di "autodistruzione" intrinseco che elimina dall'organismo le cellule infette da virus o comunque anomale. Proprio come le cellule tumorali, gli adenovirus, che causano infezioni delle vie respiratorie superiori, hanno bisogno di eliminare p53 per moltiplicarsi con successo.
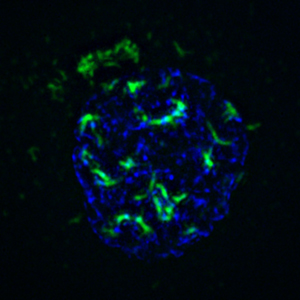
La minuscola proteina dell'adenovirus nota come ORF3 (mostrata in verde) apre la strada alla replicazione dell'adenovirus creando "file zip" di geni che aiutano la cellula a difendersi dal virus. O'Shea spera di sfruttare questa scoperta per creare adenovirus che distruggano selettivamente le cellule tumorali.
Immagine: per gentile concessione della Dott.ssa Clodagh O'Shea, Salk Institute for Biological Studies
“Invece di inattivare direttamente p53, l’adenovirus rende impotente il ‘guardiano del genoma’ prendendo di mira il genoma stesso”, spiega Clodagh O'Shea, Ph.D., professore associato presso il Laboratorio di Biologia Molecolare e Cellulare, che ha guidato lo studio. "Crea letteralmente file zip dei geni bersaglio di p53, comprimendoli fino a renderli illeggibili."
Il pathway oncosoppressore p53 è inattivato in quasi tutti i tumori umani, consentendo alle cellule di sfuggire ai normali controlli di crescita. Tuttavia, non esiste ancora una terapia oncologica mirata e razionale per trattare i pazienti che si basa sulla perdita di p53.
"Tutte le terapie mirate di cui disponiamo si basano su piccole molecole che inattivano gli oncogeni, ma il cancro non è causato solo dall'acquisizione di geni che promuovono la crescita", afferma O'Shea. "La perdita di oncosoppressori è altrettanto importante. La grande domanda è: come si può colpire qualcosa che non c'è più?"
L'adenovirus sembrava fornire la risposta. Porta con sé una proteina virale, E1B-55K, che lega e degrada p53 nelle cellule infette. Senza E1B-55K per inattivare p53, l'adenovirus dovrebbe essere in grado di replicarsi solo nelle cellule tumorali con deficit di p53. Quindi, ogni volta che rompe la cellula ospite per rilasciare migliaia di progenie virali, la generazione successiva di virus è pronta a cercare le cellule tumorali rimanenti, lasciando intatte le cellule sane.
"Questo rende l'adenovirus un candidato perfetto per la terapia oncolitica del cancro", afferma O'Shea. "Sebbene questi virus abbiano svolto il loro compito, con sorpresa di tutti, le risposte dei pazienti non erano correlate allo stato di p53 dei loro tumori", afferma O'Shea. Incuriosita, lei e il suo team hanno proseguito su questa scoperta inaspettata.
Conrado Soria, Ph.D., assistente di ricerca e co-autore principale dello studio, si è reso conto rapidamente che E1B-55K era solo metà della storia. "L'incapacità del virus mutante E1B-55K di replicarsi nelle cellule normali non era dovuta al fatto che il virus non fosse riuscito a degradare p53", spiega.
Nelle cellule normali non sottoposte a stress, p53 si trova solo a bassi livelli a causa della rapida degradazione. In risposta al danno al DNA, all'attivazione di oncogeni o all'infezione da virus a DNA, la degradazione di p53 si arresta e, di conseguenza, i livelli della proteina p53 si accumulano. Questo aumento attiva i geni bersaglio di p53, che arrestano il ciclo cellulare o inducono l'apoptosi.
Proprio come previsto, p53 iniziò ad accumularsi nelle cellule normali infettate da adenovirus privo di E1B-55K, ma non era ancora in grado di attivare i suoi geni bersaglio e avviare la cellula verso l'apoptosi. Alla fine ne scoprì il motivo: l'adenovirus porta con sé un'altra proteina, E4-ORF3, che neutralizza il checkpoint di p53 attraverso un meccanismo completamente diverso.
Invece di inattivare direttamente p53, la minuscola proteina impedisce al soppressore tumorale di legarsi ai suoi geni bersaglio nel genoma modificando la cromatina, il denso complesso istone/DNA che mantiene tutto ben organizzato all'interno del nucleo cellulare. "Queste modifiche causano la condensazione di parti dei cromosomi nella cosiddetta eterocromatina, seppellendo in profondità le regioni regolatrici dei geni bersaglio di p53", afferma la studentessa laureata e co-prima autrice Fanny E. Estermann. "Con l'accesso negato, p53 non è in grado di innescare l'apoptosi".
O'Shea spera di sfruttare queste nuove conoscenze per comprendere come alti livelli di p53 wild type possano essere inattivati nel cancro, nonché i meccanismi che inducono il silenziamento anomalo dei loci dei geni oncosoppressori nelle cellule tumorali. "Il nostro studio cambia davvero la definizione di lunga data di come p53 viene inattivato nelle cellule infettate da adenovirus e ci consentirà finalmente di sviluppare vere e proprie terapie oncolitiche selettive per p53".
Il lavoro è stato finanziato in parte dall'Alliance of Cancer Gene Therapy, dall'American Cancer Society, dalla Sontag Foundation, dalla Beckman Foundation e dal National Cancer Institute.
Informazioni sul Salk Institute for Biological Studies
Il Salk Institute for Biological Studies è uno dei più importanti istituti di ricerca di base al mondo, dove docenti di fama internazionale affrontano questioni fondamentali delle scienze della vita in un ambiente unico, collaborativo e creativo. Concentrati sia sulla scoperta che sulla formazione delle future generazioni di ricercatori, gli scienziati del Salk forniscono contributi innovativi alla nostra comprensione di cancro, invecchiamento, Alzheimer, diabete e malattie infettive, studiando neuroscienze, genetica, biologia cellulare e vegetale e discipline correlate.
I risultati conseguiti dal corpo docente sono stati riconosciuti con numerosi riconoscimenti, tra cui premi Nobel e l'iscrizione alla National Academy of Sciences. Fondato nel 1960 dal pioniere del vaccino contro la poliomielite Jonas Salk, l'Istituto è un'organizzazione indipendente senza scopo di lucro e un punto di riferimento architettonico.
Il Salk Institute celebra con orgoglio cinque decenni di eccellenza scientifica nella ricerca di base.
Ufficio delle comunicazioni
Tel: (858) 453-4100
press@salk.edu