
9 Agosto 2009
LA JOLLA, CA—Uno studio collaborativo condotto dai ricercatori del Salk Institute for Biological Studies ha scoperto che il soppressore tumorale p53, noto come "guardiano del genoma", non solo blocca sul nascere le cellule che potrebbero diventare cancerose, ma controlla anche la riprogrammazione delle cellule somatiche.
Sebbene gli scienziati abbiano imparato a riprogrammare cellule umane adulte, come quelle della pelle, trasformandole in cosiddette cellule staminali pluripotenti indotte (iPSC), l'efficienza della riprogrammazione è ancora tristemente bassa. Lo studio di Salk, pubblicato nell'edizione online anticipata del 9 agosto di Nature, fornisce una nuova comprensione del motivo per cui solo poche cellule su molte possono essere convinte a tornare indietro nel tempo.

Dott. Juan-Carlos Izpisúa Belmonte e Dott. Geoffrey M. Wahl
"Sebbene siamo in grado di riprogrammare cellule specializzate da un po' di tempo, non si sapeva nulla sui meccanismi di controllo che impediscono che ciò accada spontaneamente nel corpo e sul perché sia stato così difficile cambiare il loro destino in una capsula di Petri", afferma Juan-Carlos Izpisúa Belmonte, Ph.D., professore presso il Gene Expression Laboratory, che ha lavorato a stretto contatto con Geoffrey M. Wahl, Ph.D., anche professore presso il Gene Expression Laboratory.
Le loro scoperte avvicinano la tecnologia iPSC alla realizzazione della sua promessa di essere una fonte di cellule staminali specifiche per il paziente, ma costringono anche gli scienziati a riconsiderare lo sviluppo del cancro.
"Per decenni si è pensato che il cancro nascesse dalla de-differenziazione di cellule completamente impegnate e specializzate, ma alla fine è stata abbandonata in favore della teoria delle cellule staminali tumorali, attualmente in voga", afferma Wahl. "Ora che sappiamo che p53 previene la de-differenziazione, credo sia giunto il momento di riconsiderare la possibilità che la riprogrammazione svolga un ruolo nello sviluppo del cancro, poiché praticamente tutte le cellule tumorali perdono la funzione di p53 in un modo o nell'altro".
Man mano che gli embrioni dei mammiferi attraversano una serie di fasi di sviluppo, le scelte di cellule staminali embrionali, che godono di prospettive pressoché illimitate, si riducono progressivamente fino a dare origine ai circa 200 tipi di cellule che compongono il nostro corpo e che generalmente non hanno la capacità di tornare a una fase meno specializzata.
Sebbene la differenziazione sia generalmente irreversibile, gli scienziati hanno sviluppato diversi metodi per superare la riluttanza delle cellule a essere riprogrammate. La tecnologia più utilizzata prevede l'espressione forzata di quattro fattori di trascrizione - Oct4, Sox2, Klf4 e c-Myc - in cellule adulte completamente impegnate.
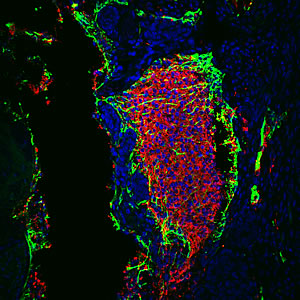
La riduzione dell'attività di p53 aumenta l'efficienza di riprogrammazione delle cellule somatiche adulte, richiedendo solo due fattori di riprogrammazione invece dei soliti quattro.
Immagine: per gentile concessione del Dott. Juan-Carlos Belmonte, Salk Institute for Biological Studies
"Purtroppo, Klf4 e c-Myc sono oncogeni e la loro aggiunta comporta il rischio di indurre il cancro", afferma Belmonte. Eppure, nonostante la spinta aggiuntiva fornita da questi potenti oncogeni, solo una piccola frazione si trasforma in iPSC che hanno l'aspetto e il comportamento di cellule staminali embrionali, portando Belmonte a chiedersi se ciò che stavano facendo per indurre le cellule a riprogrammarsi inducesse una risposta che ne impedisse la crescita?
Una conversazione con il suo vicino di casa, l'esperto di cancro Wahl, ha fornito alcune nuove idee che potrebbero essere testate in laboratorio. "Normalmente, le cellule non si riprogrammano, quindi deve esserci un meccanismo che lo impedisca", afferma Wahl. "Sapevamo che c-Myc e alcuni degli altri geni necessari per la riprogrammazione attivano il soppressore tumorale p53 e ci siamo chiesti se avesse un ruolo in questo processo".
E in effetti, gli esperimenti condotti dai ricercatori post-dottorato e co-primi autori Teruhisa Kawamura, Ph.D., e Jotaro Suzuki, Ph.D., hanno rivelato che l'aggiunta dei fattori di riprogrammazione c-Myc e Klf4, da soli o in varie combinazioni, attivava il pathway p53. Come primo soccorritore, il soppressore tumorale p53 entra in azione quando le cellule si trovano in condizioni di stress. A seconda della situazione, p53 attiva quindi geni che bloccano la divisione cellulare per dare il tempo alle riparazioni o, quando tutti i tentativi di salvataggio si rivelano vani, ordinano alla cellula di smettere di dividersi per sempre o di suicidarsi.
Nelle cellule geneticamente modificate per essere prive di p53, l'efficienza della riprogrammazione è stata almeno 10 volte maggiore rispetto alle cellule di controllo, dimostrando chiaramente che p53 ha svolto un ruolo importante nel controllare le cellule che cercavano di tornare a uno stato simile a quello staminale.
Poiché le iPSC generate con l'intero corredo di fattori di riprogrammazione corrono il rischio di diventare maligne, Belmonte e il suo team volevano scoprire se le cellule di topo prive di p53 potessero essere riprogrammate utilizzando solo due fattori, Oct4 e Sox2. Le cellule si sono rapidamente convertite in iPSC e hanno dato origine a topi sani e a termine, in grado di riprodursi superando il test definitivo per le cellule staminali embrionali pluripotenti.
"Questa collaborazione di grande successo è un ottimo esempio di ciò che rende il Salk un posto così speciale", afferma Wahl. "Juan Carlos e io parliamo ogni giorno e affrontiamo la stessa questione da prospettive molto diverse. Lui proviene da una prospettiva di biologia dello sviluppo, mentre io da quella del cancro, ma quando mettiamo insieme possono dare vita a una storia fantastica".
Per informazioni sulla commercializzazione di questa tecnologia, contattare l'ufficio di gestione e sviluppo tecnologico di Salk al numero (858) 453-4100, interno 1278.
Questo lavoro è stato sostenuto dai National Institutes of Health, da sovvenzioni di Tercel, Marato, dalla G. Harold and Leila Y. Mathers Charitable Foundation e dalla Fundacion Cellex.
Tra i ricercatori che hanno contribuito al lavoro figurano Yunyuan V. Wang, Ph.D. del laboratorio Wahl, Sergio Menendez, Ph.D., Laura Batlle Morera, Ph.D., e Angel Raya, Ph.D., tutti presso il Centro di Medicina Rigenerativa di Barcellona, in Spagna.
Informazioni sul Salk Institute for Biological Studies:
Il Salk Institute for Biological Studies è uno dei più importanti istituti di ricerca di base al mondo, dove docenti di fama internazionale affrontano questioni fondamentali delle scienze della vita in un ambiente unico, collaborativo e creativo. Concentrati sia sulla scoperta che sulla formazione delle future generazioni di ricercatori, gli scienziati del Salk forniscono contributi innovativi alla nostra comprensione di cancro, invecchiamento, Alzheimer, diabete e disturbi cardiovascolari, studiando neuroscienze, genetica, biologia cellulare e vegetale e discipline correlate.
I risultati conseguiti dal corpo docente sono stati riconosciuti con numerosi riconoscimenti, tra cui premi Nobel e l'iscrizione alla National Academy of Sciences. Fondato nel 1960 dal pioniere del vaccino contro la poliomielite Jonas Salk, l'Istituto è un'organizzazione indipendente senza scopo di lucro e un punto di riferimento architettonico.
Ufficio delle comunicazioni
Tel: (858) 453-4100
press@salk.edu