
30 aprile 2015
I risultati dello studio del Salk Institute sulla sindrome da invecchiamento precoce potrebbero portare a un modo per rallentare o invertire il processo di invecchiamento
I risultati dello studio del Salk Institute sulla sindrome da invecchiamento precoce potrebbero portare a un modo per rallentare o invertire il processo di invecchiamento
LA JOLLA–Uno studio che collega il processo di invecchiamento al deterioramento di fasci di DNA cellulare strettamente impacchettati potrebbe portare a metodi di prevenzione e trattamento di malattie legate all'età come cancro, diabete e morbo di Alzheimer, come dettagliato il 30 aprile 2015, in Scienze.
Nello studio, gli scienziati del Salk Institute e del Accademia cinese delle scienze hanno scoperto che le mutazioni genetiche alla base della sindrome di Werner, un disturbo che porta all'invecchiamento precoce e alla morte, hanno causato il deterioramento di fasci di DNA noti come eterocromatina.
La scoperta, resa possibile grazie alla combinazione di tecnologie all'avanguardia nel campo delle cellule staminali e dell'editing genetico, potrebbe portare a metodi per contrastare il declino fisiologico legato all'età, prevenendo o invertendo i danni all'eterocromatina.
"I nostri risultati mostrano che la mutazione genetica che causa la sindrome di Werner provoca la disorganizzazione dell'eterocromatina e che questa interruzione del normale impacchettamento del DNA è un fattore chiave dell'invecchiamento", afferma Juan Carlos Izpisua Belmonte, autore senior dello studio. "Questo ha implicazioni che vanno oltre la sindrome di Werner, poiché identifica un meccanismo centrale dell'invecchiamento – la disorganizzazione dell'eterocromatina – che ha dimostrato di essere reversibile."
La sindrome di Werner è una malattia genetica che causa un invecchiamento più rapido del normale. Colpisce circa una persona su 200,000 negli Stati Uniti. Le persone affette da questa malattia soffrono precocemente di malattie legate all'età, tra cui cataratta, diabete di tipo 2, indurimento delle arterie, osteoporosi e cancro, e la maggior parte muore tra i 40 e i 50 anni.
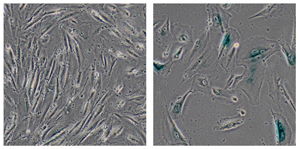
I ricercatori del Salk Institute hanno scoperto che una proteina mutata nella sindrome di Werner, un disturbo dell'invecchiamento precoce, svolge un ruolo chiave nella stabilizzazione dell'eterocromatina, una forma di DNA strettamente impacchettata. Più in generale, i risultati suggeriscono che la disorganizzazione dell'eterocromatina potrebbe essere un fattore chiave dell'invecchiamento. Questa immagine mostra cellule umane normali (a sinistra) e cellule geneticamente modificate sviluppate dagli scienziati del Salk Institute per modellare la sindrome di Werner (a destra), che mostravano segni di invecchiamento, tra cui le loro grandi dimensioni.
CLICCA QUI per un'immagine ad alta risoluzione.
Immagine: per gentile concessione del Salk Institute for Biological Studies
La malattia è causata da una mutazione del gene RecQ elicasi-simile della sindrome di Werner, noto come gene WRN in breve, che genera la proteina WRN. Studi precedenti hanno dimostrato che la forma normale della proteina è un enzima che mantiene la struttura e l'integrità del DNA di una persona. Quando la proteina è mutata nella sindrome di Werner, interrompe la replicazione e la riparazione del DNA e l'espressione dei geni, il che si pensava causasse l'invecchiamento precoce. Tuttavia, non era chiaro esattamente come la proteina WRN mutata interrompesse questi processi cellulari critici.
Nel loro studio, gli scienziati del Salk hanno cercato di determinare con precisione in che modo la proteina WRN mutata causi così tanto caos cellulare. Per farlo, hanno creato un modello cellulare della sindrome di Werner utilizzando una tecnologia di editing genetico all'avanguardia per eliminare il gene WRN nelle cellule staminali umane. Questo modello di cellule staminali della malattia ha offerto agli scienziati la possibilità senza precedenti di studiare cellule che invecchiano rapidamente in laboratorio. Le cellule risultanti imitavano la mutazione genetica osservata nei pazienti affetti da sindrome di Werner, quindi le cellule hanno iniziato a invecchiare più rapidamente del normale. A un esame più attento, gli scienziati hanno scoperto che l'eliminazione del gene WRN portava anche a alterazioni della struttura dell'eterocromatina, il DNA compattato presente nel nucleo di una cellula.
Questo raggruppamento di DNA funge da centralino per il controllo dell'attività dei geni e dirige il complesso meccanismo molecolare di una cellula. All'esterno dei fasci di eterocromatina si trovano marcatori chimici, noti come tag epigenetici, che controllano la struttura dell'eterocromatina. Ad esempio, alterazioni di questi interruttori chimici possono modificare l'architettura dell'eterocromatina, determinando l'espressione o il silenziamento di determinati geni.

Da sinistra: Pradeep Reddy, Concepcion Rodriguez Esteban, Emi Suzuki, Mo Li, Juan Carlos Izpisua Belmonte, Alejandro Ocampo, Keiichiro Suzuki
CLICCA QUI per un'immagine ad alta risoluzione.
Immagine: per gentile concessione del Salk Institute for Biological Studies
I ricercatori del Salk hanno scoperto che la delezione del gene WRN porta alla disorganizzazione dell'eterocromatina, indicando un ruolo importante della proteina WRN nel mantenimento dell'eterocromatina. E, in effetti, in ulteriori esperimenti, hanno dimostrato che la proteina interagisce direttamente con strutture molecolari note per stabilizzare l'eterocromatina, rivelando una sorta di prova schiacciante che, per la prima volta, collega direttamente la proteina WRN mutata alla destabilizzazione dell'eterocromatina.
"Il nostro studio collega i punti tra la sindrome di Werner e la disorganizzazione dell'eterocromatina, delineando un meccanismo molecolare attraverso il quale una mutazione genetica porta a un'interruzione generale dei processi cellulari, alterando la regolazione epigenetica", afferma Izpisua Belmonte. "Più in generale, suggerisce che le alterazioni accumulate nella struttura dell'eterocromatina possano essere una delle principali cause dell'invecchiamento cellulare. Questo solleva la questione se possiamo invertire queste alterazioni, come ristrutturare una vecchia casa o un'auto, per prevenire, o addirittura invertire, il declino e le malattie legate all'età".
Izpisua Belmonte ha aggiunto che saranno necessari studi più approfonditi per comprendere appieno il ruolo della disorganizzazione dell'eterocromatina nell'invecchiamento, incluso il modo in cui interagisce con altri processi cellulari implicati nell'invecchiamento, come l'accorciamento delle estremità dei cromosomi, noti come telomeri. Inoltre, il team di Izpisua Belmonte sta sviluppando tecnologie di editing epigenetico per invertire le alterazioni epigenetiche che hanno un ruolo nell'invecchiamento e nelle malattie umane.
Altri autori dell'articolo includono: Weiqi Zhang, Jingyi Li, Keiichiro Suzuki, Jing Qu, Ping Wang, Junzhi Zhou, Xiaomeng Liu, Ruotong Ren, Xiuling Xu, Alejandro Ocampo, Tingting Yuan, Jiping Yang, Ying Li, Liang Shi, Dee Guan, Huize Pan, Shunlei Duan, Zhichao Ding, Mo Li, Fei Yi, Ruijun Bai, Yayu Wang, Chang Chen, Fuquan Yang, Xiaoyu Li, Zimei Wang, Emi Aizawa, April Goebl, Rupa Devi Soligalla, Pradeep Reddy, Concepcion Rodriguez Esteban, Fuchou Tang e Guang-Hui Liu.
Il finanziamento per lo studio è stato fornito da Fondazione Glenn, l' Fondazione di beneficenza G. Harold e Leila Y. Mathers e Leona M. e Harry B. Helmsley Charitable Trust.
Informazioni sul Salk Institute for Biological Studies:
Il Salk Institute for Biological Studies è uno dei più importanti istituti di ricerca di base al mondo, dove docenti di fama internazionale affrontano questioni fondamentali delle scienze della vita in un ambiente unico, collaborativo e creativo. Concentrati sia sulla scoperta che sulla formazione delle future generazioni di ricercatori, gli scienziati del Salk forniscono contributi innovativi alla nostra comprensione di cancro, invecchiamento, Alzheimer, diabete e malattie infettive, studiando neuroscienze, genetica, biologia cellulare e vegetale e discipline correlate.
I risultati conseguiti dal corpo docente sono stati riconosciuti con numerosi riconoscimenti, tra cui premi Nobel e l'iscrizione alla National Academy of Sciences. Fondato nel 1960 dal pioniere del vaccino contro la poliomielite Jonas Salk, l'Istituto è un'organizzazione indipendente senza scopo di lucro e un punto di riferimento architettonico.
JOURNAL
Scienze
AUTORI
Weiqi Zhang, Jingyi Li, Keiichiro Suzuki, Jing Qu, Ping Wang, Junzhi Zhou, Xiaomeng Liu, Ruotong Ren, Xiuling Xu, Alejandro Ocampo, Tingting Yuan, Jiping Yang, Ying Li, Liang Shi, Dee Guan, Huize Pan, Shunlei Duan, Zhichao Ding, Mo Li, Fei Yi, Ruijun Bai, Yayu Wang, Chang Chen, Fuquan Yang, Xiaoyu Li, Zimei Wang, Emi Aizawa, April Goebl, Rupa Devi Soligalla, Pradeep Reddy, Concepcion Rodriguez Esteban, Fuchou Tang, Guang-Hui Liu, Juan Carlos Izpisua Belmonte
Ufficio delle comunicazioni
Tel: (858) 453-4100
press@salk.edu