
30 settembre 2024
Gli scienziati del Salk presentano un metodo per identificare la connettività tra i tipi di cellule cerebrali con una risoluzione senza precedenti
Gli scienziati del Salk presentano un metodo per identificare la connettività tra i tipi di cellule cerebrali con una risoluzione senza precedenti
LA JOLLA—Gli scienziati del Salk Institute stanno svelando una nuova neurotecnologia per la mappatura del cervello chiamata Single Transcriptome Assisted Rabies Tracing (START). Questo strumento all'avanguardia combina due tecnologie avanzate – il tracciamento monosinaptico del virus della rabbia e la trascrittomica a singola cellula – per mappare le intricate connessioni neuronali del cervello con una precisione senza pari.
Utilizzando questa tecnica, i ricercatori sono stati i primi a identificare i modelli di connettività dei sottotipi trascrittomici dei neuroni inibitori nella corteccia cerebrale. Affermano che questa capacità di mappare la connettività dei sottotipi neuronali guiderà lo sviluppo di nuove terapie in grado di colpire determinati neuroni e circuiti con maggiore specificità. Tali trattamenti potrebbero essere più efficaci e produrre meno effetti collaterali rispetto agli attuali approcci farmacologici.
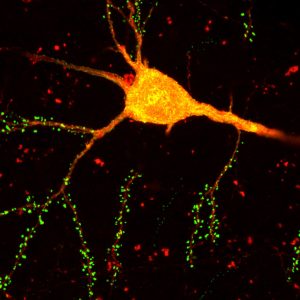
Lo studio, pubblicato il 30 settembre 2024, in Neuron, è il primo a risolvere la connettività corticale alla risoluzione dei tipi di cellule trascrittomiche.
"Quando si tratta di curare disturbi neurologici e neuropsichiatrici, abbiamo essenzialmente cercato di riparare una macchina senza comprenderne appieno le parti", afferma l'autore senior Edward Callaway, professore e titolare della cattedra Vincent J. Coates in Neurobiologia Molecolare al Salk. "START ci sta aiutando a creare un modello dettagliato delle numerose parti del cervello e di come sono tutte collegate."
È come cercare di riparare un'auto senza sapere cosa siano un motore o un asse, dice. Ma se avessi uno schema dei componenti dell'auto, potresti iniziare a capire come interagiscono per far girare le ruote e far muovere l'auto. Questa conoscenza renderebbe quindi molto più facile individuare un problema nel sistema e capire quali strumenti saranno necessari per risolverlo.
Quando si descrivono le parti del cervello, i neuroni vengono inizialmente raggruppati in due grandi classi: eccitatori (quelli che stimolano l'attività cerebrale) e inibitori (quelli che la inibiscono), simili all'acceleratore e al freno di un'auto. Da lì possono essere ulteriormente suddivisi in sottoclassi: i neuroni eccitatori sono classificati in base allo strato del cervello in cui si trovano, mentre i neuroni inibitori sono identificati dalle proteine marcatrici che esprimono.
I recenti progressi nella trascrittomica consentono ora di suddividere ulteriormente queste sottoclassi. Utilizzando il sequenziamento dell'RNA a singola cellula, gli scienziati possono ora raggruppare cellule con modelli di espressione genica simili e definire ciascun cluster come uno specifico sottotipo neuronale.
"Definire un tipo di cellula è complicato perché si potrebbero raggruppare le cellule in modo diverso a seconda del metodo utilizzato per osservarle", afferma Callaway. "Due cellule possono avere modelli di espressione genica leggermente diversi ma svolgere una funzione simile, oppure due cellule con un'espressione genica simile potrebbero essere ulteriormente separate in base alla loro anatomia, connettività o fisiologia. Se si considera solo una di queste caratteristiche, si potrebbe finire per suddividere eccessivamente o sotto-suddividere i gruppi. START ci aiuta a capire quale livello di categorizzazione può essere più significativo per la funzione del circuito, e questo ci indicherà quali cellule prendere di mira con nuove terapie".
Per creare START, il laboratorio Callaway ha ideato un modo per combinare il sequenziamento dell'RNA a singola cellula con un'altra tecnica sviluppata in precedenza: tracciamento del virus monosinaptico della rabbiaL'approccio consente a un virus modificato di passare da un tipo di cellula di interesse alle sole cellule direttamente connesse ad esso. Rilevando dove finisce il virus, i ricercatori possono mappare quali cellule sono connesse a quali.
I ricercatori hanno utilizzato per la prima volta il loro nuovo strumento per esplorare i modelli di connettività nella corteccia visiva del topo. START è stato in grado di identificare circa 50 diversi sottotipi di neuroni inibitori in questa regione e di mappare le loro connessioni con i neuroni eccitatori in ogni strato della corteccia. I risultati dei ricercatori hanno identificato modelli di connettività distinti tra vari sottotipi trascrittomici di neuroni inibitori che non avrebbero potuto essere distinti con metodi precedenti.
"Spesso si trattano tutti i neuroni inibitori come un unico gruppo uniforme, ma in realtà sono molto diversi e cercare di studiarli o di indirizzarli clinicamente come un unico gruppo può oscurare importanti differenze che sono fondamentali per la funzione e la malattia del cervello", afferma la prima autrice Maribel Patiño, ex studentessa laureata nel laboratorio di Callaway e attuale specializzanda in psichiatria presso la facoltà di medicina dell'UC San Diego.
START ha rivelato che ogni strato corticale di neuroni eccitatori riceveva input selettivi da specifici sottotipi trascrittomici di cellule inibitorie Sst, Pvalb, Vip e Lamp5. La connettività unica di ciascun sottotipo contribuisce a stabilire microcircuiti sofisticati che probabilmente contribuiscono a funzioni cerebrali specializzate.
Ad esempio, i ricercatori sono riusciti a isolare un sottotipo inibitorio chiamato cellule Sst Chodl, che si ritiene siano associate alla regolazione del sonno. Utilizzando START, hanno scoperto che le cellule Chodl erano il tipo cellulare più densamente connesso ai neuroni eccitatori dello strato 6, noti per proiettare al talamo per coordinare i ritmi del sonno.

Questa risoluzione senza precedenti consentirà ai neuroscienziati di continuare a scoprire come specifici sottotipi neuronali modellano i circuiti del cervello per produrre i nostri pensieri, le nostre percezioni, le nostre emozioni e i nostri comportamenti.
I prossimi passi dei ricercatori sono la creazione di vettori virali e tecnologie di editing genetico mirate a ogni singolo sottotipo cellulare. In futuro, questi strumenti potrebbero essere adattati a nuove terapie che modificano selettivamente le specifiche popolazioni neuronali che contribuiscono a condizioni come l'autismo, la sindrome di Rett e la schizofrenia.
"Non sappiamo esattamente come verranno utilizzate queste informazioni tra 10 o 20 anni, ma sappiamo che le tecnologie stanno cambiando rapidamente e il modo in cui il cervello viene trattato oggi con i farmaci non è lo stesso che verrà trattato in futuro", afferma Callaway. "START può contribuire a guidare questa innovazione, in modo che i virus e le risorse siano tutti liberamente accessibili all'intera comunità neuroscientifica".
Tra gli altri autori figurano Marley A. Rossa, Willian Nuñez Lagos e Neelakshi S. Patne del Salk Institute.
Il lavoro è stato sostenuto dai National Institutes of Health (R34 NS116885, T32 GM007198, P30 014195, S10 OD023689) e dalla Paul and Daisy Soros Fellowship for New Americans.
DOI: 10.1016 / j.neuron.2024.09.003
JOURNAL
Neuron
AUTORI
Maribel Patiño, Marley A. Rossa, Willian Nuñez Lagos, Neelakshi S. Patn, Edward M. Callaway
Ufficio delle comunicazioni
Tel: (858) 453-4100
press@salk.edu
Il Salk Institute è un istituto di ricerca indipendente e senza scopo di lucro, fondato nel 1960 da Jonas Salk, sviluppatore del primo vaccino antipolio sicuro ed efficace. La missione dell'istituto è quella di promuovere una ricerca fondamentale, collaborativa e rischiosa che affronti le sfide più urgenti della società, tra cui il cancro, il morbo di Alzheimer e la vulnerabilità agricola. Questa scienza fondamentale è alla base di tutti gli sforzi traslazionali, generando intuizioni che consentono nuovi farmaci e innovazioni in tutto il mondo.