
8 janvier 2016
Le facteur déterminant dans la façon dont les tumeurs malignes se propagent peut également être un élément clé du traitement
Le facteur déterminant dans la façon dont les tumeurs malignes se propagent peut également être un élément clé du traitement
LA JOLLA — Le glioblastome multiforme est une maladie particulièrement mortelle cancerUne personne diagnostiquée avec ce type de tumeur cérébrale survit généralement 15 mois, si elle reçoit les meilleurs soins. Le regretté sénateur Ted Kennedy a succombé à cette maladie en un peu plus d'un an.
Mais les scientifiques de l’Institut Salk ont découvert une clé expliquant la rapidité avec laquelle ces cellules tumorales prolifèrent, ainsi que des moyens de transformer ce moteur de croissance tumorale en une cible pour le traitement du cancer.
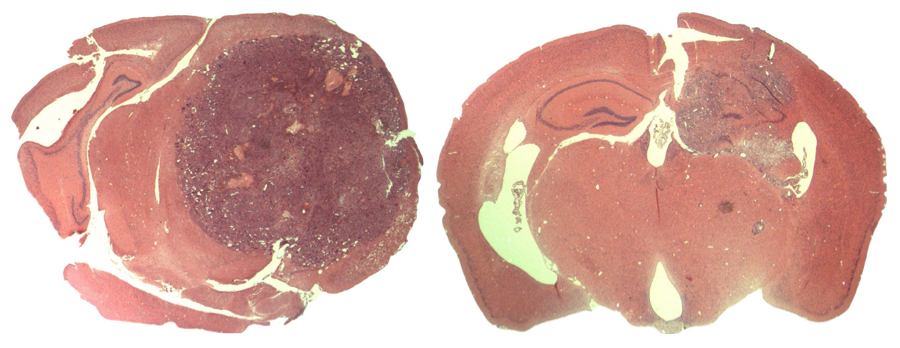
Cliquez ici pour télécharger une image haute résolution.
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
« Il s’agit d’une maladie pour laquelle il n’y a pratiquement pas eu d’amélioration des résultats du traitement depuis des années », a déclaré Inder Verma, professeur au laboratoire de génétique de l'Institut Salk et auteur principal de l'article publié le 8 janvier 2016 dans la revue Science Advances« Il est clair que même si un chirurgien retire 99.99 % d’une tumeur de glioblastome multiforme, ce qui reste reviendra et se transformera en une tumeur plus importante. »
Pour étudier la propagation du glioblastome multiforme, l'équipe de Verma s'est concentrée sur un facteur de transcription appelé facteur nucléaire kB (ou NF-kB). Un facteur de transcription est une protéine qui se lie à l'ADN et contrôle l'expression d'un ensemble particulier de gènes. Plusieurs facteurs connus peuvent déclencher l'activité du NF-kB dans une cellule, notamment les rayonnements ultraviolets et ionisants, les protéines immunitaires (cytokines) et les lésions de l'ADN.
Dans le cas du glioblastome multiforme, Verma et ses collègues ont effectué une batterie de tests pour montrer comment une activité NF-kB trop zélée poussait les cellules cancéreuses à proliférer, et comment l'arrêt de NF-kB ralentissait la croissance du cancer et augmentait la survie chez la souris.
« Nos expériences ont confirmé que NF-kB est nécessaire à la prolifération des cellules cancéreuses », explique Dinorah Friedmann-Morvinski, première auteure de l'article et actuellement chercheuse au département de biochimie et de biologie moléculaire de l'Université de Tel Aviv, en Israël. « Mais nous avons enfin trouvé un moyen d'améliorer l'état de la tumeur et d'augmenter sa durée de vie. »
L'équipe de Verma a commencé avec un modèle murin de glioblastome multiforme et a utilisé des outils génétiques pour manipuler les cellules et inhiber l'activité de NF-kB de deux manières. L'équipe a augmenté la présence d'une protéine appelée IkBaM, qui inhibe l'activité de NF-kB. Elle a également éliminé une enzyme qui augmente l'activité de NF-kB. Avec une activité NF-kB réduite, la croissance tumorale a ralenti et les souris ont vécu significativement plus longtemps que celles dont l'activité NF-kB était restée inchangée. Cependant, si ces expériences génétiques ont démontré le rôle de NF-kB dans le glioblastome multiforme, elles ne constituent pas un traitement envisageable chez l'homme.
« Nous avons donc demandé comment nous pouvions manipuler le système en utilisant la pharmacologie plutôt que la génétique », explique Verma.
Les scientifiques soupçonnent depuis longtemps que l'une des raisons de la récidive si rapide du glioblastome multiforme après une intervention chirurgicale est le microenvironnement tumoral. Autrement dit, une tumeur modifie son environnement (tissus adjacents) pour faciliter la prolifération des cellules cancéreuses, explique Verma.

Cliquez ici pour télécharger une image haute résolution.
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
Au lieu d'utiliser des outils génétiques, Verma et ses collègues ont cherché à traiter les tumeurs cérébrales en modifiant également le microenvironnement tumoral. Les scientifiques ont administré à des souris un peptide (appelé NBD) connu pour bloquer l'activité de NF-kB lorsque celui-ci est activé par des cytokines (protéines produites par le système immunitaire). Le peptide NBD traverse facilement le système nerveux central et peut pénétrer avec succès les cellules tumorales du glioblastome. Le traitement des souris avec le peptide NBD a doublé leur durée de survie moyenne par rapport aux souris n'ayant pas reçu ce peptide.
« Nous pourrions augmenter la durée de survie d'un mois sans traitement à trois mois avec traitement », explique Verma. « C'est une augmentation considérable de l'espérance de vie, surtout si l'on considère qu'une souris ne vit que deux ans. » Pourtant, si le peptide NBD a permis de contenir les tumeurs, le traitement peptidique finit par provoquer une toxicité, probablement hépatique. Les chercheurs ont donc exploré une autre stratégie pour ralentir l'activité de NF-kB.
Limiter l’activité du NF-kB peut être délicat car le NF-kB joue de nombreux rôles importants : il aide à réguler la survie cellulaire, l’inflammation et l’immunité parmi de nombreuses autres fonctions de la cellule.
« L'objectif ultime est de bloquer NF-kB, mais comme il active de nombreux gènes – au moins 100 –, notre objectif est désormais d'identifier les quelques gènes qui affectent directement la croissance tumorale », explique Verma. « Nous pourrons ainsi être plus sélectifs dans le traitement. »
Les scientifiques de Salk ont identifié les gènes influencés par NF-kB et en ont identifié un, Timp1, déjà impliqué dans le cancer du poumon. Le ciblage du gène Timp1 dans le traitement a également ralenti la croissance tumorale et augmenté la survie des souris de quelques mois.
« À l'avenir, nous souhaitons nous concentrer sur les moyens de réduire la toxicité des médicaments anti-NF-kB », a déclaré Friedmann-Morvinski. « Nous pourrions y parvenir en ciblant spécifiquement ces médicaments sur la tumeur, ou en identifiant des cibles en aval de la voie NF-kB, comme Timp1, qui prolongent également la survie. » D'autres expériences pourraient permettre d'identifier des traitements ciblant l'activité NF-kB de manière sûre et efficace.
Parmi les autres auteurs de l'article figuraient Rajesh Narasimamurthy, Yifeng Xia, Chad Myskiw et Yasushi Soda du Salk Institute for Biological Studies.
Les travaux ont été financés par le National Institutes of Health, le Fondation HN et Frances C. Bergerainsi que, Leona M. et Harry B. Helmsley Charitable Trust.
BLOG
Science Advances
AUTEURS
Dinorah Friedmann-Morvinski, Rajesh Narasimamurthy, Yifeng Xia, Chad Myskiw, Yasushi Soda, Inder M. Verma
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.