
17 février 2016
L'Institut Salk et ses collaborateurs montrent des différences moléculaires clés entre les virus lorsqu'ils interagissent avec l'ADN de l'hôte
L'Institut Salk et ses collaborateurs montrent des différences moléculaires clés entre les virus lorsqu'ils interagissent avec l'ADN de l'hôte
LA JOLLA — Grâce à une technologie d'imagerie de pointe, le Salk Institute et Harvard Medical School des chercheurs ont déterminé la structure d'un complexe protéique qui permet à des virus similaires au virus de l'immunodéficience humaine (VIH) établissent des infections permanentes chez leurs hôtes.
Contrairement aux hypothèses précédentes, la structure détaillée du complexe protéique viral indique que ce type d'architecture moléculaire diffère selon les rétrovirus. Ces informations contribuent à révéler comment les rétrovirus insèrent leur information génomique dans les cellules humaines et pourraient avoir des implications non seulement pour le traitement de maladies comme le VIH, mais aussi pour l'amélioration des méthodes de thérapie génique afin d'administrer du nouvel ADN aux patients présentant des mutations génétiques.
« Les détails de la façon dont les rétrovirus s'intègrent diffèrent beaucoup plus qu'on ne le pensait auparavant et conduisent à des schémas d'infection entièrement distincts », explique Dmitry Lyumkis, un chercheur en biologie moléculaire. Compagnon de Salk et co-auteur principal du nouvel article, publié dans Nature sur Février 18, 2016.
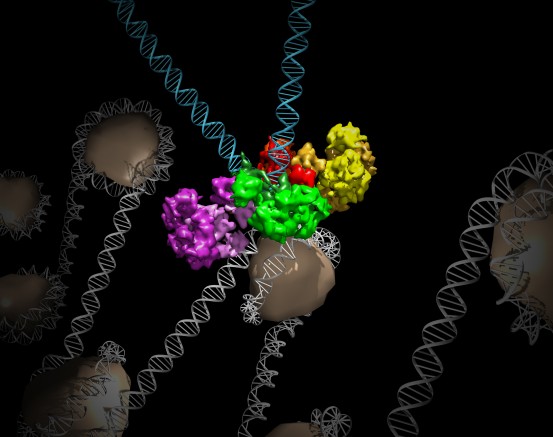
Cliquez ici pour une image haute résolution.
Crédit : Salk Institute
Un rétrovirus insère son information génétique dans le génome de son hôte, transformant ainsi ses cellules en véritables usines à virus. Dans le cas du célèbre rétrovirus VIH, ces gènes viraux s'intègrent aux cellules immunitaires humaines, les détruisant finalement. Un mystère persistant, dû en partie à la méconnaissance de la structure complexe des protéines, concerne l'emplacement de l'insertion de l'ADN viral dans le génome humain.
Un complexe protéique appelé intasome est responsable de l'insertion irréversible de l'ADN viral dans l'ADN humain, une étape essentielle pour permettre aux rétrovirus de provoquer des maladies. L'intasome du VIH étant lui-même difficile à étudier, la plupart des connaissances actuelles sur les intasomes reposent sur les travaux d'un autre rétrovirus, le prototype de virus spumeux, ou PFV. Face aux difficultés liées aux échantillons d'intasomes du VIH, Lyumkis et Engelman, en collaboration avec leur collègue Peter Cherepanov du Francis Crick Institute, ont entrepris de déterminer la structure de l'intasome du virus des tumeurs mammaires de la souris (MMTV), qui, à certains égards, est plus proche du VIH que du PFV.
« La structure de l'intasome MMTV définit un nouveau paradigme inattendu pour la base structurelle de l'intégration de l'ADN rétroviral », déclare le co-auteur principal Alan Engelman, professeur de médecine au Dana-Farber Cancer Institute et à la Harvard Medical School.
Pour déterminer la structure moléculaire du MMTV, l'équipe a utilisé une technique prometteuse appelée cryomicroscopie électronique (cryoEM), une approche qui présente plusieurs avantages par rapport aux techniques d'imagerie traditionnelles. Par exemple, les chercheurs n'ont pas besoin de cristalliser les protéines pour les imager, un processus aléatoire qui est pourtant nécessaire pour la technique plus courante de cristallographie aux rayons X. En cryoEM, les protéines sont directement congelées dans une solution liquide. Ensuite, en mesurant la déviation des faisceaux d'électrons par les échantillons congelés, les scientifiques peuvent déterminer la structure des protéines.
Lyumkis a utilisé cette technologie de pointe pour détailler la structure des intasomes du MMTV liés à des brins d'ADN viral (ce à quoi ressemblerait la structure une fois qu'elle aurait envahi une cellule hôte). L'équipe a découvert que, si le complexe PFV est composé de quatre composants protéiques, appelés intégrases, liés à deux brins d'ADN viral, l'assemblage du MMTV comporte huit molécules d'intégrase pour deux fragments d'ADN viral.
Selon Lyumkis, cette différence structurelle essentielle signifie que les complexes interagissent différemment avec l'ADN de l'hôte lorsqu'ils sont prêts à insérer l'ADN viral dans le génome. Le PFV privilégie les zones fortement courbées du génome de l'hôte, tandis que le MMTV privilégie les segments d'ADN droits. La préférence pour le VIH reste un mystère, mais les nouvelles observations fournissent un cadre moléculaire inattendu pour interpréter les données passées et futures sur le VIH et d'autres rétrovirus.
Les équipes de Lyumkis et Engelman s'efforcent désormais de comprendre la série d'événements que traverse le complexe intasome du MMTV au cours des étapes de l'intégration virale, de la liaison à l'ADN viral à la capture de l'ADN de l'hôte et à la catalyse de son insertion dans le génome de ce dernier. Lyumkis prévoit également d'appliquer les techniques de cryoEM à l'étude du complexe moléculaire de l'intasome du VIH lui-même. « L'infrastructure technologique est en place, et je pense que nous pouvons désormais nous attaquer à ces échantillons complexes et peu performants grâce à la cryoEM », ajoute Lyumkis.
Les autres chercheurs ayant participé à l'étude étaient Allison Ballandras-Colas et Tamaria G. Dewdney de l' Institut du cancer Dana-Farber et de la faculté de médecine de Harvard ; Monica Brown du Salk Institute ; Nicola J. Cook et Peter Cherepanov du Institut Francis Crick; et Borries Demeler du Centre des sciences de la santé de l'Université du Texas.
Les travaux et les chercheurs impliqués ont été soutenus par des subventions du National Institutes of Health, le Leona M. et Harry B. Helmsley Charitable Trust, le National Science Foundation et l'Institut du cancer de San Antonio.
BLOG
Nature
AUTEURS
Allison Ballandras-Colas, Tamaria G. Dewdney et Alan Engelman de la Harvard Medical School ; Monica Brown et Dmitry Lyumkis du Salk Institute ; Nicola J. Cook et Peter Cherepanov du Francis Crick Institute ; et Borries Demeler du University of Texas Health Sciences Center.
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.