
10 décembre 2009
LA JOLLA, CA — Le vieillissement est le principal facteur de risque de la maladie d'Alzheimer. Dans leur dernière étude, des chercheurs du Salk Institute for Biological Studies ont découvert que le simple fait de ralentir le processus de vieillissement chez des souris prédisposées à la maladie d'Alzheimer empêchait leur cerveau de se transformer en un désert neuronal.
« Notre étude ouvre une toute nouvelle voie pour étudier la maladie », déclare le responsable de l'étude, Howard Hughes Medical Investigator. Andrew Dilin, Ph.D., professeur associé au Laboratoire de biologie moléculaire et cellulaire de Salk. « À l'avenir, l'étude de la façon dont nous vieillissons pourrait avoir plus d'impact sur le traitement et la prévention de la maladie d'Alzheimer que l'étude de la biologie fondamentale de la maladie elle-même. »
Leurs conclusions, publiées dans le numéro du 11 décembre 2009 de la revue Cellule, est le dernier indice dans la quête continue des scientifiques de Salk pour faire la lumière sur la question de savoir si l'apparition de la maladie d'Alzheimer à un âge avancé est une conséquence désastreuse du processus de vieillissement lui-même ou si les agrégats bêta-amyloïdes qui causent la maladie prennent simplement beaucoup de temps à se former.
Heure: 00: 02: 32
Vidéo : avec l'aimable autorisation du Salk Institute for Biological Studies
L'âge est le principal facteur de risque de développement de la maladie d'Alzheimer. Au-delà de 65 ans, le nombre de personnes atteintes double tous les cinq ans. Les centenaires, en revanche, semblent échapper à la plupart des maladies courantes liées à l'âge, y compris les ravages de la maladie d'Alzheimer.
« Dans cette étude, nous sommes allés directement à la cause profonde de la maladie d'Alzheimer et nous nous sommes demandé si nous pouvions influencer l'apparition de la maladie en modulant le processus de vieillissement », explique le premier auteur Ehud Cohen, Ph.D., ancien chercheur postdoctoral dans le laboratoire de Dillin et maintenant professeur adjoint à la faculté de médecine de l'Université hébraïque-Hadassah à Jérusalem, en Israël.
Pour répondre à cette question fascinante, il a ralenti le processus de vieillissement chez un modèle murin de la maladie d'Alzheimer en diminuant l'activité de la voie de signalisation IGF-1. « Cette voie hautement conservée joue un rôle crucial dans la régulation de la longévité et de la jeunesse chez de nombreuses espèces, notamment les vers, les mouches et les souris, et est liée à une longévité extrême chez l'homme », explique-t-il. Ainsi, les souris dont la signalisation IGF-1 est réduite vivent jusqu'à 35 % plus longtemps que les souris normales.
Cohen a ensuite utilisé une batterie de tests comportementaux pour déterminer si c'était simplement le passage du temps ou le vieillissement en soi qui déterminait l'apparition de la maladie. Des animaux chronologiquement âgés, mais biologiquement jeunes, semblaient presque normaux bien après que des souris atteintes de la maladie d'Alzheimer du même âge et normalement âgées aient présenté de graves déficiences dans leur capacité à trouver une plateforme immergée dans le labyrinthe aquatique de Morris ((voir les vidéos d'accompagnement) ou restez au sommet d'une Rota Rod rotative.
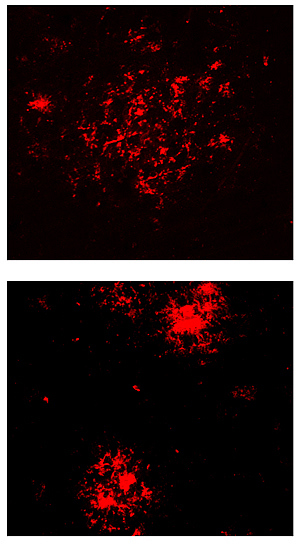
En haut : Plaques bêta-amyloïdes chez des souris atteintes de la maladie d’Alzheimer vieillissant normalement. En bas : Des plaques plus compactes chez des souris atteintes de la maladie d’Alzheimer à longue durée de vie protègent contre la maladie.
Image : avec l'aimable autorisation du Dr Ehud Cohen, Faculté de médecine de l'Université hébraïque-Hadassah
« Ces différences comportementales entre les souris normales et celles à longue durée de vie étaient apparentes à l’âge de neuf mois, mais la grande surprise est survenue lorsque nous avons examiné de plus près les plaques dans leur cerveau », explique Cohen.
L'un des signes révélateurs de la maladie d'Alzheimer est l'accumulation d'amas toxiques de plaques bêta-amyloïdes dans le cerveau. La production de bêta-amyloïdes est probablement présente dans tous les cerveaux, mais les cellules saines éliminent les quantités excédentaires. Le cerveau des personnes atteintes de la maladie d'Alzheimer, en revanche, est incapable de contrôler l'accumulation de bêta-amyloïdes. Il en va de même pour les modèles murins atteints de la maladie d'Alzheimer, génétiquement modifiés pour surproduire de la bêta-amyloïde.
Bien que les souris à longue durée de vie n'aient montré aucun des troubles cognitifs ou comportementaux typiques de la maladie d'Alzheimer jusqu'à très tard dans leur vie, leur cerveau était criblé de plaques très compactées.
« Bien qu'on ait longtemps pensé que les plaques étaient les agents responsables de la maladie d'Alzheimer, nos résultats confirment clairement l'idée émergente selon laquelle elles auraient une fonction protectrice », explique Cohen. « Avec l'âge, les souris perdent en efficacité pour stocker les fibrilles bêta-amyloïdes toxiques en agrégats compacts. »
Une étude antérieure de Cohen, Dillin et leurs collègues, dans laquelle ils avaient utilisé des ascaris pour étudier les effets du vieillissement sur l'agrégation des protéines, avait indiqué que les agrégats de bêta-amyloïde de haut poids moléculaire pourraient être moins toxiques que les fibrilles bêta-amyloïdes plus petites. « Mais les vers n'ont pas de cerveau comme nous, et il n'était pas certain que ces résultats soient pertinents pour les mammifères », explique-t-il.
Et qu'en est-il de ces centenaires lucides ? « Il est intéressant de noter que trois études ont révélé que certains humains à très longue durée de vie sont porteurs de mutations dans des composants de la voie de signalisation de l'IGF-1, la même voie que nous avons perturbée pour augmenter la durée de vie des souris dans notre étude », explique Dillin.
« La publication de ces travaux est une célébration pour l'ensemble des chercheurs sur le vieillissement, car elle valide l'hypothèse de longue date selon laquelle les changements génétiques et pharmacologiques visant à créer une durée de vie saine, ou « durée de vie en bonne santé », peuvent réduire considérablement l'apparition de certaines des maladies les plus dévastatrices qui affligent l'humanité », ajoute-t-il.
Les travaux ont été financés en partie par les National Institutes of Health et le McKnight Endowment for Neuroscience.
Les chercheurs qui ont également contribué à ce travail sont Johan F. Paulsson, Deguo Du et Jeffery W. Kelly du Skaggs Institute of Chemical Biology, du Scripps Research Institute, Pablo Blinder du Département de physique de l'Université de Californie à San Diego, Tal Burstyn-Cohen du Laboratoire de neurobiologie moléculaire du Salk Institute, Anthony Adame, Hang M. Pham et Eliezer Masliah du Département de neurosciences de l'Université de Californie à San Diego, et Gabriela Estepa du Laboratoire de biologie moléculaire et cellulaire du Salk Institute.
À propos du Salk Institute for Biological Studies :
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies cardiovasculaires en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale, ainsi que les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu