
22 mars
Une altération de la croissance des neurones et de l’expression des gènes pourrait être liée à la raison pour laquelle certaines personnes déprimées ne répondent pas aux ISRS
Une altération de la croissance des neurones et de l’expression des gènes pourrait être liée à la raison pour laquelle certaines personnes déprimées ne répondent pas aux ISRS
LA JOLLA — Les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) sont les médicaments les plus couramment prescrits pour le trouble dépressif majeur (TDM). Pourtant, les scientifiques ne comprennent toujours pas pourquoi ce traitement est inefficace chez près de 30 % des patients atteints de TDM. Des chercheurs du Salk Institute ont découvert des différences dans la croissance neuronale des patients résistants aux ISRS. Ces travaux, publiés dans Molecular Psychiatry le 22 mars 2019, a des implications sur la dépression ainsi que sur d’autres troubles psychiatriques tels que le trouble bipolaire et la schizophrénie qui impliquent probablement également des anomalies du système sérotoninergique dans le cerveau.
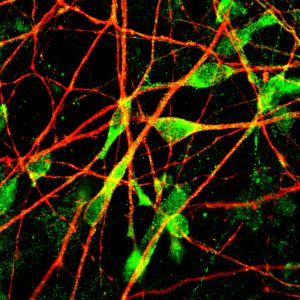
Cliquez ici pour une image haute résolution.
Crédit : Salk Institute
« Avec chaque nouvelle étude, nous nous rapprochons d'une compréhension plus complète des circuits neuronaux complexes sous-jacents aux maladies neuropsychiatriques, y compris la dépression majeure », déclare le professeur Salk. Jauge rouillée, auteur principal de l'étude, président de l'Institut et titulaire de la chaire Vi et John Adler de recherche sur les maladies neurodégénératives liées à l'âge. « Cet article, ainsi qu'un autre que nous avons récemment publié, non seulement apporte un éclairage sur ce traitement courant, mais suggère également que d'autres médicaments, comme les antagonistes sérotoninergiques, pourraient constituer des options supplémentaires pour certains patients. »
La cause de la dépression est encore inconnue, mais les scientifiques pensent que la maladie est en partie liée au circuit sérotoninergique cérébral. Cela s'explique en grande partie par le fait que les ISRS, qui augmentent les niveaux de sérotonine, un neurotransmetteur, au niveau des connexions neuronales, contribuent à soulager les symptômes de nombreuses personnes atteintes de dépression. Pourtant, le mécanisme expliquant pourquoi certaines personnes réagissent aux ISRS, tandis que d'autres n'y réagissent pas, reste un mystère. Élucider l'énigme de la résistance aux ISRS s'est avéré complexe, car cela nécessite l'étude des 300,000 100 neurones qui utilisent la sérotonine pour communiquer dans un cerveau qui en compte XNUMX milliards. L'une des solutions récemment trouvées par les scientifiques pour surmonter cet obstacle est de générer ces neurones sérotoninergiques en laboratoire.
Les équipes article précédent dans Molecular Psychiatry Il a été démontré que les patients non répondeurs aux ISRS présentaient une augmentation des récepteurs à la sérotonine, ce qui rendait les neurones hyperactifs en réponse à la sérotonine. L'article actuel visait à examiner les patients non répondeurs aux ISRS sous un angle différent.
« Nous voulions savoir si la biochimie, l'expression génétique et les circuits de la sérotonine étaient altérés chez les patients non répondeurs aux ISRS par rapport aux patients répondeurs utilisant des neurones sérotoninergiques dérivés de patients atteints de TDM », explique Krishna Vadodaria, chercheur à Salk et premier auteur de la nouvelle étude. « L'utilisation de neurones dérivés de patients atteints de TDM offre une nouvelle représentation de la comparaison entre les patients répondeurs et non répondeurs aux ISRS. »

Cliquez ici pour une image haute résolution.
Crédit : Salk Institute
À partir d'une étude clinique à grande échelle menée auprès de 800 patients atteints de trouble dépressif majeur (TDM), les chercheurs ont sélectionné les cas les plus extrêmes de réponse aux ISRS : des patients dont l'état s'est considérablement amélioré grâce aux ISRS et des patients n'ayant constaté aucun effet. L'équipe a prélevé des échantillons de peau de ces patients et a reprogrammé les cellules en cellules souches pluripotentes induites (CSPi) afin de créer des neurones sérotoninergiques à étudier.
Les scientifiques ont examiné les cibles de la sérotonine dans les neurones sérotoninergiques des patients, notamment l'enzyme qui la produit, la protéine qui la transporte et l'enzyme qui la dégrade. Ils n'ont constaté aucune différence dans les interactions biochimiques entre les groupes. Au contraire, les chercheurs ont observé une différence dans la façon dont les neurones réagissaient en fonction de leur forme.
Les neurones des patients non répondeurs aux ISRS présentaient des projections neuronales plus longues que celles des patients répondeurs. L'analyse génétique a révélé que ces patients présentaient également de faibles concentrations de gènes clés (protocadhérines PCDHA6 et PCDHA8) impliqués dans la formation des circuits neuronaux. Lorsque ces gènes étaient rendus non fonctionnels dans les neurones sérotoninergiques (imitant les faibles concentrations génétiques observées précédemment), les neurones développaient les mêmes projections anormalement longues chez les patients non répondeurs aux ISRS. Ces anomalies pourraient entraîner une communication neuronale excessive dans certaines zones du cerveau et insuffisante dans d'autres, altérant la communication au sein des circuits sérotoninergiques et expliquant pourquoi les ISRS ne sont pas toujours efficaces dans le traitement du trouble dépressif majeur.
« Ces résultats contribuent à une nouvelle façon d’examiner, de comprendre et de traiter la dépression », explique Gage.
L’étape suivante consiste à examiner les gènes de la protocadhérine pour mieux comprendre la génétique des non-répondeurs aux ISRS.
Parmi les autres auteurs figuraient : Apua Paquola, Kelly J. Heard, Callie Fredlender, Yalin Deng, James Elkins, Komal Dani, Amy T. Le et Maria C. Marchetto de Salk ; Yuan Ji de l'Université de l'Utah ; et Michelle Skime, Timothy Nelson, Daniel Hall-Flavin et Richard Weinshilboum de la Mayo Clinic
Ce travail a été financé par la Fondation Robert et Mary Jane Engman, Lynn et Edward Streim, un programme de subventions de l'Alliance pour l'innovation du consortium Takeda-Sanford (Takeda Pharmaceutical Company), le Fonds national suisse de la recherche scientifique (FNS), le Minnesota Partnership Award for Biotechnology and Medical Genomics, le Mayo Clinic Center for Regenerative Medicine, le NIH-Mayo Clinic KL2 Mentored Career Development Award (NCAT UL1TR000135), le Gerstner Family Mayo Career Development Award in Individualized Medicine et les National Institutes of Health (GM61388 PGRN et RO1 GM28157).
DOI: 10.1038/s41380-019-0377-5
BLOG
Molecular Psychiatry
AUTEURS
Krishna C. Vadodaria, Yuan Ji, Michelle Skime, Apua Paquola, Timothy Nelson, Daniel Hall-Flavin, Kelly J. Heard, Callie Fredlender, Yalin Deng, James Elkins, Komal Dani, Amy T. Le, Maria C. Marchetto, Richard Weinshilboum et Fred H. Gage
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.