
le 18 juillet, 2013
Une nouvelle méthode devrait accélérer la promesse de la médecine régénérative
Une nouvelle méthode devrait accélérer la promesse de la médecine régénérative
LA JOLLA, CA — Les cellules souches sont essentielles à la promesse de la médecine régénérative : la réparation ou le remplacement des tissus endommagés par des substituts cultivés sur mesure. Les cellules souches pluripotentes induites (CSPi), qui peuvent être créées à partir des propres tissus du patient, sont essentielles à ce processus, éliminant ainsi le risque de rejet immunitaire. Cependant, la formule de Shinya Yamanaka pour les CSPi, qui lui a valu le prix Nobel l'année dernière, utilise une recette stricte qui autorise des variations limitées dans les cellules humaines, limitant ainsi leur plein potentiel d'application clinique.
Maintenant, dans le numéro de cette semaine de Cellule souche cellulaire, l'Institut Salk Juan Carlos Izpisua Belmonte et ses collègues démontrent que la recette des cellules souches embryonnaires pluripotentes induites (iPSC) est bien plus polyvalente qu'on ne le pensait initialement. Pour la première fois, ils ont remplacé un gène jusque-là considéré comme impossible à remplacer, ouvrant la voie à des recettes plus flexibles qui devraient accélérer l'adoption des thérapies par cellules souches.

De gauche à droite : Emmanuel Nivet et Juan Carlos Belmonte. Assis : Ignacio Sancho Martínez
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
Il existe deux types de cellules souches : les cellules souches embryonnaires (CSE), immatures et jamais différenciées en types cellulaires spécifiques, et les cellules souches pluripotentes induites, matures et reprogrammées à un état indifférencié. Après la découverte initiale de Yamanaka en 2006 selon laquelle l'introduction de quatre gènes différents dans une cellule mature pouvait suffire à la reprogrammer en pluripotence, la plupart des chercheurs ont adopté sa méthode.
Izpisua Belmonte et ses collègues ont adopté une approche novatrice et ont découvert que la pluripotence (la capacité des cellules souches à se différencier en presque n'importe quel type de cellule adulte) peut également être obtenue en équilibrant les gènes nécessaires à la différenciation. Ces gènes codent des « facteurs de transcription de lignée », des protéines qui initient une cellule souche à se différencier d'abord en une lignée cellulaire particulière, ou type, comme une cellule sanguine ou une cellule cutanée, puis en une cellule spécifique, comme un globule blanc.
« Avant cette série d'expériences, la plupart des chercheurs partaient du principe qu'ils cherchaient à imposer un état de type embryonnaire aux cellules matures », explique Izpisua Belmonte, titulaire de la chaire Roger-Guillemin de l'Institut. « Par conséquent, les efforts se sont principalement concentrés sur l'identification de facteurs caractéristiques des cellules souches embryonnaires naturelles, susceptibles de permettre ou d'améliorer la reprogrammation. »
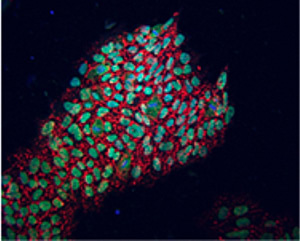
Pour la première fois, le laboratoire Belmonte a remplacé OCT4, un gène jusqu'alors considéré comme indispensable à la reprogrammation des cellules humaines en cellules de type embryonnaire.
L'image montre des cellules nouvellement reprogrammées exprimant des marques de pluripotence identifiées par fluorescence (NANOG en vert, TRA-1-81 en rouge).
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
Malgré ces efforts, il semblait impossible de déterminer, par la seule identité génétique, la pluripotence des cellules. Celle-ci était alors systématiquement évaluée par des tests fonctionnels. Autrement dit, si une cellule se comporte comme une cellule souche, il s'agit forcément d'une cellule souche.
Cette condition a conduit l'équipe à sa découverte clé. « La pluripotence ne semble pas représenter une entité cellulaire distincte, mais plutôt un état fonctionnel provoqué par un équilibre entre des forces de différenciation opposées », explique Izpisua Belmonte.
Une fois ce constat établi, ils ont compris que les quatre gènes supplémentaires n'étaient pas nécessaires à la pluripotence. Celle-ci pouvait être obtenue en modifiant l'équilibre des « spécificateurs de lignée », des gènes déjà présents dans la cellule et spécifiant le type de tissu adulte qu'elle pourrait devenir.
« L’une des implications de nos résultats est que l’identité des cellules souches n’est en réalité pas fixe, mais plutôt un équilibre qui peut être atteint par de multiples combinaisons différentes de facteurs qui ne sont pas nécessairement typiques des cellules souches embryonnaires », explique Ignacio Sancho-Martinez, l’un des premiers auteurs de l’article et chercheur postdoctoral en Le laboratoire d'Izpisua Belmonte.
L'équipe a pu démontrer que plus de sept gènes supplémentaires peuvent faciliter la reprogrammation des cellules iPSC. Plus important encore, pour la première fois dans des cellules humaines, ils ont pu remplacer un gène de la formule originale, appelé Oct4, qui avait été remplacé dans des cellules de souris, mais qui était toujours considéré comme indispensable à la reprogrammation des cellules humaines. Leur capacité à le remplacer, ainsi que SOX2, un autre gène autrefois considéré comme essentiel mais jamais remplacé en association avec Oct4, a démontré que le développement des cellules souches doit être envisagé sous un angle entièrement nouveau.
« On supposait généralement que le développement conduisait à la spécification des cellules/tissus en « ouvrant » certaines portes de différenciation », explique Emmanuel Nivet, chercheur postdoctoral au laboratoire d'Izpisua Belmonte et co-premier auteur de l'article, avec Sancho-Martinez et Nuria Montserrat de l'Université de Californie à Los Angeles. Centre de médecine régénérative de Barcelone, Espagne.
Au contraire, la substitution réussie d'Oct4 et de SOX2 démontre le contraire. « La pluripotence est comparable à une pièce dont toutes les portes sont ouvertes, où la différenciation s'opère en fermant les portes », explique Nivet. « À l'inverse, la reprogrammation vers la pluripotence s'opère en ouvrant les portes. »
L'équipe estime que ses travaux devraient contribuer à surmonter l'un des principaux obstacles à l'adoption généralisée des thérapies par cellules souches : les quatre gènes initialement utilisés pour reprogrammer les cellules souches étaient impliqués dans le cancer. « Des études récentes sur le cancer, dont beaucoup ont été réalisées par mes collègues de Salk, ont montré des similitudes moléculaires entre la prolifération des cellules souches et celle des cellules cancéreuses. Il n'est donc pas surprenant que des oncogènes [gènes liés au cancer] fassent partie de la recette des cellules souches iPS », explique Izpisua Belmonte.
Grâce à cette nouvelle méthode, qui permet une recette personnalisée, l'équipe espère faire progresser la recherche thérapeutique. « Puisque nous avons démontré qu'il est possible de remplacer des gènes considérés comme essentiels à la reprogrammation par plusieurs gènes différents, jusqu'alors non impliqués dans la tumorigenèse, nous espérons que cette étude permettra une transposition clinique plus rapide de la recherche sur les cellules iPS », déclare Izpisua Belmonte.
Les autres chercheurs participant à l'étude étaient Tomoaki Hishida, Sachin Kumar, Yuriko Hishida, Yun Xia et Concepcion Rodriguez Esteban de l'Institut Salk ; Laia Miquel et Carme Cortina du Centre de médecine régénérative de Barcelone, Espagne.
Le travail a été soutenu par le Leona M. et Harry B. Helmsley Charitable Trust, Fondation FM Kirby, le Fondation caritative G. Harold et Leila Y. Mathers, Fondation Nomis, Fundación Cellex, la Ministère de l'Économie et de la Compétitivité (MINECO), TERCEL-ISCIII-MINECO et Cardiocel.
À propos du Salk Institute for Biological Studies :
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies infectieuses en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale, et les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
BLOG
Cellule souche cellulaire
TITRE
Reprogrammation des fibroblastes humains vers la pluripotence avec des spécificateurs de lignée
AUTEURS
Emmanuel Nivet, Ignacio Sancho-Martinez, Tomoaki Hishida, Sachin Kumar, Yuriko Hishida, Yun Xia, Concepcion Rodriguez Esteban et Juan Carlos Izpisua Belmonte de l'Institut Salk ; Nuria Montserrat, Laia Miquel et Carme Cortina du Centre de médecine régénérative de Barcelone, Espagne
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu