
8 janvier 2025
Les scientifiques de Salk ont découvert que les cellules végétales entrent dans un état immunitaire rare pour combattre les agents pathogènes et déclencher des alarmes de menace dans toute la plante.
Les scientifiques de Salk ont découvert que les cellules végétales entrent dans un état immunitaire rare pour combattre les agents pathogènes et déclencher des alarmes de menace dans toute la plante.
LA JOLLA — Le corps humain se défend grâce à une population diversifiée de cellules immunitaires qui circulent d'un organe à l'autre, réagissant à toutes sortes de problèmes, des coupures aux rhumes en passant par le cancer. Mais les plantes n'ont pas ce luxe. L'immobilité des cellules végétales oblige chacune d'elles à gérer sa propre immunité, en plus de ses nombreuses autres responsabilités, comme transformer la lumière du soleil en énergie ou utiliser cette énergie pour croître. La manière dont ces cellules multitâches accomplissent tout cela – détecter les menaces, les communiquer et y répondre efficacement – reste obscure.
De nouvelles recherches menées par des scientifiques du Salk Institute révèlent comment les cellules végétales changent de rôle pour se protéger contre les agents pathogènes. Face à une menace, les cellules entrent dans un état immunitaire spécialisé et deviennent temporairement des cellules PRIMER (Primary IMmunE Responder), une nouvelle population cellulaire qui sert de plaque tournante pour déclencher la réponse immunitaire. Les chercheurs ont également découvert que les cellules PRIMER sont entourées d'une autre population de cellules appelées cellules témoins, qui semblent jouer un rôle important dans la transmission de la réponse immunitaire à l'ensemble de la plante.
Les résultats, publiés dans Nature le 8 janvier 2025, rapprocheront les chercheurs de la compréhension du système immunitaire des plantes, une tâche de plus en plus importante dans un contexte de menaces croissantes de résistance aux antimicrobiens et de changement climatique, qui aggravent tous deux la propagation des maladies infectieuses.
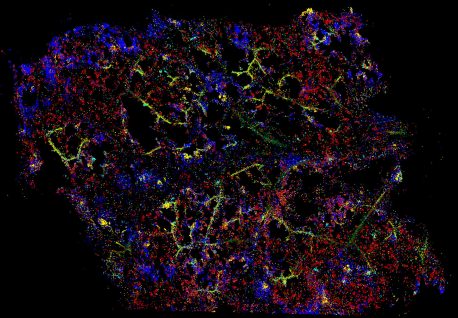
« Dans la nature, les plantes sont constamment sont attaqués et nécessitent un système immunitaire qui fonctionne bien », explique le professeur Joseph Ecker, auteur principal de l'étude, titulaire de la chaire Salk International Council en génétique et chercheur à l'Institut médical Howard Hughes. « Mais les plantes ne possèdent pas de cellules immunitaires mobiles et spécialisées comme les nôtres ; elles doivent inventer un système entièrement différent où chaque cellule peut répondre aux attaques immunitaires sans sacrifier ses autres fonctions. Jusqu'à présent, nous ne savions pas exactement comment les plantes y parvenaient. »
Les plantes sont confrontées à une grande variété d'agents pathogènes, comme les bactéries qui s'infiltrent par les pores de la surface des feuilles ou les champignons qui envahissent directement les cellules de la peau. Les cellules végétales étant stationnaires, lorsqu'elles rencontrent l'un de ces agents pathogènes, elles deviennent les seules responsables de la réaction et de l'alerte des cellules voisines. Un autre effet secondaire intéressant de l'immobilité des cellules est que différents agents pathogènes peuvent pénétrer dans une plante à différents endroits et à différents moments, ce qui entraîne différents stades de réponse immunitaire simultanés dans la plante.
Compte tenu de facteurs tels que le moment, la localisation, l'état de réponse et bien d'autres, une plante infectée est un organisme complexe à comprendre. Pour y parvenir, l'équipe Salk a eu recours à deux techniques sophistiquées de profilage cellulaire : la multiomique unicellulaire à résolution temporelle et la transcriptomique spatiale. En associant ces deux techniques, l'équipe a pu capturer la réponse immunitaire de la plante dans chaque cellule avec une résolution spatio-temporelle sans précédent.
« La découverte de ces cellules PRIMER rares et de leurs cellules témoins environnantes offre un aperçu considérable de la manière dont les cellules végétales communiquent pour survivre aux nombreuses menaces externes auxquelles elles sont confrontées au quotidien », explique le premier auteur Tatsuya Nobori, ancien chercheur postdoctoral dans le laboratoire d'Ecker et actuel chef de groupe au Sainsbury Laboratory au Royaume-Uni.

L'équipe a introduit des agents pathogènes bactériens dans les feuilles de Arabidopsis thaliana—Une mauvaise herbe à fleurs de la famille des moutardes, couramment utilisée comme modèle en recherche. Ils ont ensuite analysé la réponse de la plante afin d'identifier précisément l'état de chaque cellule lors de l'infection. Ce faisant, ils ont découvert un nouvel état de réponse immunitaire, appelé PRIMER, qui émergeait dans les cellules à des points chauds immunitaires spécifiques. Les cellules PRIMER exprimaient un nouveau facteur de transcription – un type de protéine régulant l'expression des gènes – appelé GT-3a, qui constitue probablement une importante alarme en amont pour alerter les autres cellules d'une réponse immunitaire active de la plante.
De plus, les cellules entourant ces cellules PRIMER se sont révélées tout aussi importantes. Appelées « cellules témoins », les cellules immédiatement voisines des cellules PRIMER exprimaient des gènes permettant la communication intercellulaire à longue distance. Les chercheurs prévoient d'élucider cette relation lors de futures recherches, mais pour l'instant, ils soupçonnent que les interactions entre PRIMER et les cellules témoins sont essentielles à la propagation de la réponse immunitaire à travers la feuille.
Cette nouvelle perspective spatiotemporelle et cellulaire spécifique sur la réponse immunitaire des plantes est déjà disponible comme base de données de référence Pour les chercheurs du monde entier. Alors que les agents pathogènes continuent d'évoluer et de se propager dans un contexte de changements environnementaux liés au climat et de résistance croissante aux antibiotiques, la base de données offre un tremplin important pour préserver un avenir rempli de plantes et de cultures saines.
« Il existe actuellement un vif intérêt et une forte demande pour des atlas cellulaires détaillés. Nous sommes donc ravis d'en créer un nouveau, accessible au public et utilisable par d'autres chercheurs », déclare Ecker. « Notre atlas pourrait mener à de nombreuses découvertes sur la façon dont les cellules végétales réagissent aux facteurs de stress environnementaux, ce qui sera crucial pour créer des cultures plus résilientes au climat. »
D'autres auteurs incluent Joseph Nery de Salk ; Alexander Monell de Salk et de l'UC San Diego ; Travis Lee de Salk et du Howard Hughes Medical Institute ; Yuka Sakata, Shoma Shirahama et Akira Mine de l'Université de Kyoto au Japon.
Le travail a été soutenu par le Howard Hughes Medical Institute et le Human Frontiers Science Program.
DOI: 10.1038 / s41586-024-08383-z
BLOG
Nature
AUTEURS
Tatsuya Nobori, Alexander Monell, Travis A. Lee, Yuka Sakata, Shoma Shirahama, Jingtian Zhou, Joseph Nery, Akira Mine et Joseph R. Ecker
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.