
le 7 avril 2021
Une enzyme jouant un rôle central dans le cancer et le diabète de type 2 active également la protéine de « nettoyage » dans la maladie de Parkinson
Une enzyme jouant un rôle central dans le cancer et le diabète de type 2 active également la protéine de « nettoyage » dans la maladie de Parkinson
LA JOLLA — Lorsque les cellules sont stressées, des alarmes chimiques se déclenchent, déclenchant une activité intense qui protège les acteurs les plus importants de la cellule. Durant cette période, une protéine appelée Parkin se dépêche de protéger les mitochondries, les centrales énergétiques qui produisent l'énergie nécessaire à la cellule. Les chercheurs de Salk ont désormais découvert un lien direct entre un capteur principal du stress cellulaire et Parkin elle-même. Cette même voie est également liée au diabète de type 2 et au cancer, ce qui pourrait ouvrir une nouvelle voie pour traiter ces trois maladies.
« Nos résultats représentent, et de loin, la première étape de la réaction d'alarme de Parkin jamais observée. Tous les autres événements biochimiques connus se produisent en une heure ; nous avons maintenant découvert un phénomène qui se produit en cinq minutes », explique le professeur. Ruben Shaw, directeur du Salk Cancer Center, désigné par le NCI, et auteur principal du nouveau travail, détaillé dans Science Advances le 7 avril 2021. « Décoder cette étape majeure dans la façon dont les cellules éliminent les mitochondries défectueuses a des implications pour un certain nombre de maladies. »
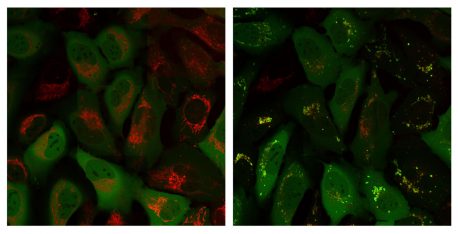
Le rôle de Parkin est d'éliminer les mitochondries endommagées par le stress cellulaire afin que de nouvelles puissent prendre leur place, un processus appelé mitophagie. Cependant, Parkin est muté dans la maladie de Parkinson familiale, ce qui rend la protéine incapable d'éliminer les mitochondries endommagées. Si les scientifiques savent depuis un certain temps que Parkin détecte le stress mitochondrial et déclenche le processus de mitophagie, personne ne comprend exactement comment Parkin détecte pour la première fois des problèmes mitochondriaux : Parkin savait d'une manière ou d'une autre comment mitochondrial devait migrer vers les mitochondries après une lésion mitochondriale, mais aucun signal ne lui était connu avant son arrivée.
Le laboratoire de Shaw, réputé pour ses travaux dans les domaines du métabolisme et du cancer, a consacré des années à des recherches intensives sur la régulation cellulaire d'un processus plus général de nettoyage et de recyclage appelé autophagie. Il y a une dizaine d'années, ils ont découvert qu'une enzyme appelée AMPK, très sensible aux stress cellulaires de toutes sortes, notamment aux lésions mitochondriales, contrôle l'autophagie en activant une enzyme appelée ULK1.
Suite à cette découverte, Shaw et l'étudiante diplômée Portia Lombardo ont commencé à rechercher des protéines liées à l'autophagie directement activées par ULK1. Ils ont examiné une cinquantaine de protéines différentes, espérant qu'environ 50 % correspondraient à ce critère. Ils ont été stupéfaits de constater que Parkin arrivait en tête de liste. Les voies biochimiques sont généralement très complexes, impliquant jusqu'à 10 participants, chacun activant le suivant. Découvrir qu'un processus aussi important que la mitophagie est initié par seulement trois participants – d'abord AMPK, puis ULK50, puis Parkin – était si surprenant que Shaw avait du mal à y croire.
Pour confirmer ces résultats, l'équipe a utilisé la spectrométrie de masse pour déterminer précisément où ULK1 fixait un groupe phosphate à Parkin. Ils ont découvert qu'il se situait dans une nouvelle région que d'autres chercheurs avaient récemment identifiée comme essentielle à l'activation de Parkin, sans en connaître la raison. Chien-Min Hung, chercheur postdoctoral du laboratoire de Shaw, a ensuite réalisé des études biochimiques précises pour vérifier chaque aspect de la chronologie et déterminer quelles protéines faisaient quoi, et où. Les recherches de Shaw commencent maintenant à expliquer cette première étape clé de l'activation de Parkin, qui, selon Shaw, pourrait servir de signal d'avertissement de l'AMPK, le long de la chaîne de commandement, via ULK1, jusqu'à Parkin, pour examiner les mitochondries après une première vague de dommages et, si nécessaire, déclencher la destruction des mitochondries trop gravement endommagées pour retrouver leur fonction.
Ces résultats ont de vastes implications. L'AMPK, le capteur central du métabolisme cellulaire, est elle-même activée par une protéine suppressive de tumeur appelée LKB1, impliquée dans de nombreux cancers, comme l'ont établi Shaw dans des travaux antérieurs, et elle est également activée par un médicament contre le diabète de type 2, la metformine. Parallèlement, de nombreuses études montrent que les patients diabétiques sous metformine présentent un risque moindre de cancer et de comorbidités liées au vieillissement. La metformine est d'ailleurs actuellement considérée comme l'un des premiers traitements « anti-âge » jamais testés dans le cadre d'essais cliniques.
« Pour moi, le principal enseignement est que le métabolisme et les changements dans la santé des mitochondries sont essentiels dans le cancer, le diabète et les maladies neurodégénératives », explique Shaw, titulaire de la chaire William R. Brody. « Nos résultats indiquent qu'un médicament contre le diabète activant l'AMPK, dont nous avons déjà démontré la capacité à inhiber le cancer, pourrait également contribuer à restaurer la fonction chez les patients atteints de maladies neurodégénératives. En effet, les mécanismes généraux qui sous-tendent la santé des cellules de notre corps sont bien plus intégrés qu'on aurait pu l'imaginer. »
BLOG
Science Advances
AUTEURS
Chien-Min Hung, Portia S. Lombardo, Nazma Malik, Sonja N. Brun, Kristina Hellberg, Jeanine L. Van Nostrand, Daniel Garcia, Joshua Baumgart, Ken Diffenderfer, John M. Asara et Reuben J. Shaw
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.