
25 janvier 2022
Les chercheurs de Salk découvrent que le cannabinol préserve la fonction mitochondriale et prévient les dommages oxydatifs aux cellules
Les chercheurs de Salk découvrent que le cannabinol préserve la fonction mitochondriale et prévient les dommages oxydatifs aux cellules
LA JOLLA — Des décennies de recherche sur le cannabis médical se sont concentrées sur les composés THC et CBD dans des applications cliniques. Cependant, les propriétés thérapeutiques du cannabinol (CBN) sont moins connues. Une nouvelle étude menée par des scientifiques de Salk montre comment le CBN peut protéger les cellules nerveuses des dommages oxydatifs, une voie majeure vers la mort cellulaire. Les résultats, publiés en ligne le 6 janvier 2022 dans la revue Biologie des radicaux libres et médecine, suggèrent que le CBN a le potentiel de traiter les maladies neurodégénératives liées à l'âge, comme la maladie d'Alzheimer.
« Nous avons découvert que le cannabinol protège les neurones du stress oxydatif et de la mort cellulaire, deux des principaux facteurs contribuant à la maladie d'Alzheimer », explique l'auteur principal. Paméla Maher, professeur-chercheur et directeur du laboratoire de neurobiologie cellulaire de Salk. « Cette découverte pourrait un jour conduire au développement de nouvelles thérapies pour traiter cette maladie et d'autres troubles neurodégénératifs, comme la maladie de Parkinson. »
Dérivé du cannabis, le CBN est moléculairement similaire au THC, mais n'est pas psychoactif. Il est également moins réglementé par la FDA. Des recherches antérieures menées par le laboratoire de Maher ont révélé que le CBN avait des propriétés neuroprotectrices, mais leur mode d'action n'était pas encore clair. Cette nouvelle étude explique désormais le mécanisme par lequel le CBN protège les cellules cérébrales des dommages et de la mort.
L'équipe de Maher a étudié le processus d'oxytose, également appelé ferroptose, qui se produirait lors du vieillissement cérébral. De plus en plus de preuves suggèrent que l'oxytose pourrait être une cause de la maladie d'Alzheimer. L'oxytose peut être déclenchée par la perte progressive d'un antioxydant appelé glutathion, provoquant des lésions et la mort des cellules nerveuses par oxydation des lipides. Dans le cadre de cette étude, les scientifiques ont traité les cellules nerveuses avec du CBN, puis ont introduit un agent stimulant les dommages oxydatifs.
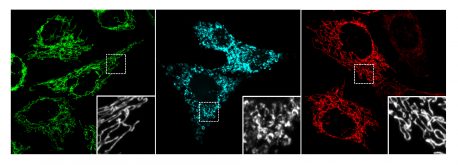
Ils ont également découvert que le CBN agissait en protégeant les mitochondries, véritables centrales énergétiques de la cellule, au sein des neurones. Dans les cellules endommagées, l'oxydation provoquait un enroulement des mitochondries comme des beignets – un changement également observé dans des cellules vieillissantes prélevées dans le cerveau de personnes atteintes de la maladie d'Alzheimer. Le traitement des cellules par le CBN empêchait l'enroulement des mitochondries et maintenait leur bon fonctionnement.
Pour confirmer l'interaction entre le CBN et les mitochondries, les chercheurs ont ensuite reproduit l'expérience sur des cellules nerveuses dépourvues de mitochondries. Dans ces cellules, le CBN n'a plus démontré son effet protecteur.
« Nous avons pu démontrer directement que le maintien de la fonction mitochondriale était spécifiquement nécessaire aux effets protecteurs du composé », a déclaré Maher.

Autre découverte clé : les chercheurs ont montré que le CBN n'activait pas les récepteurs cannabinoïdes, pourtant nécessaires à la production d'une réaction psychoactive. Ainsi, les traitements au CBN seraient efficaces sans provoquer d'effet psychotrope.
« Le CBN n'est pas une substance réglementée comme le THC, le composé psychotrope du cannabis, et des données probantes ont démontré son innocuité chez l'animal et l'humain. De plus, comme il agit indépendamment des récepteurs cannabinoïdes, il pourrait également agir sur une grande variété de cellules et offrir un potentiel thérapeutique important », explique Zhibin Liang, auteur principal et chercheur postdoctoral au laboratoire Maher.
Outre la maladie d'Alzheimer, ces résultats ont des implications pour d'autres maladies neurodégénératives, comme la maladie de Parkinson, également liée à la perte de glutathion. « Le dysfonctionnement mitochondrial est impliqué dans des modifications de divers tissus, et pas seulement dans le cerveau et le vieillissement. Par conséquent, la capacité de ce composé à maintenir la fonction mitochondriale suggère qu'il pourrait avoir des effets bénéfiques au-delà de la maladie d'Alzheimer », a déclaré Maher.
Maher ajoute que l'étude démontre la nécessité de poursuivre les recherches sur le CBN et d'autres cannabinoïdes moins étudiés. Dans une prochaine étape, l'équipe de Maher cherche à voir si elle peut reproduire ses résultats dans un modèle murin préclinique.
Les autres auteurs de l'étude sont David Soriano-Castell, Devin Kepchia, Antonio Currais et David Schubert de Salk ; et Brendan Duggan de l'Université de Californie à San Diego.
Ce travail a été financé par les National Institutes of Health, le Paul F. Glenn Center for Biology of Aging Research du Salk Institute, un Innovation Award du Salk Institute, la Shiley Foundation, la Bundy Foundation et l'Université de Californie à San Diego.
DOI: 10.1016/j.freeradbiomed.2022.01.001
BLOG
Biologie des radicaux libres et médecine
AUTEURS
Zhibin Liang, David Soriano-Castell, Devin Kepchia, Brendan M Duggan, Antonio Currais, David Schubert et Pamela Maher
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.