
13 janvier 2010
LA JOLLA, CA — Nous avons tous, à un moment ou à un autre, éprouvé les signes typiques d'une infection : fièvre, apathie, manque d'appétit. Ces symptômes sont orchestrés par le cerveau en réponse aux cytokines circulantes, les molécules de signalisation du système immunitaire. Mais la portée exacte des cytokines au-delà de la barrière hémato-encéphalique quasi impénétrable fait l'objet de nombreuses controverses.
Dans leur dernière étude, les chercheurs du Salk Institute for Biological Studies décrivent comment, selon la nature du stimulus, les macrophages résidents alignés le long de la barrière hémato-encéphalique jouent des rôles opposés dans la transmission des signaux immunitaires dans le cerveau.
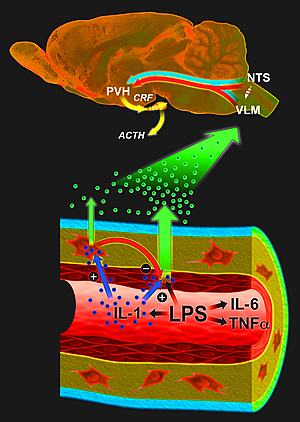
Les cellules endothéliales et les macrophages travaillent ensemble pour transmettre et moduler la force des signaux immunitaires inflammatoires au cerveau.
Image : Avec l'aimable autorisation de Jamie Simon, Salk Institute for Biological Studies.
« Ces macrophages agissent comme des accélérateurs pour enrôler la participation du cerveau dans la gestion des insultes immunitaires, mais lorsque cela est nécessaire, ils freinent brusquement pour empêcher la réponse inflammatoire centrale de prendre de l'ampleur », explique le chercheur postdoctoral Jordi Serrats, Ph.D., qui a codirigé l'étude avec Jennifer C. Schiltz, Ph.D., ancienne chercheuse postdoctorale au laboratoire de structure et de fonction neuronales de Salk et maintenant professeure adjointe à l'Uniformed Services University à Bethesda, Maryland.
Les résultats des chercheurs de Salk, publiés dans l'édition du 14 janvier 2010 de la revue Neuron, pourrait ouvrir la voie à de nouvelles thérapies pour les personnes souffrant de maladies neurodégénératives chroniques, telles que la sclérose latérale amyotrophique (SLA), la maladie de Parkinson, la maladie d'Alzheimer et les maladies à prions, dans lesquelles les mécanismes inflammatoires centraux jouent un rôle important.
« Le fait que nous ayons identifié un puissant mécanisme anti-inflammatoire dans le cerveau présente une nouvelle cible pour intervenir dans le large éventail de maladies du système nerveux central qui possèdent une composante inflammatoire », explique l'auteur principal de l'étude. Paul E. Sawchenko, Ph.D., professeur au Laboratoire de structure et de fonction neuronales.
En réponse à une infection, des cytokines inflammatoires, comme l'interleukine-1, sont produites au site de l'infection. Ces cytokines circulent dans le sang et communiquent avec les neurones cérébraux pour activer l'axe hypothalamo-hypophyso-surrénalien (HHS), partie intégrante du mécanisme cérébral de réponse au stress. L'axe HHS implique l'interaction de l'hypothalamus, l'hypophyse située juste en dessous de l'hypothalamus, et des glandes surrénales situées au sommet des reins.
Tel un centre de commandement central, l'hypothalamus sécrète un facteur de libération de corticotropine (CLR), qui stimule la sécrétion d'hormone adrénocorticotrope par l'hypophyse. Cette dernière signale aux glandes surrénales d'augmenter la production de glucocorticoïdes, qui mobilisent les réserves énergétiques pour faire face aux agressions inflammatoires. Mais ces hormones agissent également comme de puissants immunosuppresseurs, empêchant la production excessive de cytokines et la prolifération des cellules immunitaires.
« Les cytokines sont de grosses molécules qui ne traversent pas librement la barrière hémato-encéphalique », explique Sawchenko. « La question de savoir comment ces molécules accèdent au cerveau pour déclencher toute une série de réponses adaptatives telles que la fièvre, l'inactivité, la somnolence et l'activation du système nerveux central face au stress est un problème récurrent en neuroimmunologie depuis de nombreuses années. »
Des recherches antérieures menées par Sawchenko et d'autres chercheurs ont suggéré une voie vasculaire par laquelle les cytokines interagissent avec les parois vasculaires pour générer des messagers secondaires, qui activent ensuite les circuits cérébraux concernés. Les cellules endothéliales denses, qui tapissent près de 400 kilomètres de capillaires étroits à travers le cerveau, sont parfaitement positionnées pour enregistrer les signaux immunitaires circulants, mais elles nécessitent un signal très fort pour être activées. Les macrophages périvasculaires, en revanche, sont plus sensibles, mais n'ont pas d'accès direct à la circulation sanguine.
Pour démêler le rôle exact de ces deux types de cellules, Serrats a exploité la capacité des macrophages à absorber et ingérer des particules solides. Il a injecté des liposomes contenant du clodronate, un médicament capable de provoquer la mort cellulaire, dans le ventricule cérébral latéral. Les liposomes ont été absorbés par les macrophages, qui ont été sélectivement détruits.
Sans macrophages périvasculaires, les animaux étaient incapables de réagir à l'interleukine-1 sanguine et de déclencher les réponses cérébrales dites de phase aiguë, qui aident l'organisme à faire face au défi à relever, mais provoquent également la sensation familière de « se sentir malade ». Mais à leur grande surprise, les chercheurs de Salk ont découvert que ces mêmes cellules freinaient l'activité pro-inflammatoire des cellules endothéliales, qui forment la paroi des vaisseaux sanguins et ne sont activées – mais très puissamment une fois qu'elles le sont – que lorsqu'elles rencontrent le lipopolysaccharide, un composant clé de la paroi cellulaire de certaines bactéries.
« De nombreuses maladies neurodégénératives sont aggravées par une inflammation ou des infections systémiques », explique Sawchenko. « Une fois que nous aurons identifié les molécules qui assurent la communication bidirectionnelle entre les macrophages périvasculaires et les cellules endothéliales, nous pourrons développer des stratégies pour gérer les conséquences néfastes des réponses inflammatoires centrales sur la santé. »
Les chercheurs qui ont également contribué à l'étude comprennent les chercheurs postdoctoraux Borja García-Bueno, Ph.D., et Teresa M. Reyes, Ph.D., de l'Institut Salk, ainsi que Nico van Rooijen, Ph.D., professeur au centre médical Vrije Universiteit d'Amsterdam, aux Pays-Bas.
Les travaux ont été financés en partie par la Clayton Medical Research Foundation, les National Institutes of Health, le ministère espagnol de l'Éducation et des Sciences et CIBERsam.
À propos du Salk Institute for Biological Studies :
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies infectieuses en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale, et les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu