
le 30 avril 2015
Les découvertes de l'Institut Salk sur le syndrome de vieillissement prématuré pourraient conduire à un moyen de ralentir ou d'inverser le processus de vieillissement
Les découvertes de l'Institut Salk sur le syndrome de vieillissement prématuré pourraient conduire à un moyen de ralentir ou d'inverser le processus de vieillissement
LA JOLLA – Une étude reliant le processus de vieillissement à la détérioration de faisceaux d'ADN cellulaire étroitement emballés pourrait conduire à des méthodes de prévention et de traitement des maladies liées à l'âge telles que le cancer, le diabète et la maladie d'Alzheimer, comme détaillé le 30 avril 2015, dans Science.
Dans l'étude, des scientifiques de l'Institut Salk et de l' Académie chinoise des sciences Ils ont découvert que les mutations génétiques à l’origine du syndrome de Werner, un trouble qui conduit au vieillissement prématuré et à la mort, entraînaient la détérioration de faisceaux d’ADN connus sous le nom d’hétérochromatine.
Cette découverte, rendue possible grâce à une combinaison de technologies de pointe en matière de cellules souches et d’édition génétique, pourrait conduire à des moyens de contrer le déclin physiologique lié à l’âge en prévenant ou en inversant les dommages causés à l’hétérochromatine.
« Nos résultats montrent que la mutation génétique à l’origine du syndrome de Werner entraîne la désorganisation de l’hétérochromatine, et que cette perturbation de l’emballage normal de l’ADN est un facteur clé du vieillissement », explique Juan Carlos Izpisua Belmonte, auteur principal de l'article. « Cela a des implications au-delà du syndrome de Werner, car cela identifie un mécanisme central du vieillissement – la désorganisation de l'hétérochromatine – dont la réversibilité a été démontrée. »
Le syndrome de Werner est une maladie génétique qui entraîne un vieillissement plus rapide que la normale. Il touche environ une personne sur 200,000 2 aux États-Unis. Les personnes atteintes souffrent tôt de maladies liées à l'âge, notamment de cataracte, de diabète de type 40, de durcissement des artères, d'ostéoporose et de cancer, et la plupart décèdent vers la fin de la quarantaine ou le début de la cinquantaine.
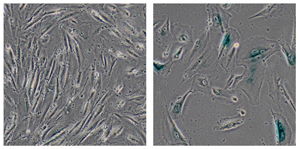
Des chercheurs de l'Institut Salk ont découvert qu'une protéine mutée dans le syndrome de Werner, une maladie du vieillissement prématuré, joue un rôle clé dans la stabilisation de l'hétérochromatine, une forme d'ADN fortement encapsulée. Plus généralement, ces résultats suggèrent que la désorganisation de l'hétérochromatine pourrait être un facteur clé du vieillissement. Cette image montre des cellules humaines normales (à gauche) et des cellules génétiquement modifiées développées par les scientifiques du Salk pour modéliser le syndrome de Werner (à droite), qui présentaient des signes de vieillissement, notamment leur grande taille.
Cliquez ici pour une image haute résolution.
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
La maladie est causée par une mutation du gène de type hélicase RecQ du syndrome de Werner, appelé gène WRN en abrégé, qui génère la protéine WRN. Des études antérieures ont montré que la forme normale de cette protéine est une enzyme qui préserve la structure et l'intégrité de l'ADN d'une personne. Lorsque la protéine est mutée dans le syndrome de Werner, elle perturbe la réplication et la réparation de l'ADN ainsi que l'expression des gènes, ce qui était considéré comme une cause de vieillissement prématuré. Cependant, on ne savait pas exactement comment la protéine WRN mutée perturbait ces processus cellulaires essentiels.
Dans leur étude, les scientifiques de Salk ont cherché à déterminer précisément comment la protéine WRN mutée provoque un tel chaos cellulaire. Pour ce faire, ils ont créé un modèle cellulaire du syndrome de Werner en utilisant une technologie de pointe d'édition génétique pour supprimer le gène WRN dans les cellules souches humaines. Ce modèle de cellules souches de la maladie a offert aux scientifiques une capacité sans précédent d'étudier le vieillissement rapide des cellules en laboratoire. Les cellules ainsi obtenues imitaient la mutation génétique observée chez les patients atteints du syndrome de Werner, de sorte que les cellules ont commencé à vieillir plus rapidement que la normale. En y regardant de plus près, les scientifiques ont découvert que la suppression du gène WRN entraînait également des perturbations de la structure de l'hétérochromatine, l'ADN dense présent dans le noyau cellulaire.
Ce faisceau d'ADN agit comme un commutateur pour contrôler l'activité des gènes et piloter la machinerie moléculaire complexe d'une cellule. À l'extérieur des faisceaux d'hétérochromatine se trouvent des marqueurs chimiques, appelés étiquettes épigénétiques, qui contrôlent la structure de l'hétérochromatine. Par exemple, des altérations de ces commutateurs chimiques peuvent modifier l'architecture de l'hétérochromatine, provoquant l'expression ou le silence des gènes.

De gauche à droite : Pradeep Reddy, Concepcion Rodriguez Esteban, Emi Suzuki, Mo Li, Juan Carlos Izpisua Belmonte, Alejandro Ocampo, Keiichiro Suzuki
Cliquez ici pour une image haute résolution.
Image : avec l'aimable autorisation du Salk Institute for Biological Studies
Les chercheurs de Salk ont découvert que la suppression du gène WRN entraîne une désorganisation de l'hétérochromatine, soulignant le rôle important de la protéine WRN dans le maintien de l'hétérochromatine. De plus, lors d'expériences ultérieures, ils ont montré que la protéine interagit directement avec des structures moléculaires connues pour stabiliser l'hétérochromatine, révélant ainsi une preuve irréfutable qui, pour la première fois, relie directement la protéine WRN mutée à la déstabilisation de l'hétérochromatine.
« Notre étude établit un lien entre le syndrome de Werner et la désorganisation de l'hétérochromatine, en décrivant un mécanisme moléculaire par lequel une mutation génétique entraîne une perturbation générale des processus cellulaires en perturbant la régulation épigénétique », explique Izpisua Belmonte. « Plus généralement, elle suggère que l'accumulation d'altérations dans la structure de l'hétérochromatine pourrait être une cause sous-jacente majeure du vieillissement cellulaire. Cela soulève la question de savoir si nous pouvons inverser ces altérations – comme en rénovant une vieille maison ou une vieille voiture – pour prévenir, voire inverser, le déclin et les maladies liés à l'âge. »
Izpisua Belmonte a ajouté que des études plus approfondies seront nécessaires pour comprendre pleinement le rôle de la désorganisation de l'hétérochromatine dans le vieillissement, notamment son interaction avec d'autres processus cellulaires impliqués dans le vieillissement, comme le raccourcissement des extrémités des chromosomes, appelées télomères. Par ailleurs, l'équipe d'Izpisua Belmonte développe des technologies d'édition épigénétique pour inverser les altérations épigénétiques jouant un rôle dans le vieillissement et les maladies humaines.
Parmi les autres auteurs de l'article figurent : Weiqi Zhang, Jingyi Li, Keiichiro Suzuki, Jing Qu, Ping Wang, Junzhi Zhou, Xiaomeng Liu, Ruotong Ren, Xiuling Xu, Alejandro Ocampo, Tingting Yuan, Jiping Yang, Ying Li, Liang Shi, Dee Guan, Huize Pan, Shunlei Duan, Zhichao Ding, Mo Li, Fei Yi, Ruijun Bai, Yayu Wang, Chang Chen, Fuquan Yang, Xiaoyu. Li, Zimei Wang, Emi Aizawa, April Goebl, Rupa Devi Soligalla, Pradeep Reddy, Concepcion Rodriguez Esteban, Fuchou Tang et Guang-Hui Liu.
Le financement de l'étude a été assuré par le Fondation Glenn, le Fondation caritative G. Harold et Leila Y. Mathers et la Leona M. et Harry B. Helmsley Charitable Trust.
À propos du Salk Institute for Biological Studies :
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies infectieuses en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale et les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
BLOG
Science
AUTEURS
Weiqi Zhang, Jingyi Li, Keiichiro Suzuki, Jing Qu, Ping Wang, Junzhi Zhou, Xiaomeng Liu, Ruotong Ren, Xiuling Xu, Alejandro Ocampo, Tingting Yuan, Jiping Yang, Ying Li, Liang Shi, Dee Guan, Huize Pan, Shunlei Duan, Zhichao Ding, Mo Li, Fei Yi, Ruijun Bai, Yayu Wang, Chang Chen, Fuquan Yang, Xiaoyu Li, Zimei Wang, Emi Aizawa, April Goebl, Rupa Devi Soligalla, Pradeep Reddy, Concepcion Rodriguez Esteban, Fuchou Tang, Guang-Hui Liu, Juan Carlos Izpisua Belmonte
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu