
24 mars
LA JOLLA, CA — Les poissons osseux comme le minuscule poisson zèbre possèdent une capacité remarquable dont les mammifères ne peuvent que rêver : si on leur coupe un morceau de cœur, ils nagent lentement pendant quelques jours, mais au bout d'un mois, ils paraissent parfaitement normaux. Comment y parviennent-ils ? Ou, plus important encore, pourquoi nous n'y parvenons pas, est l'une des questions majeures de la médecine régénérative actuelle.
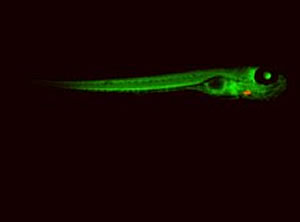
Izpisúa Belmonte et son équipe ont utilisé des poissons zèbres dont le cœur brille en rouge pour identifier les cellules qui permettent aux cœurs blessés des poissons zèbres de se réparer.
Image : Avec l'aimable autorisation de Juan Carlos Izpisúa Belmonte, Salk Institute for Biological Studies
Dans un article publié dans le numéro du 25 mars 2010 de NatureDes chercheurs travaillant à l'Institut Salk d'études biologiques et au Centre de médecine régénérative de Barcelone (CMRB) ont identifié une population de cellules cardiaques de poisson qui est à l'origine de cet étonnant exploit de guérison, une découverte qui pourrait donner un aperçu de la manière dont les cœurs des mammifères pourraient être amenés à se réparer après une blessure provoquée par une crise cardiaque.
Juan Carlos Izpisua Belmonte, Ph. D., professeur au Laboratoire d'expression génétique, et ses collègues rapportent que ce ne sont pas les cellules souches – ces suspects « habituels » de régénération – qui réparent un cœur de poisson blessé. La réparation est plutôt assurée par des cellules musculaires cardiaques différenciées appelées cardiomyocytes, ces cellules adultes dont la fonction normale est de fournir la force contractile du cœur.
« Ce que les résultats de notre étude montrent, c'est que la mère nature utilise d'autres moyens que de remonter jusqu'aux cellules souches pluripotentes pour régénérer les tissus et les organes », explique Izpisúa Belmonte, notant qu'au moins chez les poissons, le corps peut avoir développé des stratégies de réparation surprenantes entraînées par des types de cellules plus anciennes que les cellules souches.
Pour identifier quelles cellules remplissaient réellement le muscle cardiaque excisé du poisson zèbre, l'équipe d'Izpisúa Belmonte a d'abord eu recours au génie génétique pour rendre les cardiomyocytes « transgéniques » en y insérant un gène traceur qui les faisait briller en vert sous un microscope.
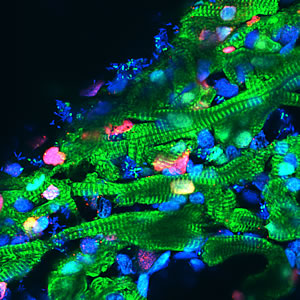
Les cellules du muscle cardiaque (représentées en vert) régressent vers un état plus jeune après une blessure, recommencent à se diviser (indiqué par un marqueur rouge) pour reconstituer les cellules perdues, puis mûrissent une seconde fois en cardiomyocytes.
Image : Avec l'aimable autorisation de Juan Carlos Izpisúa Belmonte, Salk Institute for Biological Studies
Ils ont ensuite littéralement coupé environ 20 % de chaque ventricule de poisson et ont attendu quelques semaines pour que les cœurs se régénèrent : si le muscle cardiaque régénéré ne brillait pas, cela signifierait que des cellules autres que les cardiomyocytes, comme une population de cellules souches cardiaques, avaient remplacé le muscle endommagé.
Mais, dans une découverte frappante, toutes les cellules musculaires cardiaques régénérées brillaient en vert, indiquant que les cardiomyocytes bien établis, restés après une lésion, avaient probablement régressé vers un état plus « jeune », recommencé à se diviser pour reconstituer les cellules perdues, puis mûri une seconde fois en nouveau muscle cardiaque. L'équipe a également montré que les cardiomyocytes retrouvaient leur jeunesse perdue, en partie en réactivant la production de protéines associées à la prolifération cellulaire, facteurs généralement exprimés chez les progéniteurs immatures.
Le cœur humain ne peut pas subir seul ce type de changements régénératifs. Endommagé par une crise cardiaque, notre muscle cardiaque est remplacé par du tissu cicatriciel incapable de se contracter. Cependant, avant l'insuffisance cardiaque, les cellules musculaires cardiaques endommagées des mammifères entrent dans un état de survie appelé « hibernation », où elles cessent de se contracter pour survivre.
Chris Jopling, Ph. D., chercheur postdoctoral d'Izpisúa Belmonte au CMRB et premier auteur de l'étude, considère l'hibernation cardiaque humaine comme importante. « Lors de la régénération cardiaque chez le poisson-zèbre, nous avons constaté que les cardiomyocytes présentaient des modifications structurelles similaires à celles observées chez les cardiomyocytes en hibernation », a-t-il déclaré, soulignant que ces modifications étaient en réalité nécessaires à la division des cardiomyocytes de poisson. « Compte tenu de ces similitudes, nous émettons l'hypothèse que les cardiomyocytes de mammifères en hibernation pourraient représenter des cellules qui tentent de proliférer. »
La bonne nouvelle, c'est que le cœur des mammifères peut subir une sorte de « réduction » métabolique, prélude à la division cellulaire. « Cette idée concorde parfaitement avec les conclusions de plusieurs groupes : l'expression forcée de régulateurs du cycle cellulaire peut induire la prolifération des cardiomyocytes chez les mammifères », explique Jopling. « Il leur suffit peut-être d'un petit coup de pouce. »
Des recherches sont en cours pour identifier les facteurs susceptibles d'apporter cette « poussée ». Bien qu'optimiste quant aux résultats, Izpisúa Belmonte estime également que l'étude devrait inciter les chercheurs à ne pas négliger les contributions potentielles des cellules matures à la régénération. « Nous ne pouvons plus considérer les cellules différenciées comme un point final statique du processus de différenciation », déclare Izpisúa Belmonte, qui dirige également le CMRB. « Si nous pouvions reproduire chez les cellules de mammifères ce qui se passe chez le poisson zèbre, nous pourrions peut-être comprendre pourquoi la régénération ne se produit pas chez l'homme. »
Ont également contribué à ce travail Merce Marti, Ph.D., Angel Raya, MD, Ph.D., Edward Sleep et Marina Raya, tous du CMRB en Espagne.
L'étude a été financée en partie par la Fundacion Cellex, la Fondation Ipsen, la Fondation caritative G. Harold et Leila Y. Mathers, les National Institutes of Health et Sanofi-Aventis.
-Élise Lamar
À propos de l'Institut Salk d'études biologiques
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies infectieuses en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale, et les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu