
2 de noviembre de 2015
Al analizar más de 4.000 genes en tumores humanos, un equipo del Salk descubrió una enzima responsable de suprimir un tipo común y mortal de cáncer de pulmón.
Al analizar más de 4.000 genes en tumores humanos, un equipo del Salk descubrió una enzima responsable de suprimir un tipo común y mortal de cáncer de pulmón.
LA JOLLA–Científicos del Instituto Salk descubrieron una molécula cuya mutación conduce al crecimiento agresivo de un tipo común y mortal de cáncer de pulmón. cáncer en humanos.
Esta enzima, llamada EphA2, normalmente vigila un gen responsable del crecimiento de tejidos. Pero cuando EphA2 se muta, el equipo de Salk descubrió, los sistemas celulares pueden descontrolarse y desarrollar tumores rápidamente. El nuevo trabajo, publicado la semana del 2 de noviembre de 2015 en PNAS, sugiere que EphA2 podría ser un nuevo objetivo para un subconjunto de cáncer de pulmón, que afecta tanto a no fumadores como a fumadores, y es la principal causa de muertes relacionadas con el cáncer en todo el mundo.
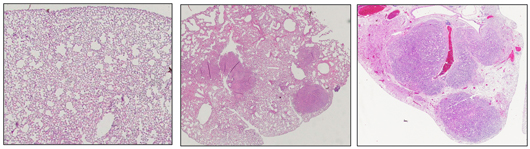
Científicos de Salk descubren una molécula en humanos llamada EphA2 que actúa como supresora de tumores en ciertos tipos de cáncer de pulmón. Esta imagen muestra tejido pulmonar normal de ratón (izquierda) y pulmones con tumores resultantes de una mutación KRAS (centro). Cuando se elimina EphA2, la mutación KRAS resulta en muchos más tumores y de mayor tamaño durante el mismo período de tiempo (derecha).
Haga clic aquí para obtener una imagen en alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
“A veces, hay cientos de mutaciones en los genes de los tumores de un paciente, pero no se sabe si son impulsoras de la enfermedad o subproductos”, dice el autor principal. Inder Verma, profesor de genética y titular de la Cátedra Irwin y Joan Jacobs de Ciencias Ejemplares de la Vida en Salk. “Encontramos una nueva forma de identificar genes supresores de tumores y comprender cómo podrían ser el objetivo de terapias”.”
Dos mutaciones genéticas en particular son conocidas por estimular el crecimiento de tumores humanos: KRAS y p53. Aunque ambos genes han sido estudiados exhaustivamente, son difíciles de tratar terapéuticamente, por lo que el equipo Salk decidió buscar genes que pudieran controlar KRAS y p53 en su lugar.
Los investigadores se enfocaron en los 4.700 genes del genoma humano relacionados con la señalización celular, específicamente, genes que tienen la capacidad de disminuir el crecimiento y la proliferación celular. Luego, el equipo adaptó una técnica de cribado genético para probar de manera rápida y eficiente el efecto de estos miles de genes en el desarrollo de tumores. En modelos animales, el equipo de Salk descubrió que 16 de estos genes de señalización celular producían moléculas que tenían un efecto significativo en los tumores relacionados con KRAS y p53.
De estas 16 moléculas, una destacó especialmente: la enzima EphA2, descubierta originalmente en el laboratorio de otro científico de Salk, Tony Hunter. Anteriormente, la importancia de EphA2 en el cáncer de pulmón no estaba clara, pero el equipo descubrió que su ausencia hacía que los tumores asociados a KRAS crecieran de forma mucho más agresiva.
“Con una mutación en KRAS, un tumor se forma en 300 días. Pero sin EphA2, la mutación KRAS conduce a tumores en la mitad de tiempo, de 120 a 150 días”, afirma Verma, quien también es Profesor de Biología Molecular de la American Cancer Society. “Esta molécula EphA2 tiene un enorme efecto en la restricción del crecimiento del cáncer cuando KRAS está mutado”. KRAS mutado es un culpable común en aproximadamente entre el 10 y el 20 por ciento de todos los cánceres, particularmente el cáncer de colon y el cáncer de pulmón humano.

De izquierda a derecha: los investigadores de Salk Yifeng Xia, Eugene Ke, Narayana Yeddula e Inder Verma
Haga clic aquí para obtener una imagen en alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
“Dado que la activación de EphA2 llevó a la supresión tanto de la señalización celular como de la proliferación celular, creemos que la enzima podría servir como un posible objetivo farmacológico en el adenocarcinoma de pulmón dependiente de KRAS”, dice Narayana Yeddula, asociada de investigación de Salk y primera autora del artículo.
Un proyecto nacional de 10 años llamado The Cancer Genome Atlas mapeó los genomas de cientos de pacientes con más de 20 tipos de cáncer diferentes y descubrió varias mutaciones genéticas relacionadas, aunque el papel de estas mutaciones no se ha entendido bien en el cáncer de pulmón (especialmente el adenocarcinoma, que representa casi una cuarta parte de todos los cánceres de pulmón). A partir de los datos del Cancer Genome Atlas, el equipo de Salk descubrió que las alteraciones genéticas de EphA2 se detectaron en 54 de 230 pacientes con adenocarcinoma. El equipo también descubrió, sorprendentemente, que la pérdida de EphA2 activaba una vía comúnmente asociada con el cáncer (denominada Hedgehog) que promueve el crecimiento tumoral.
“Curiosamente, entre los pacientes humanos con cáncer de pulmón y mutaciones en EphA2, alrededor del 8 por ciento de los pacientes tienen en realidad una alta expresión de EphA2. Por lo tanto, en algunos casos, EphA2 no está suprimiendo tumores y puede depender del contexto. Por ello, necesitamos evaluar cuidadosamente la función de la molécula al diseñar nuevas terapias”, añade Yifeng Xia, investigadora del personal de Salk involucrada en el trabajo.
Otros autores del artículo fueron Eugene Ke del Instituto Salk y Joep Beumer del Instituto Salk y del Instituto Hubrecht en los Países Bajos.
Este trabajo fue apoyado en parte por un NIH subvención Salk Cancer Center Core, Ipsen, la Fundación H.N. and Frances C. Berger, y el Fundación Benéfica Leona M. y Harry B. Helmsley.
DIARIO
PNAS
TÍTULO
Cribado de supresores de tumores: la pérdida del receptor ephrin A2 coopera con KRAS oncogénico en la promoción del adenocarcinoma de pulmón
AUTORES
Narayana Yeddula, Yifeng Xia, Eugene Ke, Joep Beumer e Inder M. Verma
Oficina de Comunicaciones
Tel.: (858) 453-4100
press@salk.edu
El Instituto Salk es un centro de investigación independiente y sin fines de lucro fundado en 1960 por Jonas Salk, creador de la primera vacuna segura y eficaz contra la poliomielitis. La misión del Instituto es impulsar una investigación fundamental, colaborativa y audaz que aborde los retos más acuciantes de la sociedad, entre ellos el cáncer, la enfermedad de Alzheimer y la vulnerabilidad agrícola. Esta ciencia fundamental sustenta todos los esfuerzos traslacionales, generando conocimientos que permiten el desarrollo de nuevos medicamentos e innovaciones en todo el mundo.