
6 de julio de 2022
Las vistas detalladas de la proteína del VIH podrían conducir a nuevos tratamientos contra el virus
Las vistas detalladas de la proteína del VIH podrían conducir a nuevos tratamientos contra el virus
LA JOLLA—Comprender cómo el VIH se replica dentro de las células es clave para desarrollar nuevas terapias que podrían ayudar a casi 40 millones de personas que viven con el VIH en todo el mundo. Ahora, un equipo de científicos del Instituto Salk y la Universidad de Rutgers ha determinado por primera vez la estructura molecular del Pol del VIH, una proteína que desempeña un papel clave en las etapas tardías de la replicación del VIH, o el proceso a través del cual el virus se propaga y se disemina por el cuerpo. Es importante destacar que determinar la estructura de la molécula ayuda a responder preguntas de larga data sobre cómo la proteína se descompone para avanzar en el proceso de replicación. El descubrimiento, publicado en Science Advances el 6 de julio de 2022, revela una nueva vulnerabilidad en el virus que podría ser atacada con medicamentos.
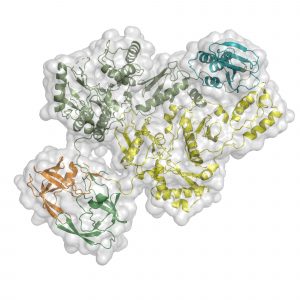
“La estructura informa la función y las ideas que obtuvimos al visualizar la arquitectura molecular de Pol nos brindan una nueva comprensión del mecanismo por el cual el VIH se replica”, dice el coautor principal. Dmitry Lyumkis, profesor asistente en el Laboratorio de Genética y Silla de Desarrollo de la Fundación Hearst en Salk.
Los científicos sabían previamente que el Pol del VIH, una poliproteína, se descompone en tres enzimas –una proteasa, una transcriptasa inversa y una integrasa– que trabajan juntas para ensamblar la forma madura del virus. La proteasa desempeña un papel fundamental al iniciar este proceso al fragmentar la molécula para separar los otros componentes. Sin embargo, hasta ahora se desconocía cómo la proteasa se liberaba a sí misma, primero de la poliproteína más grande Gag-Pol del VIH y luego del Pol del VIH, para llevar a cabo esta tarea. El nuevo artículo sugiere que la proteasa inicia el proceso auto-cortándose o cortándose para liberarse del resto de la molécula, con la ayuda de la transcriptasa inversa y, posiblemente, la integrasa.
“Se sabía (pero no se comprendía) que existe un acoplamiento entre estas enzimas antes de que el Pol del VIH se descomponga. La visualización de la estructura del Pol del VIH explica la base de este complejo mecanismo”, afirma Eddy Arnold, coautor principal, profesor de la junta de gobernadores y profesor distinguido en el Centro de Biotecnología Avanzada y Medicina de la Universidad de Rutgers.
“El primer desafío fue producir una versión estable del VIH Pol para que la estructura pudiera ser analizada, lo que nunca antes se había informado”, dice Jerry Joe Harrison, coautor principal y profesor titular de la Universidad de Ghana.

“Esta era una pieza clave que faltaba en el rompecabezas estructural del VIH”, añade Arnold.
El equipo utilizó microscopía electrónica criogénica, una técnica de imagen a la que Lyumkis ha hecho importantes contribuciones, para revelar la estructura tridimensional de la molécula de proteína pol del VIH. Esto llevó al descubrimiento de que Pol es un dímero, lo que significa que está formado por dos proteínas unidas. El hallazgo fue una sorpresa porque otras proteínas virales similares son ensamblajes de una sola proteína.
El grupo demostró que en esta estructura de dos caras, el componente proteasa de Pol está “ligeramente unido” al componente transcriptasa inversa en una configuración de unión que mantiene la proteasa ligeramente flexible.
“Mantiene a la proteasa a distancia, de forma laxa, y creemos que esto le da a la proteasa un poco de movimiento, lo que a su vez le permite iniciar el corte de poliproteínas, un requisito previo para la maduración viral”, dice el co-primer autor Dario Passos, un exinvestigador del laboratorio de Lyumkis en Salk. ’Los tratamientos actuales contra el VIH incluyen múltiples clases de inhibidores para las tres enzimas, y el descubrimiento también revela una nueva vulnerabilidad que podría ser atacada con medicamentos“.”
Los autores dicen que el descubrimiento abre la puerta a importante investigación de seguimiento, incluidos estudios sobre la estructura de la poliproteína Gag-Pol, más grande y compleja, también involucrada en el ensamblaje viral, así como a examinar más de cerca el papel de la integrasa en el ensamblaje de la forma madura del virus VIH durante la replicación.
Otros autores incluyeron a Jessica F. Bruhn del Salk; Joseph Bauman, Lynda Tuberty y Francesc Xavier Ruiz de Rutgers; y Jeffrey DeStefano de la Universidad de Maryland.
El trabajo fue financiado por los Institutos Nacionales de Salud, el Instituto Internacional de Educación, el programa Fulbright, la Fundación Margaret T. Morris y las Fundaciones Hearst.
DOI: 10.1126/sciadv.abn9874
DIARIO
Science Advances
AUTORES
Jerry Joe E. K. Harrison, Dario Oliveira Passos, Jessica F. Bruhn, Joseph D. Bauman, Lynda Tuberty, Jeffrey J. DeStefano, Francesc Xavier Ruiz, Dmitry Lyumkis, Eddy Arnold
Oficina de Comunicaciones
Tel.: (858) 453-4100
press@salk.edu
El Instituto Salk es un centro de investigación independiente y sin fines de lucro fundado en 1960 por Jonas Salk, creador de la primera vacuna segura y eficaz contra la poliomielitis. La misión del Instituto es impulsar una investigación fundamental, colaborativa y audaz que aborde los retos más acuciantes de la sociedad, entre ellos el cáncer, la enfermedad de Alzheimer y la vulnerabilidad agrícola. Esta ciencia fundamental sustenta todos los esfuerzos traslacionales, generando conocimientos que permiten el desarrollo de nuevos medicamentos e innovaciones en todo el mundo.