
16 Julio 2014
El tratamiento revierte los síntomas de la diabetes tipo 2 en ratones sin efectos secundarios.
El tratamiento revierte los síntomas de la diabetes tipo 2 en ratones sin efectos secundarios.
LA JOLLA—En ratones con diabetes inducida por dieta—el equivalente del tipo 2 diabetes en humanos: una sola inyección de la proteína FGF1 es suficiente para restaurar los niveles de azúcar en la sangre a un rango saludable durante más de dos días. El descubrimiento de los científicos de Salk, publicado hoy en la revista Nature, podría dar lugar a una nueva generación de medicamentos para la diabetes más seguros y eficaces.
El equipo encontró que el tratamiento sostenido con la proteína no solo mantiene el azúcar en la sangre bajo control, sino que también revierte la insensibilidad a la insulina, la causa fisiológica subyacente de la diabetes. Igualmente emocionante, el tratamiento recientemente desarrollado no produce efectos secundarios comunes a la mayoría de los tratamientos actuales para la diabetes.
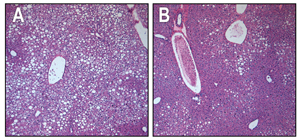
En el tejido hepático de los animales obesos con diabetes tipo 2, las células llenas de grasa no saludables son prolíficas (pequeños glóbulos blancos, panel A). Después del tratamiento crónico a través de inyecciones de FGF1, las células hepáticas pierden grasa y absorben azúcar del torrente sanguíneo (pequeñas células moradas, panel B) y se asemejan más a las células de animales normales no diabéticos.
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
“Controlar la glucosa es un problema dominante en nuestra sociedad”, dice ronald m evans, director de Salk's Laboratorio de Expresión Génica y autor correspondiente del artículo. “Y FGF1 ofrece un nuevo método para controlar la glucosa de una manera poderosa e inesperada”.
La diabetes tipo 2, que puede ser provocada por el exceso de peso y la inactividad, se ha disparado en las últimas décadas en los Estados Unidos y en todo el mundo. Se estima que casi 30 millones de estadounidenses padecen la enfermedad, en la que la glucosa se acumula en el torrente sanguíneo porque no se produce suficiente insulina que transporta el azúcar o porque las células se han vuelto resistentes a la insulina, ignorando las señales para absorber el azúcar. Como enfermedad crónica, la diabetes puede causar serios problemas de salud y no tiene una cura específica. Más bien se maneja, con diferentes niveles de éxito, a través de una combinación de dieta, ejercicio y productos farmacéuticos.
Los medicamentos para la diabetes actualmente en el mercado tienen como objetivo aumentar los niveles de insulina y revertir la resistencia a la insulina al cambiar los niveles de expresión de los genes para reducir los niveles de glucosa en la sangre. Pero los medicamentos, como Byetta, que aumentan la producción de insulina en el cuerpo, pueden hacer que los niveles de glucosa bajen demasiado y provocar una hipoglucemia potencialmente mortal, así como otros efectos secundarios.
En 2012, Evans y sus colegas descubrieron que un factor de crecimiento ignorado durante mucho tiempo tenía una función oculta: ayuda al cuerpo a responder a la insulina. Inesperadamente, los ratones que carecen del factor de crecimiento, llamado FGF1, desarrollan rápidamente diabetes cuando se los somete a una dieta rica en grasas, un hallazgo que sugiere que el FGF1 desempeñó un papel clave en el control de los niveles de glucosa en sangre. Esto llevó a los investigadores a preguntarse si proporcionar FGF1 adicional a los ratones diabéticos podría afectar los síntomas de la enfermedad.
El equipo de Evans inyectó dosis de FGF1 en ratones obesos con diabetes para evaluar el impacto potencial de la proteína en el metabolismo. Los investigadores quedaron atónitos por lo que sucedió: encontraron que con una sola dosis, los niveles de azúcar en la sangre bajaron rápidamente a niveles normales en todos los ratones diabéticos.
“Muchos estudios previos que inyectaron FGF1 no mostraron ningún efecto en ratones sanos”, dice Michael Downes, científico senior y coautor correspondiente del nuevo trabajo. “Sin embargo, cuando lo inyectamos en un ratón diabético, vimos una mejora dramática en la glucosa”.

Desde la izquierda: Jae Myoung Suh, Annette Atkins, Michael Downes, Maryam Ahmadian, Ronald Evans y Ruth Yu del Laboratorio de Expresión Génica
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Los investigadores encontraron que el tratamiento con FGF1 tenía una serie de ventajas sobre el medicamento para la diabetes Actos, que está asociado con efectos secundarios que van desde un aumento de peso no deseado hasta problemas cardíacos y hepáticos peligrosos. Es importante destacar que FGF1, incluso en dosis altas, no desencadenó estos efectos secundarios ni provocó que los niveles de glucosa cayeran a niveles peligrosamente bajos, un factor de riesgo asociado con muchos agentes reductores de glucosa. En cambio, las inyecciones restauraron la capacidad del cuerpo para regular naturalmente los niveles de insulina y azúcar en la sangre, manteniendo las cantidades de glucosa dentro de un rango seguro, revirtiendo de manera efectiva los síntomas centrales de la diabetes.
"Con FGF1, realmente no hemos visto hipoglucemia u otros efectos secundarios comunes", dice Jae Myoung Suh, investigador postdoctoral de Salk, miembro del laboratorio de Evans y primer autor del nuevo artículo. "Puede ser que FGF1 conduzca a un tipo de respuesta más 'normal' en comparación con otros medicamentos porque se metaboliza rápidamente en el cuerpo y se dirige a ciertos tipos de células".
El mecanismo de FGF1 aún no se comprende por completo, ni el mecanismo de la resistencia a la insulina, pero el grupo de Evans descubrió que la capacidad de la proteína para estimular el crecimiento es independiente de su efecto sobre la glucosa, lo que acerca a la proteína un paso más al uso terapéutico.
“Hay muchas preguntas que surgen de este trabajo y las vías para investigar el FGF1 en la diabetes y el metabolismo ahora están abiertas de par en par”, dice Evans. Precisar las vías de señalización y los receptores con los que interactúa FGF1 es una de las primeras preguntas que le gustaría abordar. También está planeando ensayos en humanos de FGF1 con colaboradores, pero llevará tiempo ajustar la proteína en un fármaco terapéutico.
“Queremos llevar esto a las personas mediante el desarrollo de una nueva generación de variantes de FGF1 que afecten únicamente a la glucosa y no al crecimiento celular”, dice. “Si podemos encontrar la variación perfecta, creo que tendremos en nuestras manos una herramienta muy nueva y muy efectiva para el control de la glucosa”.
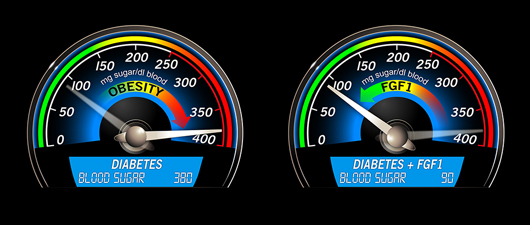
En esta analogía, demasiada azúcar en el torrente sanguíneo equivale a un automóvil en la zona de peligro. En la diabetes tipo 2 (comúnmente asociada con la obesidad), el cuerpo no puede usar el azúcar adecuadamente, lo que genera serios problemas de salud. Se ha demostrado que el factor de crecimiento FGF1 disminuye la cantidad de azúcar en la sangre en ratones diabéticos, lo que hace que los niveles de glucosa vuelvan a la normalidad.
Haga clic aquí para una imagen de alta resolución.
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Otros investigadores del estudio fueron Maryam Ahmadian, Eiji Yoshihara, Weiwei Fan, Yun-Qiang Yin, Ruth T. Yu y Annette R. Atkins del Instituto Salk de Estudios Biológicos; Weilin Liu, Johan W. Jonker, Theo van Dijk y Rick Havea de la Universidad de Groningen; Christopher Liddle de la Universidad de Sydney; Denise Lackey, Olivia Osborn y Jerrold M. Olefsky de la Universidad de California en San Diego; y Regina Goetz, Zhifeng Huang y Moosa Mohammadi de la Facultad de Medicina de la Universidad de Nueva York.
Ronald Evans es un Instituto Médico Howard Hughes investigador y también cuenta con el apoyo de subvenciones de la Los Institutos Nacionales de Salud, Leona M. y Harry B. Helmsley Charitable Trust, Fundación Glenn para la Investigación Médica, Ipsen/biomedida, CIRM, y Fundación Médica Ellison. Otros autores del estudio recibieron subvenciones de los Institutos Nacionales de Salud, el Consejo Nacional de Investigación Médica y de Salud de Australia, Consejo Europeo de Investigación, Programa de ciencias de la frontera humana, Organización Holandesa para la Investigación Científica, y Fundación Digestiva Holandesa.
Sobre el Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
REVISTA
Nature
AUTORES
Jae Myoung Suh, Maryam Ahmadian, Eiji Yoshihara, Weiwei Fan, Yun-Qiang Yin, Ruth T. Yu, Annette R. Atkins, Michael Downes y Ronald M. Evans del Instituto Salk de Estudios Biológicos; Weilin Liu, Johan W. Jonker, Theo van Dijk y Rick Havea de la Universidad de Groningen; Christopher Liddle de la Universidad de Sydney; Denise Lackey, Olivia Osborn y Jerrold M. Olefsky de la Universidad de California en San Diego; y Regina Goetz, Zifeng Huang y Moosa Mohammadi de la Facultad de Medicina de la Universidad de Nueva York
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu