
Enero 13, 2010
LA JOLLA, CA—Todos hemos experimentado en un momento u otro los signos típicos de una infección: fiebre, apatía, falta de apetito. Son orquestados por el cerebro en respuesta a las citocinas circulantes, las moléculas de señalización del sistema inmunitario. Pero cómo el alcance de las citoquinas se extiende más allá de la casi impenetrable barrera hematoencefálica ha sido tema de mucha controversia.
En su último estudio, los investigadores del Instituto Salk de Estudios Biológicos describen cómo, según la naturaleza del estímulo, los macrófagos residentes alineados a lo largo de la barrera hematoencefálica desempeñan papeles opuestos en la transmisión de señales inmunitarias al cerebro.
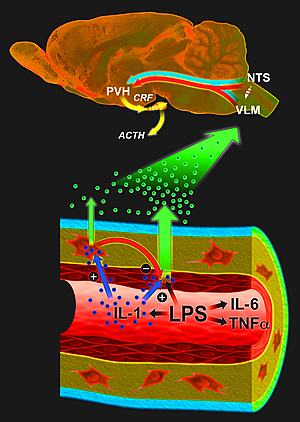
Las células endoteliales y los macrófagos trabajan juntos para transmitir y modular la fuerza de las señales inmunitarias inflamatorias al cerebro.
Imagen: Cortesía de Jamie Simon, Instituto Salk de Estudios Biológicos.
"Estos macrófagos actúan como aceleradores para conseguir la participación del cerebro en el tratamiento de los insultos inmunitarios, pero cuando es necesario, frenan de golpe para evitar que la respuesta inflamatoria central se desborde", explica el investigador postdoctoral Jordi Serrats, Ph.D., quien codirigió el estudio con Jennifer C. Schiltz, Ph.D., anteriormente investigadora postdoctoral en el Laboratorio de Función y Estructura Neuronal de Salk y ahora profesora asistente en la Universidad de Servicios Uniformados en Bethesda, Maryland.
Los hallazgos de los investigadores de Salk, que se publican en la edición del 14 de enero de 2010 de la revista Neurona, puede allanar el camino para nuevas terapias para quienes padecen enfermedades neurodegenerativas crónicas, como la esclerosis lateral amiotrófica (ELA), el Parkinson, el Alzheimer y las enfermedades priónicas, en las que los mecanismos inflamatorios centrales juegan un papel importante.
“El hecho de que hayamos identificado un potente mecanismo antiinflamatorio en el cerebro presenta un nuevo objetivo para intervenir en la amplia gama de enfermedades del sistema nervioso central que poseen un componente inflamatorio”, dice el autor principal del estudio, Pablo E. Sawchenko, Ph.D., profesor en el Laboratorio de Estructura y Función Neuronal.
En respuesta a una infección, se generan citocinas inflamatorias como la interleucina-1 en el sitio de la infección. Estas citocinas circulan en la sangre y se comunican con las neuronas del cerebro para activar el eje hipotálamo-pituitario-suprarrenal (HPA), una parte integral de la maquinaria de respuesta al estrés del cerebro. El eje HPA implica la interacción del hipotálamo, la glándula pituitaria, que se encuentra justo debajo del hipotálamo y las glándulas suprarrenales en la parte superior de los riñones.
Como un centro de comando central, el hipotálamo envía factor liberador de corticotropina, que estimula a la glándula pituitaria para que secrete la hormona adrenocorticotrópica. Este último le indica a las glándulas suprarrenales que aumenten la producción de glucocorticoides, que movilizan las reservas de energía para hacer frente a los insultos inflamatorios. Pero también actúan como inmunosupresores muy poderosos que previenen la producción excesiva de citocinas y la proliferación de células inmunitarias.
“Las citoquinas son moléculas grandes que no cruzan la barrera hematoencefálica libremente”, dice Sawchenko. "La cuestión de cómo estas moléculas acceden al cerebro para desencadenar toda esta serie de respuestas adaptativas, como fiebre, inactividad, somnolencia y activación de la maquinaria de respuesta al estrés del cerebro, ha sido un problema persistente en el lado de la neuroinmunología durante muchos años".
Investigaciones anteriores de Sawchenko y otros sugirieron una ruta vascular mediante la cual las citoquinas interactúan con las paredes de los vasos para generar mensajeros secundarios, que luego se involucran en los circuitos relevantes del cerebro. Las células endoteliales estrechamente empaquetadas, que recubren casi 400 millas de estrechos capilares en todo el cerebro, están perfectamente posicionadas para registrar las señales inmunitarias circulantes, pero requieren una señal muy fuerte para activarse. Los macrófagos perivasculares, por otro lado, son más sensibles pero no tienen acceso directo al torrente sanguíneo.
Para desentrañar el papel exacto de estos dos tipos de células, Serrats aprovechó la capacidad de los macrófagos para engullir e ingerir partículas sólidas. Inyectó liposomas que contenían clodronato, un fármaco que puede provocar la muerte celular, en el ventrículo cerebral lateral. Los liposomas fueron captados por los macrófagos, que fueron eliminados selectivamente.
Sin macrófagos perivasculares, los animales no pudieron responder a la interleucina-1 transmitida por la sangre e iniciar las llamadas respuestas de fase aguda del cerebro, que ayudan al cuerpo a enfrentar el desafío en cuestión, pero también causan la sensación familiar de "estar enfermo". Pero para su sorpresa, los investigadores de Salk descubrieron que las mismas células frenan las actividades proinflamatorias de las células endoteliales, que forman el revestimiento de los vasos sanguíneos y solo se ponen en acción, pero con mucha fuerza una vez que se encuentran, cuando se encuentran con lipopolisacárido, un componente clave de la pared celular de ciertas bacterias.
“Muchas enfermedades neurodegenerativas empeoran por inflamación o infecciones sistémicas”, dice Sawchenko. "Una vez que identificamos las moléculas que median la comunicación bidireccional entre los macrófagos perivasculares y las células endoteliales, podemos desarrollar estrategias para manejar las consecuencias adversas para la salud de las respuestas inflamatorias centrales".
Los investigadores que también contribuyeron al estudio incluyen a los investigadores postdoctorales Borja García-Bueno, Ph.D., y Teresa M. Reyes, Ph.D., en el Instituto Salk, así como a Nico van Rooijen, Ph.D., profesor en el Centro Médico Vrije Universiteit en Ámsterdam, Países Bajos.
El trabajo ha sido financiado en parte por la Fundación de Investigación Médica Clayton, los Institutos Nacionales de Salud, el Ministerio de Educación y Ciencia de España y CIBERsam.
Sobre el Instituto Salk de Estudios Biológicos:
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y las enfermedades infecciosas mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu