
17 de agosto de 2016
Los científicos de Salk revelan por qué las personas con el gen ApoE4 son más susceptibles a la enfermedad de Alzheimer
Los científicos de Salk revelan por qué las personas con el gen ApoE4 son más susceptibles a la enfermedad de Alzheimer
LA JOLLA—Durante décadas, los científicos han sabido que las personas con dos copias de un gen llamado apolipoproteína E4 (ApoE4) tienen muchas más probabilidades de tener La enfermedad de Alzheimer a los 65 años que el resto de la población. Ahora, los investigadores del Instituto Salk han identificado una nueva conexión entre la ApoE4 y la acumulación de proteínas asociada con el Alzheimer que proporciona una posible explicación bioquímica de cómo la ApoE4 adicional causa la enfermedad.
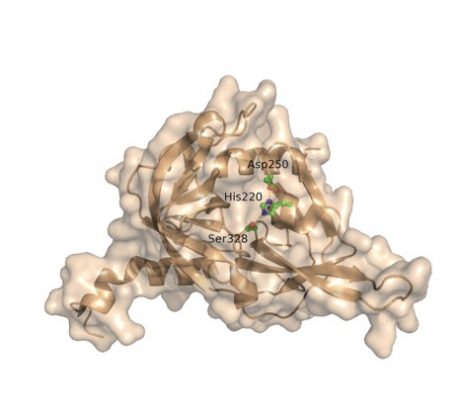
Haga clic aquí para una imagen de alta resolución.
Crédito: Instituto Salk
"El panorama general aquí es que hemos encontrado una forma muy diferente de pensar acerca de cómo se pueden regular las proteínas en la enfermedad de Alzheimer", dice Alan Saghatelian, profesor de Salk y titular de la Cátedra Dr. Frederik Paulsen en los Laboratorios de Biología de Péptidos de la Fundación Clayton de Salk. Sus hallazgos, que aparecen en la edición de agosto de 2016 de la Revista de la Sociedad Americana de Química, subrayan la importancia de observar genes y proteínas que no se asocian clásicamente con la enfermedad de Alzheimer para avanzar en la comprensión de la enfermedad.
La enfermedad de Alzheimer de inicio tardío, el subconjunto del trastorno que ocurre en personas de 65 años o más, afecta a más de 5 millones de estadounidenses y se caracteriza por pérdida progresiva de la memoria y demencia. Los científicos han presentado una variedad de hipótesis sobre sus causas, incluida la acumulación de grupos de proteínas llamados placas beta-amiloides y ovillos tau en el cerebro.
La apolipoproteína E viene en tres versiones o variantes, llamadas ApoE2, ApoE3 y ApoE4. Todas las proteínas ApoE tienen la misma función normal: transportar grasas, colesterol y vitaminas por todo el cuerpo, incluido el cerebro. Mientras que ApoE2 es protectora y ApoE3 parece no tener efecto, una mutación en ApoE4 es un factor de riesgo genético bien establecido para la enfermedad de Alzheimer de aparición tardía. Informes anteriores sugirieron que la ApoE4 podría afectar la forma en que el cerebro elimina la beta-amiloide, pero no estaba claro qué sucedía a nivel molecular.
"ApoE4 es el cambio genético más predictivo para el inicio tardío de la enfermedad de Alzheimer, pero nadie ha entendido realmente lo que sucede a nivel molecular", dice Saghatelian. Sin embargo, los científicos habían descubierto previamente indicios de que ApoE4 podría degradarse de manera diferente a las otras variantes, pero se desconocía la proteína que llevó a cabo esta descomposición de ApoE4.
Para encontrar la proteína responsable de la degradación de ApoE4, Saghatelian y el investigador asociado Qian Chu, primer autor del nuevo artículo, analizaron los tejidos en busca de posibles sospechosos y se concentraron en una enzima llamada serina peptidasa A1 (HtrA1) que requiere alta temperatura.
Cuando compararon cómo HtrA1 degradaba ApoE4 con ApoE3, encontraron que la enzima procesaba más ApoE4 que ApoE3, masticando ApoE4 en fragmentos más pequeños y menos estables. Los investigadores confirmaron la observación tanto en proteínas aisladas como en células humanas. El hallazgo sugiere que las personas con ApoE4 podrían tener menos ApoE en general en sus células cerebrales y más de los productos de descomposición de la proteína.

Haga clic aquí para una imagen de alta resolución
Crédito: Instituto Salk
“Ha habido una idea de que los productos de descomposición de ApoE4 podrían ser tóxicos”, dijo Saghatelian. "Ahora, conociendo la enzima que la descompone, tenemos una manera de probar esta idea".
Pero no es solo la falta de ApoE completa o un aumento en sus fragmentos lo que puede estar causando el Alzheimer en personas con ApoE4. Saghatelian y Chu también descubrieron que ApoE4, debido a que se une tan bien a HtrA1, evita que la enzima descomponga la proteína tau, responsable de los ovillos tau asociados con el Alzheimer.
"La gente ha pensado en tau o beta amiloide como cosas que causan la enfermedad de Alzheimer, pero esto sugiere que debemos pensar de manera más global sobre las proteínas que podrían afectar a tau o amiloide a través de vías bioquímicas", dijo Saghatelian.
Los resultados deben probarse y confirmarse en estudios con animales antes de que los investigadores puedan estar seguros de que HtrA1 es el vínculo entre ApoE4 y el Alzheimer en humanos. Pero si son ciertos, podrían apuntar hacia una mejor comprensión de la enfermedad y posibles nuevas estrategias de tratamiento.
Otros investigadores del estudio fueron Jolene K. Diedrich, Joan M. Vaughan, Cynthia J. Donaldson, Michael F. Nunn y Kuo-Fen Lee del Instituto Salk.
El trabajo y los investigadores involucrados fueron apoyados por subvenciones de la Los Institutos Nacionales de Salud, la Fundación Clayton, la Fundación Schlink, la Fundación de la Familia Gemcon, la Beca Hewitt, la Fundación Joe W. y Dorothy Dorsett Brown, la Cátedra Helen McLoraine de Neurobiología Molecular, el Centro Nacional del Cáncer y el Leona M. y Harry B. Helmsley Charitable Trust.
PERIODICO
Revista de la Sociedad Americana de Química
AUTORES
Qian Chu, Jolene K. Diedrich, Joan M. Vaughan, Cynthia J. Donaldson, Michael F. Nunn, Kuo-Fen Lee y Alan Saghatelian
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.