
7 de diciembre de 2015
El equipo de Salk identifica un fármaco que previene y revierte el daño hepático mortal en ratones
El equipo de Salk identifica un fármaco que previene y revierte el daño hepático mortal en ratones
LA JOLLA—El daño crónico al hígado eventualmente crea una herida que nunca sana. Esta afección, llamada fibrosis, reemplaza gradualmente las células hepáticas normales, que desintoxican los alimentos y los líquidos que consumimos, con más y más tejido cicatricial hasta que el órgano deja de funcionar.
Los científicos del Instituto Salk han identificado un fármaco que detiene esta acumulación descontrolada de tejido cicatricial en el hígado. La pequeña molécula, llamada JQ1, previno y revirtió la fibrosis en animales y podría ayudar a millones de personas en todo el mundo afectadas por fibrosis hepática y cirrosis, causadas por el alcoholismo y enfermedades como la hepatitis. Estos resultados fueron publicados en PNAS la semana del 7 de diciembre de 2015.
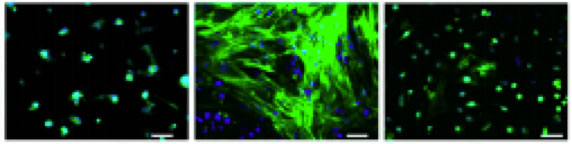
Crédito: Instituto Salk de Estudios Biológicos
“Después de demasiado daño en el hígado, el propio tejido cicatricial causa más tejido cicatricial”, dice ronald evans, profesor y director del Laboratorio de Expresión Génica de Salk e investigador del Instituto Médico Howard Hughes. "De hecho, podemos revertir la fibrosis hepática en animales y ahora estamos explorando posibles aplicaciones terapéuticas para humanos".
Cuando el hígado está dañado, se recurre a pequeñas acumulaciones de células estrelladas hepáticas que se especializan en almacenar vitamina A para atender la herida. Estas células estrelladas activadas arrojan su vitamina A, viajan al sitio de la lesión y crean tejido cicatricial grueso y fibroso para tapar y reparar el daño. Sin embargo, con el estrés prolongado de los órganos, las células sanas del hígado se reemplazan por tejido cicatricial, lo que finalmente conduce a la insuficiencia orgánica.
"Las terapias tradicionales dirigidas a la inflamación no funcionan porque estas células tienen múltiples formas de eludir el fármaco", dice Michael Downes, científico principal de Salk y autor del artículo. "Por el contrario, nuestra estrategia fue detener la respuesta fibrótica a nivel del genoma donde convergen estas vías".
La búsqueda de la ruta crítica del genoma dio en el blanco y descubrió una proteína reguladora, llamada BRD4, que es un regulador maestro de la fibrosis hepática.

Haga clic aquí para una imagen de alta resolución»
Imagen: Cortesía del Instituto Salk de Estudios Biológicos
Con este nuevo conocimiento en la mano, el equipo de Salk descubrió que JQ1 inhibió con éxito BRD4 y detuvo la transformación de las células estrelladas hepáticas en células productoras de fibra. Esta es una buena noticia, ya que JQ1 es un prototipo de una nueva clase de medicamentos que actualmente se están probando en ensayos clínicos en humanos para varios tipos de cáncer.
"JQ1 no solo protege contra la respuesta de la herida, sino que también invierte la respuesta fibrótica en ratones", dice Ruth Yu, investigadora del personal de Salk y una de las autoras del artículo.
"Nuestros resultados indican que BRD4 es un impulsor de la fibrosis crónica y un objetivo terapéutico prometedor para el tratamiento de la enfermedad hepática", dice Evans, quien también ocupa la cátedra de Biología Molecular y del Desarrollo de March of Dimes. “Creemos que este descubrimiento también puede tratar la fibrosis en otros órganos, como el pulmón, el páncreas y el riñón”.
Otros autores incluyen a Ning Ding, Nasun Hah, Mara Sherman, Chris Benner, Mathias Leblanc y Mingxiao He del Instituto Salk, y Christopher Liddle de la Universidad de Sydney.
El trabajo fue financiado por los NIH, las subvenciones para proyectos del Consejo Nacional de Investigación Médica y de Salud de Australia, Leona M. y Harry B. Helmsley Charitable Trust, la Fundación de Investigación del Cáncer Samuel Waxman e Ipsen/Biomeasure.
PERIODICO
PNAS
AUTORES
Ning Ding, Nasun Hah, Ruth T. Yu, Mara H. Sherman, Chris Benner, Mathias Leblanc, Mingxiao He, Christopher Liddle, Michael Downes y Ronald M. Evans
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu
Descubrir los secretos de la vida misma es la fuerza impulsora detrás del Instituto Salk. Nuestro equipo de científicos galardonados de clase mundial traspasa los límites del conocimiento en áreas como neurociencia, investigación del cáncer, envejecimiento, inmunobiología, biología vegetal, biología computacional y más. Fundado por Jonas Salk, desarrollador de la primera vacuna contra la polio segura y eficaz, el Instituto es una organización de investigación independiente y sin fines de lucro y un hito arquitectónico: pequeño por elección, íntimo por naturaleza y valiente ante cualquier desafío.