
5. Dezember 2016
Salk scientists discover a small protein important for cellular housekeeping
Salk scientists discover a small protein important for cellular housekeeping
LA JOLLA—We all know how hard it is to find something small like a dropped contact lens that blends into the background. It’s similarly tough for biologists to find tiny proteins against the complex background of the cell. But, increasingly, scientists are learning that such microproteins, which are overlooked by traditional detection methods, also have important biological roles to play.
Using a new microprotein detection strategy, Salk scientists discovered a human microprotein involved in one of the cells’ key housekeeping tasks: clearing out genetic material that’s no longer needed. The new molecule could provide a better understanding of how the levels of genes, including disease genes, are controlled in the cell.
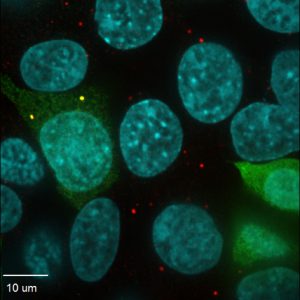
Klicken Sie hier für ein hochauflösendes Bild
Credit: MIT/Yale University
“Despite how much we know about the human genome, there are still blind spots in the genome discovery algorithms,” says Alan Saghatelian, Salk professor and one of the senior authors on the paper that appears in the December 5, 2016 issue of Nature Chemical Biology. “You can sequence the whole human genome and never know a protein, like this one, was there because it’s too short and falls below the usual length requirement for gene assignment algorithms.”
In cells, a gene’s DNA is transcribed into mRNA, which then guides production of specific proteins. After the necessary protein is created, the RNA blueprint is recycled to stop the production of the protein. While this process is crucial for healthy cells, no one was aware of a critical microprotein in this process, called NoBody (for non-annotated P-body dissociating polypeptide).
Saghatelian and Salk researcher Jiao Ma, with co-senior author Sarah Slavoff and first author Nadia D’Lima, both of Yale University, decided to study NoBody because its sequence is conserved throughout evolution, suggesting it had a critical function in human biology. Their experiments showed that NoBody interacts with proteins involved in the mRNA recycling process known to form P-body granules—clusters of mRNAs and proteins that perform the first step in breaking down the mRNAs. The team found that the introduction of NoBody into these cells caused the disappearance of these P-body granules and that changes to NoBody levels inside cells can disturb the RNA recycling pathway, highlighting a biochemical function for NoBody and potential target for future therapeutics related to RNA dysfunction.
Part of the reason this molecule has been overlooked for so long, according to Saghatelian, is that no one knew NoBody existed. In addition, no one looked for microproteins because it was unclear whether any microproteins would have important functions. “The discovery of NoBody and its function in mRNA recycling suggests that at least some of the hundreds of other microproteins that we have found might also be functional, which is an exciting proposition,” he says.
Slavoff adds, “The fact that NoBody has been present in this intensively studied complex of proteins all this time, but completely escaped our notice, really hammers home how many more currently unknown microproteins could be associated with essential cellular machineries.”

Klicken Sie hier für ein hochauflösendes Bild
Kredit: Salk Institut
To get around issues of detection and find out what small microproteins might be overlooked, the paper’s authors combined genomic sequencing and protein mass spectrometry (proteomics) to predict and identify non-annotated microproteins. The team began by isolating the contents of cells from the commonly studied myeloid leukemia cell line and removing the larger proteins to leave behind only the smaller ones. Then they used an analytical chemistry technique called liquid chromatography-mass spectroscopy proteomics to determine the amino acid sequences of every protein, including microproteins, that were present in the sample.
To figure out which genes these mapped to, the team used a homemade computational method to predict every possible microprotein from a myeloid cell’s total mRNA content, which they sequenced using genomics techniques. This custom database was then used to search their proteomics data for novel microproteins and led to the discovery of over 400 novel microproteins, including NoBody.
“We predict millions of theoretical protein sequences from the genomics data, but the key was to determine which of those predicted sequences are real using mass spectrometry data,” says Ma, who was the lead on this project in the Saghatelian lab.
The group thinks that NoBody might signal other important microproteins that might be involved in disease. Protein granules are found in many biological processes and are of particular relevance in neurological diseases, where proteins clump and aggregate together, such as in the amyloid plaques that are associated with Alzheimer’s disease.
“While NoBody is not directly involved in Alzheimer’s disease or other diseases, this discovery suggests that other microproteins might be,” adds Saghatelian, who is also holder of the Dr. Frederik Paulsen Chair. “The search for and characterization of these other microproteins in biology and disease represents an exciting frontier in molecular biology.”
Other authors on the paper included Qian Chu of the Salk Institute, Lauren Winkler of Yale University, Ken H. Loh of the Massachusetts Institute of Technology, Elizabeth O. Corpuz and Jens Lykke-Anderson of the Universität von Kalifornien, San Diego, and Bogdan A. Budnik of Harvard University.
The work was funded by a George E. Hewitt Foundation for Medical Research postdoctoral fellowship, the NIH, Die Leona M. und Harry B. Helmsley Charitable Trust grant, and Dr. Frederik Paulsen Chair/Ferring Pharmaceuticals.
JOURNAL
Nature Chemical Biology
AUTOREN
Nadia G. D’Lima, Jiao Ma, Lauren Winkler, Qian Chu, Ken H. Loh, Elizabeth O. Corpuz, Bogdan A. Budnik, Jens Lykke-Andersen, Alan Saghatelian, and Sarah A. Slavoff
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.