
20. September 2017
Salk-Wissenschaftler entdecken, dass ein Mikropeptid den Zellen hilft, den besten Weg zur Reparatur von Genen zu wählen und Krebs zu vermeiden
Salk-Wissenschaftler entdecken, dass ein Mikropeptid den Zellen hilft, den besten Weg zur Reparatur von Genen zu wählen und Krebs zu vermeiden
Klicken Sie hier für ein hochauflösendes Bild
Kredit: Salk Institut
LA JOLLA – Ist es besser, eine Aufgabe schnell zu erledigen und Fehler zu machen, oder sie langsam, aber perfekt zu erledigen? Wenn es darum geht, Brüche in der DNA zu reparieren, stehen Zellen vor der gleichen Wahl zwischen zwei Hauptreparaturwegen. Die Entscheidung ist wichtig, da die falsche Wahl noch mehr DNA-Schäden verursachen und zu Krebs führen könnte.
Wissenschaftler des Salk Institute haben herausgefunden, dass ein winziges Protein namens CYREN den Zellen hilft, zur richtigen Zeit den richtigen Weg zu wählen, und damit ein langjähriges Rätsel über DNA-Reparatur klärt und Forschern ein mächtiges Werkzeug bietet, das zu besseren Krebsbehandlungen führen könnte. Die Arbeit erscheint in Natur am 20. September 2017.
“Die Aufklärung von DNA-Reparaturwegen ist entscheidend für das Verständnis, wie sie manchmal toxisch sein können”, sagt Jan Karlseder, Professor am Labor für Molekulare und Zelluläre Biologie des Salk Institute und leitender Autor der neuen Arbeit. “Unsere Entdeckung der Funktion von CYREN erweitert nicht nur unser Wissen, sondern gibt uns auch ein neues Werkzeug, mit dem wir Krebs möglicherweise bekämpfen können.”

Klicken Sie hier für ein hochauflösendes Bild
Kredit: Salk Institut
Doppelstrangbrüche, die schwerwiegendsten Schäden, die an DNA auftreten können, können über einen von zwei Signalwegen repariert werden: einen schnellen, aber fehleranfälligen Prozess, der als NHEJ (nicht-homologes Endverknüpfen) bekannt ist, und einen langsameren, fehlerfreien Signalweg, der als HR (homologe Rekombination) bekannt ist. Der schnellere Signalweg verknüpft defekte Stränge effizient; im Falle mehrerer Brüche kann er jedoch falsche Enden miteinander verbinden, was für eine Zelle die Situation erheblich verschlimmert. Der langsamere Signalweg ist fehlerfrei, da er auf eine unbeschädigte DNA-Sequenz zur Anleitung der Reparatur angewiesen ist. Dies bedeutet jedoch, dass er nur dann eingesetzt werden kann, wenn eine Zelle ihre genetische Information zur Zellteilung kopiert hat. Angesichts dessen findet der schnelle Signalweg ausschließlich vor der DNA-Kopie statt, obwohl seine Maschinerie so effizient und produktiv ist, dass sich Wissenschaftler gefragt haben, warum diese nicht auch nach der Kopie den langsameren, genaueren Signalweg übertrifft. Wissenschaftler vermuten schon lange, dass etwas die schnellere Option in diesen Fällen zurückhalten muss.
Dieses Etwas, das die neue Arbeit enthüllt, ist ein Mikromanprotein namens CYREN, das den schnelleren Weg hemmt, wenn eine DNA-Kopie für den langsameren Weg verfügbar ist. CYREN wurde von einem anderen Salk-Wissenschaftler entdeckt., Alan Saghatelian, im Rahmen einer Initiative aus dem Jahr 2015 zur Identifizierung kleiner Proteine, sogenannter “short ORF-encoded peptides” oder SEPs, von denen zunehmend bekannt wird, dass sie entscheidende biologische Rollen spielen.
“Wir haben in unserer früheren Studie viele dieser Peptide gefunden, aber wir wussten nicht wirklich, ob sie wichtig waren, bis das Labor von Karlseder sich daran beteiligte,” sagt Saghatelian, Professor in den Clayton Foundation Laboratories for Peptide Biology und einer der Koautoren der Arbeit. “Dank dieser beeindruckenden neuen Arbeit wissen wir jetzt, dass sich unter den Hunderten, die wir entdecken, einige wirklich wichtige Moleküle befinden.”
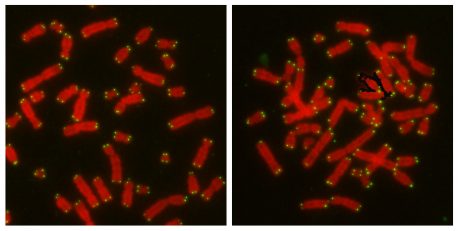
Saghatelians Forschung hatte darauf hingedeutet, dass CYREN mit dem Hauptschalter des schnelleren Signalwegs, einem Protein namens Ku, interagiert. Um die genaue Natur dieser Interaktion zu bestimmen, arbeitete Karlseders Team mit einer Region des Genoms, in der die Reparatur normalerweise unterdrückt wird, um gefährliche Fusionen zu verhindern: den Enden der Chromosomen, den sogenannten Telomeren. Forscher können Telomere künstlich stören, um den schnellen Signalweg zu aktivieren, und so ein Modellsystem schaffen, um die Auswirkungen von CYREN zu testen.

Klicken Sie hier für ein hochauflösendes Bild
Kredit: Salk Institut
“Telomere sind ein großartiges Forschungswerkzeug, da sie Reparaturen unbedingt unterdrücken müssen, aber es gibt Wege, die Reparaturmaschinerie zu aktivieren, so dass man sie sehr kontrolliert untersuchen kann”, sagt Nausica Arnoult, wissenschaftliche Mitarbeiterin am Salk Institute und Erstautorin der Arbeit. Dies tat das Salk-Team und stellte fest, dass in Anwesenheit von CYREN nach der Verdopplung der DNA keine Reparaturen erfolgten, was darauf hindeutet, dass es den Hauptschalter, Ku, ausschaltet. Ohne CYREN war der schnelle Weg von Ku sowohl vor als auch nach der DNA-Replikation aktiv.
Da die Telomer-Experimente dem Team nicht viel über den Wettstreit zwischen dem schnellen und dem langsamen Weg verrieten, nutzte Arnoult als Nächstes molekulare Werkzeuge, um die Reparatur in lebenden Zellen mit und ohne CYREN zu vergleichen. Sie kombinierte die DNA-Schere CRISPR mit Genen für fluoreszierende Proteine, die durch die Reparatur ausgelöst würden, sodass sie DNA auf spezifische Weise schneiden und anhand der entstehenden Farbe erkennen konnte, welcher Weg die Reparatur durchgeführt hatte. Außerdem analysierte sie alle Proteininteraktionen, die stattfanden.
Diese Experimente zeigten, dass CYREN direkt an Ku bindet, um den schnellen Weg zu hemmen, was sowohl vom Timing (vor oder nach der DNA-Kopie) als auch von der Art der DNA-Schädigung (z. B. glatt im Gegensatz zu gezackt) abhängt. Seine Aktivität kann sogar das Verhältnis von schnellen zu langsamen Reparaturen steuern.
“Unsere Studie zeigt, dass CYREN ein wichtiger Regulator der Wahl des DNA-Reparaturweges ist”, sagt Karlseder, der den Donald und Darlene Shiley Chair am Salk-Institut innehat. “Die Arbeit deutet auch auf die spannende Möglichkeit hin, DNA-Schäden in Krebszellen gezielt hervorzurufen und CYREN zu nutzen, um deren Reparatur zu verhindern.”
Weitere Autoren waren: Adriana Correia, Jiao Ma und Anna Merlo vom Salk; Sara Garcia-Gomez, Marija Maric und Simon J. Boulton vom Francis Crick Institut; Marco Tognetti von ETH Zürich; und Christopher W. Benner von Universität von Kalifornien, San Diego.
Die Arbeit wurde finanziert durch: das Human Frontiers Science Program, das Paul F. Glenn Center for Biology of Aging Research, ein Larry Hillblom Foundation Fellowship Grant, einen Wellcome Trust Senior Investigator Award, das Francis Crick Institute (Cancer Research UK), das UK Medical Research Council, das Wellcome Trust, die National Institutes of Health, das National Cancer Institute, den The Leona M. and Harry B. Helmsley Charitable Trust, den Dr. Frederick Paulsen Chair/Ferring Pharmaceuticals, einen Salk Institute Cancer Center Core Grant, den Donald and Darlene Shiley Chair, die Highland Street Foundation, die Fritz B. Burns Foundation und die Emerald Foundation.
JOURNAL
Natur
AUTOREN
Nausica Arnoult, Adriana Correia, Jiao Ma, Anna Merlo, Sara Garcia-Gomez, Marija Maric, Marco Tognetti, Christopher W. Benner, Simon J. Boulton, Alan Saghatelian und Jan Karlseder.
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.