
22. Juli 2024
Salk-Wissenschaftler entwickeln Methoden zur Untersuchung von Botenproteinen im Gehirn, sogenannten Neuropeptiden, und stellen fest, dass diese die Angstreaktion des Gehirns bei Mäusen steuern – eine Entdeckung, die bei der Entwicklung wirksamerer Schmerzmittel und Behandlungen für angstige Störungen wie PTBS und Angstzustände helfen könnte.
Salk-Wissenschaftler entwickeln Methoden zur Untersuchung von Botenproteinen im Gehirn, sogenannten Neuropeptiden, und stellen fest, dass diese die Angstreaktion des Gehirns bei Mäusen steuern – eine Entdeckung, die bei der Entwicklung wirksamerer Schmerzmittel und Behandlungen für angstige Störungen wie PTBS und Angstzustände helfen könnte.
LA JOLLA – In der Sekunde, in der Sie versehentlich den heißen Griff einer gusseisernen Pfanne berühren, übermannen Sie Schmerz und ein Gefühl der Gefahr. Sinneseindrücke wandern von den Schmerzrezeptoren in Ihrem Finger, durch Ihr Rückenmark und in Ihren Hirnstamm. Dort angekommen leitet eine spezielle Nervengruppe diese Schmerzsignale an einen höheren Gehirnbereich, die Amygdala, weiter, wo sie Ihre emotionale Angst auslösen und Ihnen helfen, sich zukünftig vor heißen Pfannen zu hüten.

Dieser Prozess der Umwandlung von Schmerz in eine Gefahrenerinnerung geschieht so schnell, dass Wissenschaftler lange glaubten, er müsse durch schnell wirkende Neurotransmitter vermittelt werden. Doch als Forscher des Salk-Instituts die Rolle größerer, langsamer wirkender Moleküle namens Neuropeptide untersuchten, entdeckten sie, dass diese die primären Botenstoffe in diesem Angstschaltkreis waren.
Neuropeptide spielen eine wichtige Rolle in der Gehirnkommunikation, aber die Details waren unklar, da den Wissenschaftlern nicht die richtigen Werkzeuge zur Verfügung standen, um sie bei sich verhaltenden Tieren zu untersuchen. Um die Rolle von Neuropeptiden in diesem Schaltkreis zu bestimmen, entwickelte das Salk-Team zwei neue Werkzeuge, die es Wissenschaftlern endlich ermöglichen, die Freisetzung von Neuropeptiden im Gehirn lebender Mäuse zu beobachten und zu manipulieren.
Die neue Studie, veröffentlicht in Zelle am 22. Juli 2024 enthüllte, dass der Schaltungsüberträger auf Neuropeptide als seine Hauptbotenstoffe und nicht auf schnelle Neurotransmitter angewiesen ist und mehr als ein Neuropeptid an dem Prozess beteiligt ist. Ihre Ergebnisse könnten zur Entwicklung wirksamerer Schmerzmittel oder neuer Behandlungen für angstbezogene Erkrankungen wie Angstzustände und PTBS (posttraumatische Belastungsstörung) führen.
“Es gibt noch so viel über Neuropeptide zu entdecken, aber glücklicherweise haben wir am Salk Institute das Erbe des Nobelpreisträgers Roger Guillemin’s Arbeit, um ihre Bedeutung hervorzuheben und unsere Entdeckungen zu fördern”, sagt der leitende Autor Sung Han, außerordentlicher Professor und Inhaber des Pioneer Fund Development Chair am Salk Institute. “Dazu haben wir zwei genetisch kodierte Werkzeuge zur Überwachung und Unterdrückung der Freisetzung von Neuropeptiden aus Nervenenden entwickelt. Wir glauben, dass diese neuen Werkzeuge die Neuropeptidforschung erheblich voranbringen werden, und unsere Entdeckung ihrer Rolle bei der Angstverarbeitung ist eigentlich erst der Anfang.”
Um Dinge in unserer Umgebung zu verarbeiten und darauf zu reagieren, müssen Informationen durch unseren Körper und unser Gehirn wandern. Diese Signale werden von Neuronen gesendet und empfangen, die organisierte Schaltkreise bilden, die die Informationen dorthin leiten, wo sie benötigt werden. Neuronen kommunizieren miteinander, indem sie Moleküle wie Neurotransmitter und Neuropeptide senden und empfangen.
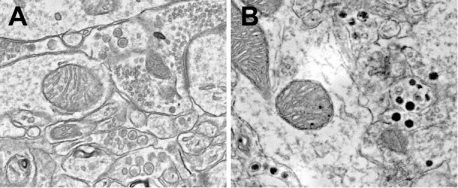
Neuropeptide werden allgemein als Neuromodulatoren anerkannt, die die Wirkung der Haupttransmitter unterstützen und modulieren. Frühe Pioniere wie Roger Guillemin schlugen jedoch vor, dass Neuropeptide selbst als Haupttransmitter fungieren können. Dieses Konzept wurde aufgrund fehlender Werkzeuge zur Visualisierung und Manipulation ihrer Freisetzung bei sich verhaltenden Tieren nicht rigoros getestet. Das Salk-Team machte sich daran, Neuropeptide zu erforschen, mit dem Ziel, neue Werkzeuge zu entwickeln, um ihre Rolle in Gehirnschaltkreisen besser zu verstehen.
Um gezielt Neuropeptide anzusteuern, nutzte Hans' Team eine ihrer einzigartigen Eigenschaften – während typische Neurotransmitter in kleinen Bläschen, den synaptischen Vesikeln, verpackt sind, sind Neuropeptide in große dichte Kernvesikel. Durch die Entwicklung biochemischer Werkzeuge, die auf diese großen Vesikel abzielen, entwickelten sie Werkzeuge zur Erfassung und Unterdrückung von Neuropeptiden. Die Sensoren markieren große, dicht-kernige Vesikel mit Proteinen, die leuchten, wenn sie aus dem Nervenende freigesetzt werden, wodurch die Forscher die Freisetzung von Neuropeptiden in Echtzeit beobachten können. Die Silencer bauen Neuropeptide spezifisch in großen, dicht-kernigen Vesikeln ab, wodurch enthüllt wird, was im Gehirn geschieht, wenn Neuropeptide fehlen.
"Wir haben eine neuartige Methode entwickelt, um die Wanderung und Funktion von Neuropeptiden im Gehirn lebender Tiere zu verfolgen”, sagt Dong-Il Kim, Erstautor der Studie und Postdoktorand in Hans Labor. “Diese Werkzeuge werden uns helfen, die Neuropeptid-Schaltkreise des Gehirns besser zu verstehen und Neurowissenschaftlern zu ermöglichen, Fragen zu erforschen, die bisher schwer zu beantworten waren.”
Mithilfe ihrer neu entwickelten Neuropeptid-Sensoren und -Silencer sowie bestehender Sensor- und Silencer-Werkzeuge für Glutamat (den häufigsten Neurotransmitter im Gehirn) untersuchten die Forscher, wie sich Neuropeptide und Glutamat bei lebenden Mäusen verhalten, wenn diese einem leichten Reiz ausgesetzt waren – gerade genug, um den Furchtkreis zu reizen. Sie stellten fest, dass während des Reizes Neuropeptide, aber kein Glutamat freigesetzt wurden. Darüber hinaus reduzierten Neuropeptid-Silencer die Angstverhaltensweisen bei den Mäusen, während die Silencer von Glutamat keine Wirkung hatten.
Zu Hans Überraschung und Freude nutzte dieser Hirnstamm-Angstschaltkreis Neuropeptide als seine primären Botenmoleküle und nicht Glutamat. Darüber hinaus unterstützen ihre Ergebnisse ihre laufenden Untersuchungen zu PACAP – ein Neuropeptid, das Panikstörungen moduliert.
“Diese neuen Werkzeuge und Entdeckungen sind ein wichtiger Schritt hin zu einer besseren Entwicklung neurowissenschaftlicher Medikamente”, sagt Han. “Wir fanden heraus, dass mehrere Neuropeptide zusammen in einer einzigen Vesikel verpackt und auf einmal durch einen schmerzhaften Reiz freigesetzt werden, um in diesem Angstkreislauf zu wirken, was uns zum Nachdenken brachte:‘Dies Das könnte der Grund sein, warum einige Medikamente, die nur auf ein Neuropeptid abzielen, in klinischen Studien scheitern. Mit diesen neuen Informationen können wir Erkenntnisse zur Entwicklung neuer Medikamente liefern, die mehrere Neuropeptidrezeptoren gleichzeitig ansprechen, was als bessere Schmerzmittel dienen oder bei der Behandlung angstbezogener Störungen wie PTBS helfen kann.’
Ausgestattet mit ihrem neuen Neuropeptid-Werkzeugkasten wird das Team bald andere Gehirnschaltkreise und -prozesse untersuchen. Zukünftige Erkenntnisse über die Neuropeptid-Signalübertragung in anderen Gehirnregionen sowie das neu gewonnene Verständnis, dass die gleichzeitige Beeinflussung mehrerer Neuropeptide notwendig ist, sollten die Entwicklung wirksamerer Medikamente zur Behandlung verschiedener neurologischer Störungen inspirieren.
Weitere Autoren sind Seahyung Park, Mao Ye, Sukjae Kang, Jinho Jhang, Joan Vaughan und Alan Saghatelian vom Salk Institute; Sekun Park, Jane Chen, Avery Hunker, Larry Zweifel und Richard Palmiter von der University of Washington; sowie Kathleen Caron von der University of North Carolina in Chapel Hill.
Die Arbeit wurde von den National Institutes of Health (NIMH 5R01MH116203, NINDS 1RF1NS128680) und dem Salk Institute unterstützt Innovationsförderung.
DOI: 10.1016/j.cell.2024.06.035
JOURNAL
Zelle
AUTOREN
Dong-Il Kim, Sekun Park, Seahyung Park, Mao Ye, Jane Y. Chen, Sukjae J. Kang, Jinho Jhang, Avery C. Hunker, Larry S. Zweifel, Kathleen M. Caron, Joan M. Vaughan, Alan Saghatelian, Richard D. Palmiter, Sung Han
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.