
25. Juni 2015
Das Salk Institute und das Sanford Burnham Prebys Medical Discovery Institute haben eine Verbindung entwickelt, die einen zellulären Recyclingprozess stoppt
Das Salk Institute und das Sanford Burnham Prebys Medical Discovery Institute haben eine Verbindung entwickelt, die einen zellulären Recyclingprozess stoppt
LA JOLLA – Mit dem Wachstum eines Tumors steigern dessen Krebszellen einen energieerfassenden Prozess, um ihre rasche Entwicklung zu unterstützen. Dieser Prozess, Autophagie genannt, wird normalerweise von einer Zelle zum Recycling beschädigter Organellen und Proteine genutzt, aber auch von Krebszellen zweckentfremdet, um ihren erhöhten Energie- und Stoffwechselbedarf zu decken.
Salk Institut und Sanford Burnham Prebys Medical Discovery Institute Wissenschaftler am SBP haben ein Medikament entwickelt, das das Einsetzen dieses Prozesses in Krebszellen verhindert. Veröffentlicht am 25. Juni 2015 in Molekulare Zelle, identifiziert die neue Studie ein niedermolekulares Medikament, das den ersten Schritt der Autophagie gezielt blockierte und damit die recycelten Nährstoffe, die Krebszellen zum Überleben benötigen, effektiv abschaltete.
“Der Fund eröffnet die Möglichkeit einer neuen Art und Weise, Krebs zu bekämpfen”, sagt Reuben Shaw, ein leitender Verfasser der Arbeit, Professor am Labor für Molekular- und Zellbiologie am Salk Institute und ein Howard Hughes Medical Institute Nachwuchswissenschaftler. “Die größte Nützlichkeit wird der Inhibitor wahrscheinlich in Kombination mit ziel gerichteten Therapien finden.”
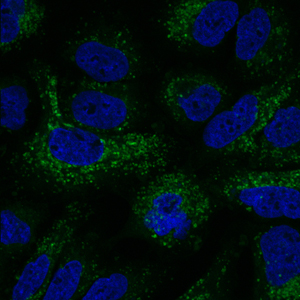
Zellrecycling (grün dargestellt) ist in Lungenkrebszellen, die mit einem etablierten Krebsmedikament behandelt wurden, erhöht. Das Recycling wird bei gleichzeitiger Behandlung mit einem neu entdeckten Enzymhemmer unterdrückt.
Klicken Sie hier für ein hochauflösendes Bild.
Bild: Mit freundlicher Genehmigung des Salk Institute for Biological Studies
Neben Krebs wurden Defekte in der Autophagie auch mit Infektionskrankheiten, Neurodegeneration und Herzerkrankungen in Verbindung gebracht. In einer Studie aus dem Jahr 2011 in der Fachzeitschrift Science entdeckten Shaw und sein Team, wie nährstoffarme Zellen das Schlüsselmolekül aktivieren, das die Autophagie auslöst, ein Enzym namens ULK1.
Da die Hemmung von ULK1 einige Krebsarten auslöschen könnte, indem sie eine Hauptenergieversorgung aus dem Recyclingprozess drosselt, wollte Shaws Gruppe und andere ein Medikament finden, das das Enzym hemmt. Nur ein Bruchteil solcher Inhibitoren, die im Reagenzglas vielversprechend sind, wirken letztendlich gut in lebenden Zellen. Shaws Gruppe verbrachte mehr als ein Jahr damit, die Funktionsweise von ULK1 zu untersuchen und neue Strategien zur Untersuchung seiner Funktion in Zellen zu entwickeln.
Ein wichtiger Durchbruch gelang, als Shaw den anderen leitenden Autor der Arbeit, Nicholas Cosford, Professor am NCI-Designierten Krebsforschungszentrum des SBP, traf. Cosford hatte ULK1 mittels medizinischer Chemie und chemischer Biologie untersucht und durch rationales Design einige vielversprechende Leitverbindungen identifiziert. Die beiden Labors bündelten ihre Anstrengungen, um Hunderte von potenziellen Molekülen auf deren Hemmung von ULK1 zu testen, die Liste auf einige Dutzend und schließlich auf ein Molekül zu reduzieren.
“Der Schlüssel zum Erfolg dieses Projekts lag in der Kombination von Reubens tiefem Verständnis der grundlegenden Biologie der Autophagie mit unserer chemischen Expertise”, sagt Cosford. “Dadurch konnten wir einen Wirkstoff finden, der ULK1 nicht nur im Reagenzglas, sondern auch in Tumorzellen gezielt bekämpfte. Eine weitere Herausforderung bestand darin, Moleküle zu finden, die das ULK1-Enzym selektiv angreifen, ohne gesunde Zellen zu beeinträchtigen. Unsere Arbeit bildet die Grundlage für einen neuartigen Wirkstoff, der resistente Krebsarten behandeln wird, indem er einen wichtigen Überlebensprozess der Tumorzellen unterbindet.”
Das Ergebnis war ein hochselektives Medikament namens SBI-0206965, das erfolgreich eine Reihe von Krebszelltypen abtötete, darunter menschliche und muride Lungenkrebszellen sowie menschliche Gehirnkrebszellen, von denen einige zuvor als besonders auf zelluläre Wiederverwertung angewiesen galten.
Interessanterweise aktivieren einige Krebsmedikamente (wie mTOR-Inhibitoren) die Zellrecycling weiter, indem sie die Fähigkeit der Zellen zur Aufnahme von Nährstoffen blockieren, wodurch diese stärker vom Recycling abhängig werden, um alle Bausteine zu erhalten, die die Zellen zum Überleben benötigen. Rapamycin beispielsweise wirkt, indem es das Zellwachstum und die Zellteilung stoppt. Als Reaktion darauf schalten die Zellen in den Recycling-Modus, indem sie ULK1 aktivieren, was möglicherweise ein Grund dafür ist, dass einige Krebszellen anstatt zu sterben in einen Ruhezustand verfallen und nach Beendigung der Behandlung – oft resistenter gegen Medikamente – wiederkehren.

Matthew Chun, Nicholas Cosford und Reuben Shaw
Klicken Sie hier für ein hochauflösendes Bild.
Bild: Mit freundlicher Genehmigung des Salk Institute for Biological Studies
“Die Hemmung von ULK1 würde diesen letzten Überlebensmechanismus der Krebszellen ausschalten und könnte bestehende Krebsbehandlungen wesentlich wirksamer machen”, sagt Matthew Chun, einer der Hauptautoren der Studie und Postdoktorand im Shaw-Labor am Salk.
In der Tat wurde die Kombination von SBI-0206965 mit mTOR-Inhibitoren wirksamer und tötete zwei- bis dreimal so viele Lungenkrebszellen wie SBI-0206965 allein oder die mTOR-Inhibitoren allein.
Die Autophagie-Signalwege zu manipulieren, um Krebs zu bekämpfen, wurde bereits versucht. Die einzigen Medikamente, die derzeit die Zellrecycling blockieren, zielen auf das Lysosom, ein Zellorganell, das im letzten Stadium der Autophagie wirkt. Obwohl diese lysosomalen Therapien in frühen klinischen Studien getestet werden, hemmen sie auch andere Lysosomenfunktionen, die über die Autophagie hinausgehen, und können daher zusätzliche Nebenwirkungen haben.
Im Vergleich äquivalenter Konzentrationen des lysosomalen Medikaments Chloroquin mit SBI-0206965, in Kombination mit mTOR-Inhibitoren, stellten die Wissenschaftler fest, dass SBI-0206965 Chloroquin bei der Abtötung von Krebszellen überlegen war.
Die Gruppe testet das Medikament jetzt in Mausmodellen für Krebs. “Ein wichtiger nächster Schritt wird sein, dieses Medikament bei anderen Krebsarten und in Kombination mit anderen Therapieansätzen zu testen”, sagt Shaw, stellvertretender Direktorin des NCI-Designierten Krebszentrums von Salk. “In der Zwischenzeit gibt diese Entdeckung den Forschenden ein spannendes neues Werkzeug für die Hemmung und Messung des Zellrecyclings an die Hand.”
Weitere Autoren der Studie sind der Co-Leitautor Daniel Egan vom Molecular and Cell Biology Laboratory des Salk Institute; Mitchell Vamos, Haixia Zou, Juan Rong, Dhanya Raveendra-Panickar, Douglas Sheffler und Peter Teriete vom Cell Death and Survival Networks Research Program im NCI-Designated Cancer Center des SBP; Chad Miller, Hua Jane Lou und Benjamin Turk von der Abteilung für Pharmakologie an der Yale University School of Medicine; John Asara von der Abteilung für Signaltransduktion am Beth Israel Deaconess Medical Center und der Abteilung für Medizin an der Harvard Medical School; sowie Chih-Cheng Yang vom Functional Genomics Core des SBP.
Die Forschung wurde unterstützt von Nationale Gesundheitsinstitute, der Verteidigungsministerium, und die Die gemeinnützige Stiftung von Leona M. und Harry B. Helmsley.
Über das Sanford Burnham Prebys Medical Discovery Institute:
Das Sanford Burnham Prebys Medical Discovery Institute (SBP) ist eine unabhängige gemeinnützige Forschungsorganisation, die hochmoderne Grundlagenforschung mit robuster Wirkstoffentdeckung verbindet, um ungedeckte klinische Bedürfnisse in den Bereichen Krebs, Neurowissenschaften, Immunität und Stoffwechselerkrankungen zu adressieren. Das Institut investiert in Talente, Technologie und Partnerschaften, um die Translation von Laborergebnissen zu beschleunigen, die die größte Auswirkung auf Patienten haben werden. Anerkannt für sein erstklassiges, vom NCI anerkanntes Krebsforschungszentrum und das Conrad Prebys Center for Chemical Genomics, beschäftigt SBP mehr als 1.100 Wissenschaftler und Mitarbeiter in San Diego (La Jolla), Kalifornien, und Orlando (Lake Nona), Florida. Weitere Informationen finden Sie unter SBPdiscovery.org. Das Institut ist auch auf Facebook unter facebook.com/SBPdiscovery und auf Twitter unter @SBPdiscovery zu finden.
JOURNAL
Molekulare Zelle
AUTOREN
Daniel F. Egan, Matthew G.H. Chun, Mitchell Vamos, Haixia Zou, Juan Rong, Chad J. Miller, Hua Jane Lou, Dhanya Raveendra-Panickar, Chih-Cheng Yang, Douglas J. Sheffler, Peter Teriete, John M. Asara, Benjamin E. Turk, Nicholas D. P. Cosford und Reuben J. Shaw
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.