
6. September 2019
Salk-Forschung erklärt, wie Pflanzen in der Lage sind, die Verbindungen, die sie zur Anpassung an Stress verwenden, effizient herzustellen
Salk-Forschung erklärt, wie Pflanzen in der Lage sind, die Verbindungen, die sie zur Anpassung an Stress verwenden, effizient herzustellen
LA JOLLA – Pflanzen können viele erstaunliche Dinge. Zu ihren Talenten gehört die Herstellung von Verbindungen, die ihnen helfen, Schädlinge abzuwehren, Bestäuber anzulocken, Infektionen zu heilen und sich vor extremen Temperaturen, Trockenheit und anderen Umwelteinflüssen zu schützen.
Forscher des Salk Institute, die untersuchen, wie Pflanzen die Fähigkeit zur Herstellung dieser natürlichen Chemikalien entwickelt haben, haben aufgedeckt, wie sich ein Enzym namens Chalconisomerase entwickelt hat, um Pflanzen die Herstellung von für ihr eigenes Überleben wichtigen Produkten zu ermöglichen. Die Forscher hoffen, dass dieses Wissen die Herstellung von Produkten beeinflussen wird, die für den Menschen von Vorteil sind, einschließlich Medikamenten und verbesserten Nutzpflanzen. Die Studie erschien in der Printversion von ACS Catalysis am 6. September 2019.
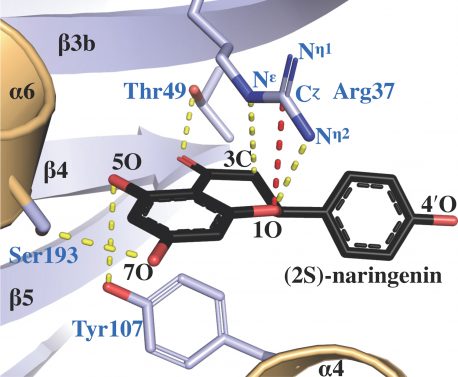
Klicken Sie hier für ein hochauflösendes Bild.
Quelle: Salk Institute/ACS Catalysis
“Seit dem Auftauchen der Landpflanzen auf der Erde vor etwa 450 Millionen Jahren haben sie ein ausgeklügeltes Stoffwechselsystem entwickelt, um Kohlendioxid aus der Atmosphäre in eine Vielzahl natürlicher Chemikalien in ihren Wurzeln, Sprossen und Samen umzuwandeln”, sagt der Salk-Professor. Joseph Noel, “Dies ist der Höhepunkt der Arbeit, die wir seit 20 Jahren in meinem Labor leisten, um die chemische Evolution von Pflanzen zu verstehen. Sie liefert uns detaillierte Erkenntnisse darüber, wie Pflanzen diese einzigartige Fähigkeit entwickelt haben, einige sehr ungewöhnliche, aber wichtige Moleküle herzustellen.”
Frühere Forschung im Noel-Labor untersuchte, wie sich diese Enzyme aus Nicht-Enzym-Proteinen entwickelten, einschließlich der Untersuchung primitiverer Versionen von ihnen, die in Organismen wie Bakterien und Pilzen vorkommen.
Als Enzym wirkt Chalconisomerase als Katalysator, um chemische Reaktionen in Pflanzen zu beschleunigen. Sie hilft auch dabei, sicherzustellen, dass die in der Pflanze hergestellten Chemikalien die richtige Form haben, da Moleküle mit der gleichen chemischen Formel zwei verschiedene, spiegelbildliche Variationen annehmen können (Isomere genannt).
“In der Pharmaindustrie ist es wichtig, dass die hergestellten Medikamente die richtige Version oder das richtige Isomer sind, da die Verwendung des falschen zu unbeabsichtigten Nebenwirkungen führen kann”, sagt Noel, Direktor des Salk’s Jack H. Skirball Center for Chemical Biology and Proteomics und Inhaber des Arthur and Julie Woodrow Chair. “Indem wir untersuchen, wie Chalcon-Isomerase funktioniert, können wir mehr darüber lernen, wie die Herstellung der richtigen Isomere von Pharmazeutika und anderen Produkten, die für die menschliche Gesundheit wichtig sein können, beschleunigt werden kann.”
In der vorliegenden Studie nutzten die Forscher verschiedene strukturbiologische Techniken, um die einzigartige Form des Enzyms und seine Formveränderungen bei der Interaktion mit anderen Molekülen zu untersuchen. Sie identifizierten den Teil der Struktur der Chalconisomerase, der es ihr ermöglichte, Reaktionen unglaublich schnell zu katalysieren und gleichzeitig sicherzustellen, dass sie das richtige, biologisch aktive Isomer bildet. Diese Reaktionen führen zu einer Vielzahl von Aktivitäten in Pflanzen, einschließlich der Umwandlung von primären Metaboliten wie Phenylalanin und Tyrosin in wichtige spezialisierte Moleküle, die Flavonoide genannt werden.
Es stellte sich heraus, dass eine bestimmte Aminosäure, Arginin, die eine von vielen miteinander verbundenen Aminosäuren in der Chalconisomerase war, in einer durch Evolution geformten Position saß, die es ihr ermöglichte, eine Schlüsselrolle bei der Katalyse von Chalconisomerase-Reaktionen zu spielen.

Klicken Sie hier für ein hochauflösendes Bild.
Kredit: Salk Institut
“Durch strukturelle Studien und Computermodellierung konnten wir die sehr präzisen Positionen von Arginin im aktiven Zentrum des Enzyms während der Reaktion sehen”, sagt der Erstautor Jason Burke, ein ehemaliger Postdoktorand in Noels Labor, der jetzt Assistenzprofessor an der California State University San Bernardino ist. “Ohne dieses Arginin funktioniert es nicht auf die gleiche Weise.”
Burke fügt hinzu, dass diese Art von Katalysator von organischen Chemikern lange gesucht wurde. “Dies ist ein Beispiel dafür, wie die Natur bereits ein Problem gelöst hat, mit dem sich Chemiker seit langem beschäftigen”, fügt er hinzu.
“Durch das Verständnis der Chalconisomerase können wir einen neuen Werkzeugkasten schaffen, den Chemiker für die von ihnen untersuchten Reaktionen nutzen können”, sagt Noel. “Es ist absolut unerlässlich, diese Art von Grundlagenwissen zu haben, um molekulare Systeme entwerfen zu können, die eine bestimmte Aufgabe erfüllen können, selbst in der nächsten Generation von nährstoffreichen Nutzpflanzen, die in der Lage sind, das Treibhausgas Kohlendioxid in für das Leben essentielle Moleküle umzuwandeln.”
Weitere Forscher der Publikation waren James La Clair, Ryan Philippe, Joseph Jez, Marianne Bowman, Gordon Louie und Katherine Woods vom Salk Institute; Anna Pabis, Marina Corbella und Shina Kamerlin von der Universität Uppsala in Schweden; George Cortina von der University of Virginia; Miriam Kaltenbach und Dan Tawfik vom Weizmann Institute of Science in Israel; und Andrew Nelson von der University of Texas in Austin.
Diese Arbeit wurde auch durch das Howard Hughes Medical Institute, die US National Science Foundation Grant EEC-0813570, die Wenner-Gren Foundations, den European Research Council ERC Grant Agreement 30647 und ein Wallenberg Academy Fellowship der Knut und Alice Wallenberg Foundation unterstützt. Das schwedische nationale Infrastrukturzentrum für Computerwissenschaft stellte die Rechenzeit für die in dieser Studie durchgeführten Simulationen zur Verfügung.
DOI: 10.1021/acscatal.9b01926
JOURNAL
ACS Catalysis
AUTOREN
Jason R. Burke, James J. La Clair, Ryan N. Philippe, Anna Pabis, Marina Corbella, Joseph M. Jez, George A. Cortina, Miriam Kaltenbach, Marianne E. Bowman, Gordon V. Louie, Katherine B. Woods, Andrew T. Nelson, Dan S. Tawfik, Shina C.L. Kamerlin und Joseph P. Noel
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.