
13. Februar 2009
LA Jolla, Kalifornien – Fruchtfliegen und Menschen teilen die meisten ihrer Gene, einschließlich 70 Prozent aller bekannten menschlichen Krankheitsgene. Unter Ausnutzung dieser bemerkenswerten evolutionären Konservierung haben Forscher am Salk Institute for Biological Studies die Fruchtfliege zu einem Labormodell für eine innovative Studie über Gliome, die häufigsten bösartigen Hirntumore, umfunktioniert.
"Gliome sind eine verheerende Krankheit, aber wir wissen immer noch sehr wenig über den zugrundeliegenden Krankheitsprozess", erklärt John B. Thomas, Ph.D., ein Professor im Molekularen Neurobiologielabor und leitender Autor der Studie, die in der aktuellen Ausgabe der Public Library of Science Genetik. "Wir können nun die Macht von Drosophila Genetik zur Aufdeckung von Genen, die diese Tumore antreiben, und zur Identifizierung neuartiger therapeutischer Ziele, was die Entwicklung wirksamer Medikamente beschleunigen wird."
Bessere Modelle für die Forschung an menschlichen Gliomen werden dringend benötigt. Allein im letzten Jahr wurden in diesem Land bei rund 21.000 Menschen Krebsarten des Gehirns und des Nervensystems diagnostiziert, darunter der bekannteste, Senator Edward M. Kennedy. Etwa 77 Prozent der bösartigen Hirntumore sind Gliome und ihre Prognose ist in der Regel düster. Während sie sich selten auf andere Körperteile ausbreiten, infiltrieren Krebszellen aus Gliazellen schnell das Gehirn und wachsen rasant, was sie selbst mit aktuellen Therapien weitgehend unheilbar macht.
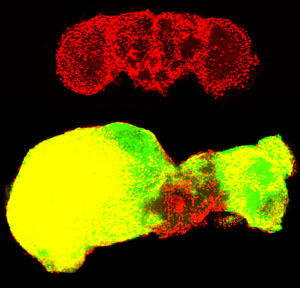
Oben: Normales Fliegengehirn zum Vergleich. Gliazellen sind rot dargestellt. Unten: Tumorzellen (grün dargestellt) haben fast das gesamte Gehirn einer erwachsenen Fliege überwuchert.
Bild: Mit freundlicher Genehmigung von Dr. Renee Read, Salk Institute for Biological Studies
Gliome entstehen aus Gehirnzellen, die als "Gliazellen" bezeichnet werden, und werden je nach Aggressivität in Subtypen eingeteilt, wobei das Glioblastom die häufigste und aggressivste Form von Gliomen ist. Ihre Vielfalt spiegelt sich in der Anzahl der verschiedenen Signalwege wider, die an der Entstehung dieser Tumore beteiligt sind. Aggressive Gliome scheinen jedoch alle eine Gemeinsamkeit zu haben: Die meisten, wenn nicht alle menschlichen Glioblastome weisen Mutationen auf, die die Signalwege EGFR-Ras und PI-3K aktivieren. Es wird angenommen, dass solche Mutationen auch eine Schlüsselrolle bei der Entwicklung von Medikamentenresistenzen spielen.
"Fruchtfliegen besitzen Homologe vieler relevanter menschlicher Gene, darunter EGFR, Ras und PI-3K", erklärt die Postdoktorandin und Erstautorin Renee Read, die das Projekt leitete. "Wir entwickelten die Drosophila Modell zur Ermittlung, wie diese Gene spezifisch die Pathogenese von Hirntumoren regulieren und zur Entdeckung neuer Wege, diese Tumore zu bekämpfen."
Als Read beide Signalwege gezielt in Gliazellen gentechnisch veränderter Fruchtfliegen aktivierte, stellte sie fest, dass, genau wie im Gehirn von Säugetieren, die Aktivierung der EGFR-Ras- und PI-3K-Signalwege zu sich schnell teilenden, invasiven Zellen führte, die tumorähnliche Wucherungen im Gehirn der Fliege hervorbrachten und die menschliche Krankheit nachahmten.
"Sobald ich verifiziert hatte, dass die Fliegen-Tumore wichtige Aspekte mit menschlichen Gliomen teilen, konnte ich das Modell verwenden, um nach neuen Genen zu suchen, die am Krankheitsverlauf beteiligt sind, und sie mit den Genen vergleichen, die im Rahmen der Glioblastom-Initiative des Cancer Genome Atlas gefunden wurden', erklärt Read.
Glioblastom ist eines der ersten Tumoren, das vom Forschungsnetzwerk The Cancer Genome Atlas untersucht wurde. Dessen Ziel ist es, das Verständnis der molekularen Grundlagen von Krebs durch den Einsatz moderner Genomcharakterisierungstechnologien wie der groß angelegten Genomsequenzierung zu beschleunigen.
Wie die meisten Krebsarten entstehen Gliome durch Veränderungen in der DNA einer Person, die sich im Laufe des Lebens ansammeln, aber es war eine Herausforderung, die Veränderungen mit weitreichenden Auswirkungen von unschuldigen Mitläufern zu trennen. "Während diese Initiativen uns große Listen veränderter Gene liefern, sagen sie uns nicht viel darüber, welche davon wirklich wichtig sind", sagt Read. "Die Beantwortung dieser Frage in Mausmodellen oder Patientenstudien ist extrem teuer und zeitaufwendig. Bei Fliegen kann ich jede Woche Hunderte von Genen testen."
Die Forscher des Salk-Instituts nutzen nun ihr Fliegenmodell, um nach Genen und Medikamenten zu suchen, die EGFR/PI-3K-assoziierte Hirntumore blockieren könnten. Die Medikamententests werden in Zusammenarbeit mit den Co-Autoren Professor Webster Cavenee, Ph.D., und Juniorprofessor Frank Furnari, Ph.D., durchgeführt, beides Experten für menschliche Hirntumorbiologie am Ludwig-Institut für Krebsforschung der University of California, San Diego.
Die Forscher hoffen, dass durch ihre gemeinsamen Anstrengungen neue Erkenntnisse aus dem Fliegenmodell schnell in Studien zu Hirntumoren bei Mäusen und Menschen übertragen werden können und zur Entwicklung neuer Therapien für diese tödliche Krebsart führen.
Die Arbeit wurde durch die National Institutes for Neurological Disorders and Stroke und die American Brain Tumor Association unterstützt.
Für Informationen zur Kommerzialisierung dieser Technologie wenden Sie sich bitte an das Salk Office of Technology Development unter (858) 453-4100, Durchwahl 1278.
Das Salk Institute for Biological Studies in La Jolla, Kalifornien, ist eine unabhängige gemeinnützige Organisation, die sich grundlegenden Entdeckungen in den Biowissenschaften, der Verbesserung der menschlichen Gesundheit und der Ausbildung zukünftiger Forschergenerationen widmet. Jonas Salk, M.D., dessen Polioimpfstoff die lähmende Krankheit poliomyelitis im Jahr 1955 fast ausrottete, eröffnete das Institut 1965 mit einem Grundstücksgeschenk der Stadt San Diego und der finanziellen Unterstützung der March of Dimes.
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu