
20. Dezember 2016
Salk-Wissenschaftler finden 3D-“Mini-Gehirne” liefern neue Einblicke in Entwicklung und potenzielle Krankheitsbehandlungen
Salk-Wissenschaftler finden 3D-“Mini-Gehirne” liefern neue Einblicke in Entwicklung und potenzielle Krankheitsbehandlungen
LA JOLLA – Wenn man Modelle baut, sei es von Schiffen oder Autos, möchte man, dass sie möglichst echt wirken. Diese Qualität ist für den Bau von Modellorganen sogar noch wichtiger, da Krankheitsbehandlungen, die auf diesen Modellen entwickelt werden, für den Menschen sicher und wirksam sein müssen. Nun haben Wissenschaftler des Salk Institute ein 3D-“Minigehirn” untersucht, das aus menschlichen Stammzellen gezüchtet wurde, und festgestellt, dass es dem realen Gehirn strukturell und funktionell ähnlicher ist als die weit verbreiteten 2D-Modelle. Die Entdeckung, die in der Ausgabe vom 20. Dezember 2016 veröffentlicht wurde, Cell Reports, weist darauf hin, dass das neue Modell Wissenschaftlern helfen könnte, die Gehirnentwicklung sowie neurologische Krankheiten wie Alzheimer oder Schizophrenie besser zu verstehen.
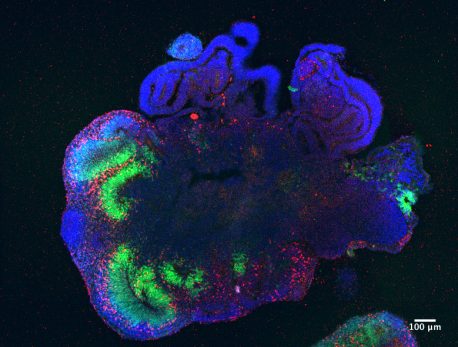
Klicken Sie hier für ein hochauflösendes Bild
Quelle: Madeline Lancaster/MRC-LMB (Medical Research Council, Laboratory of Molecular Biology), Großbritannien
“Die Möglichkeit, menschliche Gehirnzellen als dreidimensionale Miniaturorgane züchten zu können, war ein echter Durchbruch”, sagt der leitende Autor Joseph Ecker, der ein Investigator des Howard Hughes Medical Institute sowie Professor und Direktor des Genomic Analysis Laboratory am Salk Institute ist. “Nachdem wir nun ein strukturell realistisches Modell haben, können wir damit beginnen zu untersuchen, ob es auch funktional realistisch ist, indem wir uns seine genetischen und epigenetischen Merkmale ansehen.”
Seit Jahren veranlassen Zellbiologen embryonale Stammzellen in Petrischalen chemisch dazu, sich in verschiedene Arten von Gehirnzellen zu entwickeln (“differenzieren”). Während Forscher in der Lage sind, eine Fülle von Informationen aus diesen einzelnen Zellschichten zu gewinnen, liegt die offensichtliche Einschränkung darin, dass echtes Gehirngewebe nicht zweidimensional ist. Im Jahr 2013 entwickelten europäische Forscher eine Methode, um embryonale Gehirnzellen in 3D-Gelen zu züchten, wo sie beginnen, sich wie ein echtes Gehirn in realistische Schichten zu differenzieren. Bislang war jedoch nicht bekannt, wie genau diese im Labor gezüchteten Mini-Gehirne, sogenannte zerebrale Organoide (COs), echten Gehirnen ähneln und sich verhalten.
In Zusammenarbeit mit dem europäischen Labor, das das Protokoll für das Wachstum von COs entwickelt hat, verglich Eckers Labor COs in frühen Phasen der Gehirnentwicklung mit echtem Gehirngewebe im gleichen Entwicklungsstadium.
“Unsere Arbeit zeigt in bemerkenswertem Maße, wie die menschliche Gehirnentwicklung in einer Schale in zerebralen Organoiden wiederholt werden kann“, sagt Juergen Knoblich, Co-Seniorautor der neuen Arbeit und Leiter des europäischen Labors.
Um COs für die Analyse zu erstellen, verwendeten die Teams eine menschliche embryonale Zelllinie namens H9 und fügten die richtigen Chemikalien hinzu, um die Zellen 60 Tage lang auf einen neuroentwicklungsbezogenen Weg zu lenken. Anschließend analysierten sie die Epigenetik der COs, das Muster chemischer Markierungen auf der DNA, die für die Aktivierung oder Unterdrückung von Genen verantwortlich ist. Die Epigenome von Zellen – die von Umweltfaktoren wie Ernährung oder Stress beeinflusst werden – werden zunehmend mit Entwicklung und Krankheiten (wie Schizophrenie) in Verbindung gebracht.

Klicken Sie hier für ein hochauflösendes Bild
Kredit: Salk Institut
“Bisher hat noch niemand eine Epigenom-Sequenzierung für zerebrale Organoide durchgeführt”, sagt Chongyuan Luo, wissenschaftlicher Mitarbeiter am Salk Institute und Erstautor der Studie. “Diese Art der Bewertung ist so wichtig für das Verständnis der Gehirnentwicklung, insbesondere wenn wir diese Gewebe eines Tages für neurologische Therapien einsetzen werden.”
Das Team verglich seine Ergebnisse sowohl mit altersentsprechendem Echtgewebe aus der NeuroBioBank der National Institutes of Health als auch mit 2D-Gehirnmodelldaten anderer Forscher. Sie stellten fest, dass COs in Bezug auf den Differenzierungsgrad der Zellen und ihre Genexpression echten Gehirngeweben viel ähnlicher waren als 2D-Modelle; mit anderen Worten, COs entwickeln sich entlang sehr ähnlicher früher Entwicklungszeitpläne wie echte Gehirne, obwohl sie nicht das gleiche Reifegrad erreichen.
Wenn es jedoch um Epigenetik ging, zeigten sowohl 3D- als auch 2D-Modelle ähnliche abweichende Muster, die allen in Kultur gezüchteten Zellen im Gegensatz zu denen im Gehirn gemeinsam zu sein scheinen. Was dieser Unterschied bedeutet, ist nicht ganz klar, aber da er so auffällig ist, schlägt Ecker vor, dass er ein nützliches Maß dafür sein könnte, wie ähnlich ein Modell dem realen Gehirn ist.
“Unsere Ergebnisse zeigen, dass zerebrale Organoide als 3D-Modell der Gehirnfunktion einem echten Gehirn näher kommen als 2D-Modelle, sodass wir durch die Verwendung des epigenetischen Musters als Messgröße vielleicht noch näher herankommen”, sagt Ecker, der auch den Salk International Council Chair in Genetics innehat.
Weitere Autoren waren: Rosa Castanon und Joseph R. Nery vom Salk Institute sowie Madeline A. Lancaster vom Institut für Molekulare Biotechnologie der Österreichische Akademie der Wissenschaften.
Die Arbeit wurde finanziert durch die Howard Hughes Medical Institute, der Gordon und Betty Moore Stiftung, die Österreichische Akademie der Wissenschaften, die Österreichischer Wissenschaftsfonds, der Europäischer Forschungsrat, ein Marie-Curie-Postdoc-Stipendium und das Medical Research Council.
JOURNAL
Cell Reports
AUTOREN
Chongyuan Luo, Madeline A. Lancaster, Rosa Castanon, Joseph R. Nery, Juergen A. Knoblich und Joseph R. Ecker
Büro für Kommunikation
Telefon: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Die Aufgabe des Instituts besteht darin, grundlegende, kooperative und risikofreudige Forschung voranzutreiben, die sich mit den dringendsten Herausforderungen der Gesellschaft befasst, darunter Krebs, Alzheimer und die Gefährdung der Landwirtschaft. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und führt zu Erkenntnissen, die neue Medikamente und Innovationen weltweit ermöglichen.