
6. April 2016
Salk-Wissenschaftler zeigen, wie Immunrezeptoren tote und dysfunktionale Gehirnzellen beseitigen und wie sie als Ziele für die Behandlung neurodegenerativer Erkrankungen dienen könnten
Salk-Wissenschaftler zeigen, wie Immunrezeptoren tote und dysfunktionale Gehirnzellen beseitigen und wie sie als Ziele für die Behandlung neurodegenerativer Erkrankungen dienen könnten
LA JOLLA – Im Jugendalter enthält Ihr Gehirn bereits die meisten Neuronen, die Sie für den Rest Ihres Lebens haben werden. In einigen Regionen wachsen jedoch weiterhin neue Nervenzellen – und sie benötigen die Dienste zellulärer Wächter, spezialisierter Immunzellen, die das Gehirn schützen, indem sie tote oder funktionsgestörte Zellen entfernen.
Nun haben Salk-Wissenschaftler das überraschende Ausmaß entdeckt, in dem sowohl sterbende als auch tote Neuronen beseitigt werden, und spezifische zelluläre Schalter identifiziert, die für diesen Prozess von entscheidender Bedeutung sind. Die Arbeit wurde detailliert beschrieben Natur April 6, 2016.
„Wir haben herausgefunden, dass Rezeptoren auf Immunzellen im Gehirn sowohl für gesunde als auch für verletzte Zustände lebenswichtig sind“, sagt er Greg Lemke, leitender Autor der Arbeit, Salk-Professor für molekulare Neurobiologie und Inhaber des Françoise Gilot-Salk-Lehrstuhls. „Diese Rezeptoren könnten potenzielle therapeutische Ziele für neurodegenerative Erkrankungen oder entzündungsbedingte Erkrankungen sein, wie z Parkinson-Krankheit"
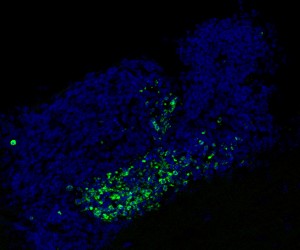
Zu den offenen Stellen für ein hochauflösendes Bild
Bildnachweis: Salk Institute
Vor zwei Jahrzehnten entdeckte das Lemke-Labor, dass Immunzellen kritische Moleküle namens TAM-Rezeptoren exprimieren, die seitdem in vielen Labors zu einem Schwerpunkt der Autoimmun- und Krebsforschung geworden sind. Zwei der TAM-Rezeptoren, Mer und Axl genannt, helfen Immunzellen, sogenannten Makrophagen, als Müllsammler zu fungieren und die über 100 Milliarden toten Zellen, die täglich im menschlichen Körper entstehen, zu identifizieren und zu verbrauchen.
Für die aktuelle Studie fragte das Team, ob Mer und Axl im Gehirn die gleiche Aufgabe erfüllen. Spezialisierte Makrophagen des Zentralnervensystems, sogenannte Mikroglia, machen etwa 10 Prozent der Zellen im Gehirn aus, wo sie Krankheitserreger erkennen, darauf reagieren und sie zerstören. Die Forscher entfernten Axl und Mer in der Mikroglia ansonsten gesunder Mäuse. Zu ihrer Überraschung stellten sie fest, dass das Fehlen der beiden Rezeptoren zu einer großen Ansammlung abgestorbener Zellen führte, jedoch nicht überall im Gehirn. Zellkadaver wurden nur in den kleinen Regionen gesehen, in denen die Produktion neuer Neuronen – Neurogenese – beobachtet wird.
Viele Zellen sterben normalerweise während der Neurogenese im Erwachsenenalter ab, werden jedoch sofort von Mikroglia gefressen. „Es ist sehr schwierig, auch nur eine einzige tote Zelle in einem normalen Gehirn zu entdecken, weil sie von Mikroglia so effizient erkannt und beseitigt wird“, sagt Paqui G. Través, Mitautor der Arbeit und ehemaliger wissenschaftlicher Mitarbeiter von Salk. „Aber in den neurogenen Regionen von Mäusen, denen Mer und Axl fehlen, haben wir viele solcher Zellen entdeckt.“
Als die Forscher diesen Prozess genauer untersuchten, indem sie die neu wachsenden Neuronen in den Mikroglia von Mäusen markierten, denen Mer und Axl fehlten, bemerkten sie noch etwas anderes Interessantes. Neue Neuronen, die zum Riechkolben oder Geruchszentrum wandern, nahmen ohne Axl und Mer dramatisch zu. Mäuse, denen die TAM-Rezeptoren fehlten, hatten im Vergleich zu normalen Mäusen eine um 70 Prozent höhere Zahl neu gebildeter Zellen im Riechkolben.
Wie – und in welchem Ausmaß – dieses unkontrollierte neue Nervenwachstum den Geruchssinn einer Maus beeinflusst, ist laut Lemke noch nicht bekannt, obwohl das Labor diesen Bereich erforschen wird. Aber die Tatsache, dass so viel mehr lebende Nervenzellen in Abwesenheit der Rezeptoren in den Riechkolben wandern konnten, legt nahe, dass Mer und Axl neben der Beseitigung toter Zellen noch eine andere Rolle spielen – sie könnten tatsächlich auch lebende, aber funktionell beeinträchtigte Zellen angreifen .

Zu den offenen Stellen für ein hochauflösendes Bild
Bildnachweis: Salk Institute
„Es scheint, dass ein erheblicher Teil des Zelltods in neurogenen Regionen nicht auf den intrinsischen Zelltod zurückzuführen ist, sondern vielmehr auf die Mikroglia selbst zurückzuführen ist, die einen Teil der Zellen durch Verschlingung abtötet“, sagt Lemke. „Mit anderen Worten, einige dieser neugeborenen Neuronen-Vorläufer werden tatsächlich lebendig gefressen.“
Für ein gesundes Gehirn sei das nicht unbedingt etwas Schlechtes, fügt Lemke hinzu. Das Gehirn produziert mehr Neuronen, als es nutzen kann, und schneidet dann die nicht benötigten Zellen zurück. Bei einem entzündeten oder erkrankten Gehirn kann die Zerstörung lebender Zellen jedoch nach hinten losgehen.
Das Lemke-Labor führte eine weitere Versuchsreihe durch, um die Rolle von TAM-Rezeptoren bei Krankheiten zu verstehen: Sie untersuchten die Aktivität von Axl und Mer in einem Mausmodell der Parkinson-Krankheit. Dieses Modell produziert ein menschliches Protein, das in einer vererbten Form der Krankheit vorkommt und zu einer langsamen Degeneration des Gehirns führt. Das Team stellte fest, dass Axl in dieser Situation weitaus aktiver war, was mit anderen Studien übereinstimmt, die zeigten, dass ein erhöhter Axl ein zuverlässiger Indikator für Entzündungen im Gewebe ist.
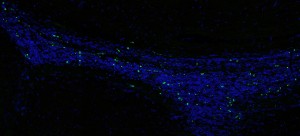
Zu den offenen Stellen für ein hochauflösendes Bild
Bildnachweis: Salk Institute
Doch die Forscher erlebten eine Überraschung, als sie Axl und Mer aus den Parkinson-Mäusen entfernten. Anstatt schlechter zu sein als Mäuse mit der Krankheit, aber mit normalen Mikroglia, lebten die Mäuse, denen Axl und Mer fehlten, tatsächlich länger. Dies kann daran liegen, dass Axl und Mer kranke, dysfunktionale Neuronen angreifen und zerstören. Bei Vorliegen einer Krankheit könnte es mehr dysfunktionale Neuronen als normal geben, sodass Axl und Mer möglicherweise die Zerstörung zu vieler Neuronen veranlassen und so die Krankheit beschleunigen.
„Es scheint, dass wir den Krankheitsverlauf in einem Tiermodell verändern können, indem wir Axl und Mer manipulieren“, sagt Lawrence Fourgeaud, Co-Erstautor des Artikels und ehemaliger wissenschaftlicher Mitarbeiter von Salk. Das Team weist darauf hin, dass weitere Untersuchungen erforderlich sind, um festzustellen, ob die Modulation der TAM-Rezeptoren eine praktikable Therapie für neurodegenerative Erkrankungen mit Mikroglia sein könnte.
Weitere Forscher des Artikels waren Yusuf Tufail, Humberto Leal-Bailey, Erin D. Lew, Patrick G. Burrola, Perri Callaway, Anna Zagórska und Axel Nimmerjahn vom Salk Institute; und Carla V. Rothlin von der Yale University School of Medicine.
Die Arbeit wurde unterstützt durch die National Institutes of Health, hat das Leona M. und Harry B. Helmsley Charitable Trust, hat das Howard Hughes Medical Instituteund die Nomis, HN und Frances C. Berger, Fritz B. Burns, HKT, Warte, Rita Allenund Hearst Stiftungen
JOURNAL
Natur
AUTOREN
Lawrence Fourgeaud, Paqui G. Través, Yusuf Tufail, Humberto Leal-Bailey, Erin D. Lew, Patrick G. Burrola, Perri Callaway, Anna Zagórska, Carla V. Rothlin, Axel Nimmerjahn und Greg Lemke
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Das Institut hat es sich zur Aufgabe gemacht, grundlegende, kooperative und risikoreiche Forschung zu betreiben, die sich mit den drängendsten gesellschaftlichen Herausforderungen wie Krebs, Alzheimer und der Anfälligkeit der Landwirtschaft auseinandersetzt. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und generiert Erkenntnisse, die weltweit die Entwicklung neuer Medikamente und Innovationen ermöglichen.