
17 de fevereiro de 2016
Salk Institute e colaboradores mostram as principais diferenças moleculares entre os vírus à medida que interagem com o DNA do hospedeiro
Salk Institute e colaboradores mostram as principais diferenças moleculares entre os vírus à medida que interagem com o DNA do hospedeiro
LA JOLLA—Usando tecnologia de imagem de ponta, Salk Institute e Harvard Medical School pesquisadores determinaram a estrutura de um complexo proteico que permite que vírus semelhantes ao vírus da imunodeficiência humana (HIV) estabelecem infecções permanentes em seus hospedeiros.
Ao contrário das suposições anteriores, a estrutura complexa da proteína viral recentemente detalhada indica que esse tipo de arquitetura molecular difere entre os retrovírus. Essas informações ajudam a revelar como os retrovírus inserem suas informações genômicas nas células humanas e podem ter implicações não apenas no tratamento de doenças como o HIV, mas também na melhoria dos métodos de terapia genética para fornecer novo DNA a pacientes com mutações genéticas.
“Os detalhes de como os retrovírus se integram diferem muito mais do que se pensava anteriormente e levam a padrões totalmente distintos de infecção”, diz Dmitry Lyumkis, um Companheiro Salk e co-autor sênior do novo artigo, publicado em Natureza fevereiro 18, 2016.
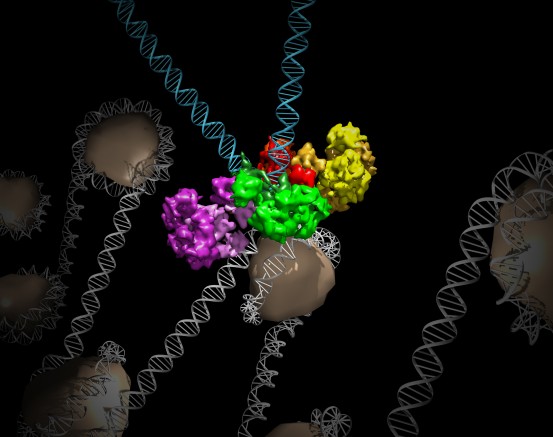
Clique aqui para uma imagem de alta resolução.
Crédito: Salk Institute
Um retrovírus insere sua informação genética no próprio genoma do hospedeiro, essencialmente transformando as células do hospedeiro em fábricas de produção de vírus. No caso do conhecido retrovírus HIV, esses genes virais se integram às células imunológicas humanas, acabando por matá-las. Um mistério de longa data - causado em parte pela falta de conhecimento sobre a estrutura do complexo proteico - é o que determina onde o DNA viral é inserido no genoma humano.
Um complexo proteico chamado intassoma é responsável pela inserção irreversível do DNA viral no DNA humano, uma etapa vital para permitir que os retrovírus causem doenças. Como o próprio intassoma do HIV é difícil de estudar, a maior parte do que se sabe sobre os intassomas se baseia no trabalho de outro retrovírus chamado protótipo do vírus espumoso, ou PFV. À luz dos desafios relacionados aos espécimes pertencentes aos intasomas do HIV, Lyumkis e Engelman, juntamente com seu colega Peter Cherepanov no Francis Crick Institute, decidiram determinar a estrutura do intassoma do vírus do tumor mamário do camundongo (MMTV), que de algumas maneiras está mais intimamente relacionado com o HIV do que com o PFV.
“A estrutura do intassoma MMTV define um novo paradigma inesperado para a base estrutural da integração do DNA retroviral”, diz o co-autor sênior Alan Engelman, professor de medicina no Dana-Farber Cancer Institute e na Harvard Medical School.
Para determinar a estrutura molecular do MMTV, a equipe usou uma técnica promissora chamada microscopia crioeletrônica (cryoEM), uma abordagem que tem várias vantagens sobre as técnicas tradicionais de imagem. Por exemplo, os pesquisadores não precisam transformar as proteínas em formas cristalinas para obter uma imagem delas, um processo imprevisível que é necessário para a técnica mais comum de cristalografia de raios-x. No cryoEM, as proteínas são congeladas diretamente em uma solução líquida. Então, medindo como os feixes de elétrons são desviados das amostras congeladas, os cientistas podem determinar a estrutura das proteínas.
Lyumkis usou essa tecnologia de ponta para detalhar a estrutura dos intasomas MMTV ligados a cadeias de DNA viral (a aparência da estrutura ao invadir uma célula hospedeira). A equipe descobriu que, enquanto o complexo PFV é composto por quatro componentes proteicos, chamados integrases, ligados a duas cadeias de DNA viral, o conjunto MMTV possui oito moléculas de integrase por dois pedaços de DNA viral.
Essa diferença estrutural fundamental, diz Lyumkis, significa que os complexos interagem de maneira diferente com o DNA do hospedeiro quando estão preparados para inserir o DNA viral no genoma. O PFV prefere pontos no genoma do hospedeiro que são altamente dobrados, enquanto o MMTV escolhe trechos retos de DNA. A preferência pelo HIV permanece um mistério, mas as novas observações fornecem uma estrutura molecular inesperada para interpretar dados passados e futuros sobre o HIV e outros retrovírus.
As equipes de Lyumkis e Engelman agora estão trabalhando para entender a série de eventos pelos quais o complexo intassoma MMTV passa durante as etapas de integração viral, desde a ligação do DNA viral até a captura do DNA do hospedeiro e a catalisação da inserção do DNA viral no genoma do hospedeiro. Lyumkis também planeja aplicar técnicas de cryoEM para estudar o próprio complexo molecular intassoma do HIV. “A infraestrutura tecnológica está pronta, então agora acho que podemos lidar com esses espécimes complicados e malcomportados usando cryoEM”, acrescenta Lyumkis.
Outros pesquisadores no estudo foram Allison Ballandras-Colas e Tamaria G. Dewdney do Instituto do Câncer Dana-Farber e Harvard Medical School; Monica Brown, do Salk Institute; Nicola J. Cook e Peter Cherepanov do Instituto Francis Crick; e Borries Demeler da Centro de Ciências da Saúde da Universidade do Texas.
O trabalho e os pesquisadores envolvidos foram apoiados por bolsas do National Institutes of Health, Leona M. e Harry B. Helmsley Charitable Trust, National Science Foundation e o San Antonio Cancer Institute.
JORNAL
Natureza
IMERSÃO DE INGLÊS
Cryo-EM revela uma nova estrutura de integrase octamérica para a função do intassoma betaretroviral
AUTORES
Allison Ballandras-Colas, Tamaria G. Dewdney e Alan Engelman da Harvard Medical School; Monica Brown e Dmitry Lyumkis do Salk Institute; Nicola J. Cook e Peter Cherepanov do Francis Crick Institute; e Borries Demeler do Centro de Ciências da Saúde da Universidade do Texas
Escritório de Comunicações
Tel: (858) 453-4100
press@salk.edu
O Instituto Salk é um instituto de pesquisa independente e sem fins lucrativos, fundado em 1960 por Jonas Salk, criador da primeira vacina segura e eficaz contra a poliomielite. A missão do Instituto é impulsionar pesquisas fundamentais, colaborativas e inovadoras que abordem os desafios mais urgentes da sociedade, incluindo câncer, doença de Alzheimer e vulnerabilidade agrícola. Essa ciência fundamental sustenta todos os esforços translacionais, gerando conhecimento que possibilita o desenvolvimento de novos medicamentos e inovações em todo o mundo.