
1 juni 2015
Deze nieuwe atlas van epigenomen van menselijke organen biedt een startpunt om de rol van chemische markers bij ontwikkeling, gezondheid en ziekte te begrijpen
Deze nieuwe atlas van epigenomen van menselijke organen biedt een startpunt om de rol van chemische markers bij ontwikkeling, gezondheid en ziekte te begrijpen
LA JOLLA – Al meer dan tien jaar beschikken wetenschappers over een werkende kaart van het menselijk genoom, een compleet beeld van de DNA-sequentie die het menselijk leven codeert. Maar er worden nog steeds nieuwe pagina's aan die atlas toegevoegd: kaarten van chemische markers, methylgroepen genaamd, die DNA-strengen bedekken en beïnvloeden welke genen worden onderdrukt en wanneer.
Nu hebben Salk-wetenschappers de meest uitgebreide kaarten tot nu toe gemaakt van deze chemische patronen - gezamenlijk het epigenoom genoemd - in meer dan een dozijn verschillende menselijke organen van individuele donoren (waaronder een vrouw, een man en een kind). Hoewel de methylering de overgeërfde genetische sequentie van een individu niet verandert, heeft onderzoek steeds meer aangetoond dat het een diepgaand effect heeft op ontwikkeling en gezondheid.
"Wat we ontdekten, is dat niet alle organen die we hebben onderzocht gelijk zijn in termen van hun methylatiepatronen", zegt senior auteur Joseph R.Ecker, professor en directeur van Salk's Laboratorium voor genomische analyse en mededirecteur van Het Centre of Excellence voor stamcelgenomica. "De handtekeningen van methylering zijn duidelijk genoeg tussen organen dat we naar de methylatiepatronen van een weefsel kunnen kijken en weten of het weefsel een spier of thymus of pancreas is." De nieuwe gegevens zijn op 1 juni 2015 gepubliceerd in NATUUR.
Hoewel het genoom van een individu in elke cel hetzelfde is, variëren epigenomen omdat ze nauw verwant zijn aan de genen die een cel daadwerkelijk op een bepaald moment gebruikt. Methyleringsmarkeringen helpen bloedcellen de genen te negeren die nodig zijn om bijvoorbeeld een hersen- of levercel te zijn. En ze kunnen in de loop van de tijd variëren - er is bijvoorbeeld aangetoond dat een verandering in iemands leeftijd, dieet of omgeving de methylering beïnvloedt.
"We wilden een basisbeoordeling maken van hoe het epigenoom, in het bijzonder DNA-methylatie, eruitziet in normale menselijke organen", zegt Ecker. Om dat te doen, verzamelden de wetenschappers cellen van 18 organen in 4 individuen en brachten hun methyleringsprofielen in kaart.
Van links: Matthew Schultz, Yupeng He en Joseph Ecker
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
Zoals verwacht kwamen de patronen enigszins overeen met genen waarvan bekend is dat ze belangrijk zijn voor de functie van een cel - er was bijvoorbeeld minder methylering in de buurt van spiergenen in cellen die uit spieren werden verzameld. Maar andere aspecten van de nieuwe kaarten waren verrassend. De onderzoekers ontdekten een ongebruikelijke vorm van methylering, niet-CG-methylering genaamd, waarvan men dacht dat deze alleen wijdverspreid was in de hersenen en stamcellen.
"De enige plaats waar dit eerder was waargenomen, was in de hersenen, skeletspieren, geslachtscellen en stamcellen", zegt Matthew Schultz, voormalig een afgestudeerde student in het Ecker-lab en een eerste auteur van het nieuwe werk. "Dus het was echt opwindend om het in verschillende normale volwassen weefsels te zien." Onderzoekers kennen de functie van die niet-CG-methylatie bij volwassenen nog niet, maar veronderstellen dat dit de aanwezigheid van stamcelpopulaties in de volwassen weefsels kan suggereren.
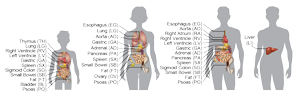
Een team van het Salk Institute bracht uitgebreide epigenomen van verschillende organen en weefseltypen van vier verschillende donoren in kaart, wat zou kunnen helpen om gezondheid en ziekte beter te begrijpen.
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
Het team vond andere verrassingen in hun onderzoek, die wijzen op nieuwe wegen om te verkennen. Ze ontdekten bijvoorbeeld dat veel regio's die dynamische methylering vertonen, zich niet bevinden waar verwacht - in een deel van het DNA dat de promotor wordt genoemd, evenals de regulerende regio's stroomopwaarts van de promotor. "In het verleden dachten mensen echt dat de promotor of de stroomopwaartse regio's zijn waar alles gebeurt", zegt Ecker, die ook een Howard Hughes Medical Institute en Gordon en Betty Moore Foundation-onderzoeker is. "Maar we ontdekten dat methyleringsveranderingen die het meest gecorreleerd zijn met gentranscriptie zich vaak in de stroomafwaartse regio's van de promotor bevinden." De observatie kan van invloed zijn op hoe en waar onderzoekers naar methylering zoeken wanneer ze bestuderen hoe een individueel gen wordt gereguleerd.
Een andere verrassing was hoe sterk organen van elkaar verschilden in de mate van genoombrede methylering. De alvleesklier had een ongewoon laag methylatieniveau, terwijl de thymus een hoog methylatieniveau had. Onderzoekers weten nog niet waarom.
De nieuwe resultaten krabben slechts het oppervlak van volledig begrip van DNA-methylatiepatronen - er zijn nog tientallen organen om te profileren, talloze onbekenden over wat het epigenoom vormt en verandert, en vragen over of verschillende cellen - zelfs binnen een enkel orgaan - variëren in hun methylatiepatronen .
"Wat interessant zou zijn om vervolgens te doen, is verschillende celtypen uitsplitsen", zegt Yupeng He, een afgestudeerde student in het Ecker-lab en co-eerste auteur van het nieuwe artikel. "De monsters die we hebben zijn heterogene mengsels van veel cellen."
De onderzoekers hopen echter dat de resultaten een startpunt bieden om te begrijpen hoe ziekten, zoals ziekten die de organen aantasten die ze hebben geprofileerd, kunnen worden weerspiegeld in veranderingen in het epigenoom.
"Je zou je kunnen voorstellen dat uiteindelijk, als iemand een probleem heeft, een biopsie niet alleen kijkt naar het karakteriseren van de cellen of genen, maar ook naar het epigenoom", zegt Ecker.
Andere onderzoekers van het onderzoek waren Manoj Hariharan, Eran A. Mukamel, Joseph R. Nery, Mark A. Urich, Huaming Chen en Terrence J. Sejnowski van het Salk Institute; John W. Whitaker, Siddarth Selvaraj en Wei Wang, van de University of California, San Diego; Danny Leung, Nisha Rajagopal, Inkyung Jung, Anthony D. Schmitt en Bing Ren, van de Ludwig Instituut voor Kankeronderzoek; Shin Lin, van Stanford University; en Yiing Lin, van de Washington University School of Medicine.
Het werk en de betrokken onderzoekers werden ondersteund door de National Institutes of Health Epigenome Roadmap-project Nationaal Instituut voor Neurologische Ziekten en Beroerte Gordon en Betty Moore Foundation en Howard Hughes Medical Institute.
Over het Salk Instituut voor Biologische Studies:
Het Salk Institute for Biological Studies is een van 's werelds meest vooraanstaande instellingen voor fundamenteel onderzoek, waar internationaal gerenommeerde faculteiten fundamentele levenswetenschappelijke vragen onderzoeken in een unieke, collaboratieve en creatieve omgeving. Salk-wetenschappers zijn zowel gericht op ontdekking als op het begeleiden van toekomstige generaties onderzoekers en leveren baanbrekende bijdragen aan ons begrip van kanker, veroudering, Alzheimer, diabetes en infectieziekten door neurowetenschappen, genetica, cel- en plantenbiologie en aanverwante disciplines te bestuderen.
Faculteitsprestaties zijn erkend met tal van onderscheidingen, waaronder Nobelprijzen en lidmaatschappen van de National Academy of Sciences. Het instituut, opgericht in 1960 door poliovaccinpionier Jonas Salk, MD, is een onafhankelijke non-profitorganisatie en architectonisch monument.
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu