
14 januari 2016
Salk-wetenschappers ontdekken hoe mitochondriën herstellen na schade, en bieden aanwijzingen voor kanker, diabetes en hersenziekte
Salk-wetenschappers ontdekken hoe mitochondriën herstellen na schade, en bieden aanwijzingen voor kanker, diabetes en hersenziekte
LA JOLLA—Mitochondria, de energiegeneratoren in onze cellen, zijn essentieel voor het leven. Wanneer ze worden aangevallen - door gifstoffen, omgevingsstress of genetische mutaties - wringen cellen deze krachtcentrales uit elkaar, halen de beschadigde stukken eruit en zetten ze weer in elkaar tot bruikbare mitochondriën.
Nu hebben wetenschappers van het Salk Institute een onverwachte manier ontdekt waarop cellen deze kritieke reactie op bedreigingen activeren, wat inzicht biedt in aandoeningen zoals mitochondriale ziekte, kanker, diabetes en neurodegeneratieve ziekte, met name de ziekte van Parkinson, die verband houdt met disfunctionele mitochondriën. Het werk verschijnt 15 januari 2016 in Wetenschap.

Klik hier voor een afbeelding in hoge resolutie.
Krediet: Salk Institute
"Buiten plunderaars komen in deze krachtcentrales van de cel - de mitochondriën - en als reactie daarop breken de krachtcentrales in kleinere fragmenten", zegt Ruben Shaw, senior auteur en Salk-professor in het laboratorium voor moleculaire en celbiologie.
In een gemiddelde menselijke cel produceren ergens tussen de 100 en 500 mitochondriën energie in de vorm van ATP-moleculen, die werken als batterijen om stroom naar de rest van de cel te transporteren. Op elk willekeurig moment fragmenteren een of twee mitochondria (splijting) of hervormen (fusie) om eventuele beschadigde delen uit te schakelen. Maar wanneer een gif, zoals cyanide of arseen, of andere gevaren de mitochondriën bedreigen, vindt er een massale fragmentatie plaats.
Onderzoekers weten al jaren dat mitochondriën deze fragmentatie ondergaan wanneer ze worden behandeld met medicijnen die de mitochondriën aantasten, maar de biochemische details van hoe de mitochondriënschade wordt waargenomen en hoe dat de snelle splijtingsreactie veroorzaakt, was tot nu toe niet duidelijk.
In het nieuwe werk ontdekte het Salk-team dat wanneer cellen worden blootgesteld aan mitochondriënschade, een centrale cellulaire brandstofmeter, het enzym AMPK, een noodwaarschuwing naar mitochondriën stuurt met de opdracht om uit elkaar te vallen in vele kleine mitochondriale fragmenten. Interessant is dat AMPK wordt geactiveerd door het veelgebruikte diabetestherapeutische metformine, evenals door lichaamsbeweging en een beperkt dieet. De nieuwe bevindingen suggereren dat sommige van de voordelen van deze therapieën het gevolg kunnen zijn van hun effecten op het bevorderen van de mitochondriale gezondheid.

Klik hier voor een afbeelding in hoge resolutie
Krediet: Salk Institute
Eerder onderzoek door de groep van Shaw en anderen had de rol van AMPK blootgelegd bij het helpen recyclen van beschadigde mitochondriale stukken en het signaleren van de cel om nieuwe mitochondriën te maken. Maar deze nieuwe rol van snel teweegbrengende mitochondriale fragmentatie "plaatst AMPK echt in het hart van de gezondheid van mitochondriën en het welzijn op de lange termijn", zegt Shaw, die ook houder is van de William R. Brody-leerstoel.
Om precies te ontdekken wat er in die eerste paar minuten gebeurt, gebruikte het team de genbewerkingstechniek CRISPR om AMPK in cellen te verwijderen en toonde aan dat, zelfs wanneer gif of andere bedreigingen in de mitochondriën worden geïntroduceerd, ze niet fragmenteren zonder AMPK. Dit geeft aan dat AMPK op de een of andere manier direct inwerkt op mitochondria om fragmentatie te induceren.
De groep keek vervolgens naar een manier om AMPK chemisch aan te zetten zonder aanvallen naar mitochondriën te sturen. Tot hun verbazing ontdekten ze dat alleen het activeren van AMPK voldoende was om de mitochondriën te laten fragmenteren, zelfs zonder de schade.
“Ik kon niet geloven hoe zwart-wit de resultaten waren. Alleen al door AMPK aan te zetten, krijg je net zoveel fragmentatie als een mitochondriaal gif", zegt Shaw.
Het team ontdekte waarom dit zo was: wanneer de energiecentrales van de cel worden verstoord, wordt de hoeveelheid energie die rond een cel zweeft - ATP - verlaagd. Al na een paar minuten detecteert AMPK deze vermindering van energie in de cel en haast zich naar de mitochondriën. Net als een bewaker die een brandalarm trekt, activeert AMPK een receptor op het buitenmembraan van een mitochondrion om te signaleren dat het fragmenteert.
Toen ze verder gingen, ontdekten de onderzoekers dat AMPK in feite inwerkt op twee gebieden van een mitochondriale receptor, de mitochondriale splijtingsfactor (MFF) genaamd, om het proces te starten. MFF roept een eiwit op, Drp1, dat zich bindt en rond het mitochondrion wikkelt als een gerolde strop om het te draaien en uit elkaar te halen.
"We ontdekten dat de wijziging van MFF door AMPK nodig is om MFF meer Drp1 naar de mitochondriën te laten sturen", zegt Erin Quan Toyama, een van de eerste auteurs van het artikel en een Salk-onderzoeksmedewerker. "Zonder AMPK die het alarm verzendt, kan MFF niet bellen naar Drp1 en is er geen nieuwe fragmentatie van mitochondriën na schade."
Volgens Sébastien Herzig, de andere eerste auteur van het artikel en een Salk-onderzoeksmedewerker, wil het team in de toekomst onderzoeken welke andere gevolgen deze signaalroute heeft voor specifieke celtypen. "We willen zien wat een defect in de communicatie tussen de mitochondriën en AMPK zou doen met verschillende weefsels, met name weefsels die erg afhankelijk zijn van gezonde mitochondriën, zoals hersenen, spieren en hart", zegt Herzig.
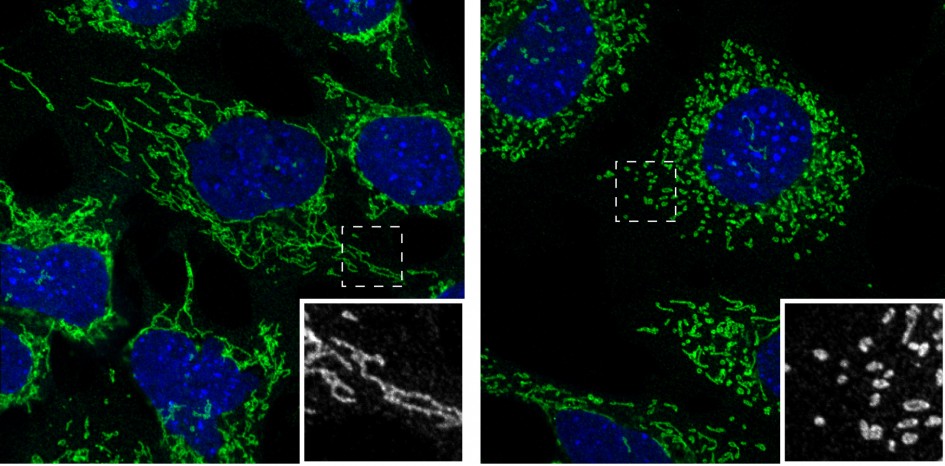
Klik hier voor een afbeelding in hoge resolutie
Krediet: Salk Institute
Toyama voegt eraan toe: “Aan de ene kant staat AMPK bekend als belangrijk voor diabetes type 2, immuunziekte en kanker. Aan de andere kant wordt mitochondriale disfunctie steeds meer in verband gebracht met stofwisselingsziekten en neurodegeneratieve ziekten. We zetten enkele van de eerste stappen in het verbinden van deze twee dingen die grote gevolgen hebben voor de ziekte."
Andere auteurs van het werk waren Kristina Hellberg en Nathan P. Young van het Salk Institute; Julien Courchet, Tommy L. Lewis Jr. en Franck Polleux van Columbia University; en Oliver C. Losón, Hsiuchen Chen en David C. Chan van de California Institute of Technology.
Het werk werd mede gefinancierd door de Howard Hughes Medical Institute, NIH en De Leona M. en Harry B. Helmsley Charitable Trust.
BLOG
Wetenschap
TITEL
AMP-geactiveerde proteïnekinase bemiddelt mitochondriale splijting als reactie op energiestress
AUTEURS
Erin Quan Toyama, Sébastien Herzig, Julien Courchet, Tommy L. Lewis Jr., Oliver C. Losón, Kristina Hellberg, Nathan P. Young, Hsiuchen Chen, Franck Polleux, David C. Chan, Reuben J. Shaw
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het ontsluiten van de geheimen van het leven zelf is de drijvende kracht achter het Salk Institute. Ons team van bekroonde wetenschappers van wereldklasse verlegt de grenzen van de kennis op gebieden als neurowetenschappen, kankeronderzoek, veroudering, immunobiologie, plantenbiologie, computationele biologie en meer. Het Instituut, opgericht door Jonas Salk, ontwikkelaar van het eerste veilige en effectieve poliovaccin, is een onafhankelijke onderzoeksorganisatie zonder winstoogmerk en een architectonisch monument: klein van opzet, intiem van aard en onbevreesd als het om uitdagingen gaat.