
November 28, 2023
Salk-onderzoekers ontdekken dat eiwit Mitf de reparatiefunctie in het perifere zenuwstelsel van muizen medieert, wat een potentieel nieuw therapeutisch doelwit biedt
Salk-onderzoekers ontdekken dat eiwit Mitf de reparatiefunctie in het perifere zenuwstelsel van muizen medieert, wat een potentieel nieuw therapeutisch doelwit biedt
LA JOLLA – Elk jaar zijn er in de Verenigde Staten meer dan 3 miljoen gevallen van perifere neuropathie, waarbij zenuwen buiten de hersenen en het ruggenmerg beschadigd raken en pijn en gevoelsverlies in de getroffen gebieden veroorzaken. Perifere neuropathie kan optreden als gevolg van diabetes, letsel, genetisch overgeërfde ziekten, infecties en meer. Salk-wetenschappers hebben nu bij muizen een mechanisme ontdekt voor het repareren van beschadigde zenuwen tijdens perifere neuropathie. Ze ontdekten dat het eiwit Mitf de reparatiefunctie van gespecialiseerde Schwann-cellen van het zenuwstelsel helpt inschakelen.
De bevindingen, gepubliceerd in Cell Reports op 28 november 2023 hebben het potentieel om nieuwe therapieën te inspireren die de herstelfunctie versterken en perifere neuropathie genezen.
“We wilden weten welke mechanismen de schadereactie in perifere zenuwen beheersen onder verschillende omstandigheden, zoals acuut trauma, genetische aandoeningen of degeneratieve ziekten”, zegt senior auteur professor. Samuel Paff. "We ontdekten dat Schwann-cellen, speciale cellen in zenuwen die de axonen van neuronen beschermen en ondersteunen, in hun hersteltoestand terechtkomen vanwege een route die wordt gemedieerd door het eiwit Mitf."
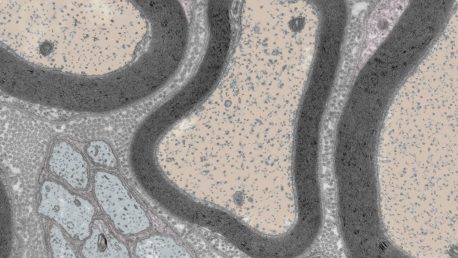
Het perifere zenuwstelsel bestaat uit alle zenuwen die zich vanuit de hersenen en het ruggenmerg vertakken en ons door ons hele lichaam sensaties geven. Er zijn veel celtypen in perifere zenuwen, maar Pfaff en zijn team concentreren zich op het begrijpen van neuronen, die informatie door het zenuwstelsel doorgeven, en Schwann-cellen, die gezonde neuronen beschermen en beschadigde neuronen repareren.
Het vermogen van het perifere zenuwstelsel om schade te herstellen is opmerkelijk gezien het feit dat het centrale zenuwstelsel – bestaande uit de hersenen en het ruggenmerg – niet in staat is om schade te herstellen. Toch zijn de mechanismen die deze prestatie orkestreren nog steeds slecht begrepen.
Om te ontrafelen hoe Schwann-cellen differentiëren om te beginnen met het herstellen van perifere zenuwbeschadiging, keken de onderzoekers naar muismodellen van de ziekte van Charcot Marie Tooth (CMT), een vorm van erfelijke neuropathie.
“Toen ik aan dit project begon, dacht ik dat als je een genetische zenuwdegeneratiestoornis hebt, de cellen afsterven en herstel niet mogelijk is”, zegt eerste auteur Lydia Daboussi, een voormalig postdoctoraal onderzoeker in het laboratorium van Pfaff en huidig assistent-professor aan de UC Los Angeles. . “Maar onze bevindingen laten zien dat er door Mitf genprogramma’s zijn ingeschakeld die een deel van de schade herstellen die wordt aangericht in die chronische ziektescenario’s, en als je die programma’s uitschakelt, worden de ziektesymptomen erger.”

Bij muizen met CMT merkten de onderzoekers dat de Schwann-cellen die de reparaties voltooiden een hoog gehalte aan Mitf in hun kernen hadden – waar de genetische instructies voor hoe je een Schwann-cel moet zijn en hoe je reparaties moet uitvoeren, worden opgeslagen.
Bij onderzoek naar deze relatie tussen Mitf- en Schwann-cellen ontdekten ze dat Mitf zich in het cytoplasma van Schwann-cellen bevond totdat ze neuronale schade waarnamen. Schade bracht Mitf er vervolgens toe om zich van het cytoplasma van de cel naar de kern te verplaatsen, waar het de Schwann-cel opdracht zou geven reparaties uit te voeren.
Om het belang van Mitf bij het creëren van reparatie-Schwann-cellen te valideren, hebben de onderzoekers Mitf helemaal verwijderd. In gevallen van zowel trauma als CMT werd het zenuwherstel stopgezet bij afwezigheid van Mitf, wat aantoont dat Mitf nodig is voor herstel en regeneratie van perifere zenuwen.
Volgens Daboussi fungeert Mitf als een brandblusser. Altijd daar, zittend in de Schwann-cel, onopgemerkt totdat er schade ontstaat. En wanneer die schade optreedt, is Mitf klaar om te gaan en schakelt hij onmiddellijk de reparatiefuncties van de cel in.
Het meest verrassende, merkte Pfaff op, was dat Mitf deze reparaties orkestreerde tijdens een chronische ziekte als CMT.
“Het inzetten van Schwann-celreparatieprogramma’s heeft een groot potentieel bij de behandeling van chronische ziekten”, zegt Pfaff, tevens voorzitter van de Benjamin H. Lewis-leerstoel bij Salk. “Het is mogelijk dat we met gerichte therapieën meer Schwann-cellen kunnen stimuleren om perifere zenuwbeschadiging te herstellen en die reparaties in chronische gevallen tot een goed einde te brengen. Bovendien kunnen we, nu we de reparatiemechanismen beter begrijpen, kijken of het mogelijk is om ook reparaties in de hersenstam en het ruggenmerg te initiëren.”
In de toekomst willen de onderzoekers specifieker kijken naar diabetesneuropathie, de meest voorkomende aandoening van perifere neuropathie. Ze hopen ook therapieën te onderzoeken die dit hersteltraject ondersteunen om meer Schwann-cellen te creëren die geprogrammeerd zijn om schade te herstellen, ongeacht of de bron trauma, genetica of ontwikkeling in de loop van de tijd is.
Andere auteurs zijn onder meer Giancarlo Costaguta, Miriam Gullo, Nicole Jasinski, Veronica Pessino, Brendan O'Leary, Karen Lettieri en Shawn Driscoll van Salk.
Het werk werd ondersteund door de Sol Goldman Charitable Trust, Howard Hughes Medical Institute, National Institutes of Health (subsidies NCI CCSG: P30 014195, NCI CCSG: P30 014195, S10 OD023427, S10 OD026929, 1 RO1 NS123160-01), een George E Hewitt Fellowship, een Salk Women & Science Fellowship en een Jonas Salk Fellowship.
DOI: https://doi.org/10.1016/j.celrep.2023.113282
BLOG
Cell Reports
AUTEURS
Lydia Daboussi, Giancarlo Costaguta, Miriam Gullo, Nicole Jasinski, Veronica Pessino, Brendan O'Leary, Karen Lettieri, Shawn Driscoll, Samuel L. Pfaff
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.