
6 april 2016
Salk-wetenschappers laten zien hoe immuunreceptoren dode en disfunctionele hersencellen opruimen en hoe ze doelwitten kunnen zijn voor de behandeling van neurodegeneratieve ziekten
Salk-wetenschappers laten zien hoe immuunreceptoren dode en disfunctionele hersencellen opruimen en hoe ze doelwitten kunnen zijn voor de behandeling van neurodegeneratieve ziekten
LA JOLLA - In de puberteit bevatten je hersenen al de meeste neuronen die je de rest van je leven zult hebben. Maar in een paar regio's blijven nieuwe zenuwcellen groeien - en hebben ze de hulp nodig van cellulaire schildwachten, gespecialiseerde immuuncellen die de hersenen beschermen door dode of disfunctionele cellen te verwijderen.
Nu hebben Salk-wetenschappers de verrassende mate ontdekt waarin zowel stervende als dode neuronen worden opgeruimd, en hebben ze specifieke cellulaire schakelaars geïdentificeerd die de sleutel zijn tot dit proces. Het werk was gedetailleerd in NATUUR april 6, 2016.
"We ontdekten dat receptoren op immuuncellen in de hersenen van vitaal belang zijn voor zowel een gezonde als een beschadigde toestand", zegt Greg Lemke, senior auteur van het werk, een Salk-professor in moleculaire neurobiologie en de houder van de Françoise Gilot-Salk-leerstoel. "Deze receptoren kunnen potentiële therapeutische doelen zijn voor neurodegeneratieve aandoeningen of ontstekingsgerelateerde aandoeningen, zoals Parkinson. '
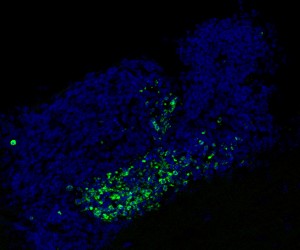
Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
Twee decennia geleden ontdekte het Lemke-lab dat immuuncellen kritische moleculen tot expressie brengen, TAM-receptoren genaamd, die sindsdien in veel laboratoria een focus zijn geworden voor auto-immuun- en kankeronderzoek. Twee van de TAM-receptoren, genaamd Mer en Axl, helpen immuuncellen, macrofagen genaamd, fungeren als vuilnismannen, die de meer dan 100 miljard dode cellen identificeren en consumeren die elke dag in een menselijk lichaam worden gegenereerd.
Voor de huidige studie vroeg het team of Mer en Axl hetzelfde werk deden in de hersenen. Gespecialiseerde macrofagen van het centrale zenuwstelsel, microglia genaamd, vormen ongeveer 10 procent van de cellen in de hersenen, waar ze ziekteverwekkers detecteren, erop reageren en vernietigen. De onderzoekers verwijderden Axl en Mer in de microglia van verder gezonde muizen. Tot hun verbazing ontdekten ze dat de afwezigheid van de twee receptoren resulteerde in een grote opeenhoping van dode cellen, maar niet overal in de hersenen. Cellulaire lijken werden alleen gezien in de kleine regio's waar de productie van nieuwe neuronen - neurogenese - wordt waargenomen.
Veel cellen sterven normaal tijdens volwassen neurogenese, maar ze worden onmiddellijk opgegeten door microglia. "Het is heel moeilijk om zelfs maar een enkele dode cel in een normaal brein te detecteren, omdat ze zo efficiënt worden herkend en opgeruimd door microglia", zegt Paqui G. Través, een co-eerste auteur van de krant en voormalig Salk-onderzoeksmedewerker. "Maar in de neurogene gebieden van muizen zonder Mer en Axl hebben we veel van dergelijke cellen gedetecteerd."
Toen de onderzoekers dit proces nader onderzochten door de nieuw groeiende neuronen in de microglia van muizen die Mer en Axl misten te taggen, merkten ze nog iets interessants op. Nieuwe neuronen die migreren naar de bulbus olfactorius, of het reukcentrum, namen dramatisch toe zonder Axl en Mer in de buurt. Muizen zonder de TAM-receptoren hadden een toename van 70 procent in nieuw gegenereerde cellen in de bulbus olfactorius dan normale muizen.
Hoe - en in welke mate - deze ongecontroleerde nieuwe neurale groei het reukvermogen van een muis beïnvloedt, is volgens Lemke nog niet bekend, hoewel het een gebied is dat het lab zal onderzoeken. Maar het feit dat zoveel meer levende zenuwcellen in staat waren om naar de bulbus olfactorius te migreren in afwezigheid van de receptoren, suggereert dat Mer en Axl een andere rol spelen dan het opruimen van dode cellen - ze kunnen zich in feite ook richten op levende, maar functioneel gecompromitteerde cellen. .

Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
"Het lijkt erop dat een aanzienlijk deel van de celdood in neurogene regio's niet te wijten is aan intrinsieke dood van de cellen, maar eerder het gevolg is van de microglia zelf, die een fractie van de cellen doden door verzwelging", zegt Lemke. "Met andere woorden, sommige van deze voorlopers van pasgeboren neuronen worden levend opgegeten."
Dit is niet noodzakelijk een slechte zaak in het gezonde brein, voegt Lemke toe. De hersenen produceren meer neuronen dan ze kunnen gebruiken en snoeien vervolgens de cellen terug die niet nodig zijn. In een ontstoken of ziek brein kan de vernietiging van levende cellen echter averechts werken.
Het Lemke-lab deed nog een reeks experimenten om de rol van TAM-receptoren bij ziekte te begrijpen: ze keken naar de activiteit van Axl en Mer in een muismodel van de ziekte van Parkinson. Dit model produceert een menselijk eiwit dat aanwezig is in een erfelijke vorm van de ziekte die resulteert in een langzame degeneratie van de hersenen. Het team zag dat Axl veel actiever was in deze setting, in overeenstemming met andere onderzoeken die aantonen dat verhoogde Axl een betrouwbare indicator is van ontsteking in weefsels.
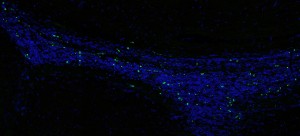
Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
Maar de onderzoekers stonden voor een verrassing toen ze Axl en Mer verwijderden van de Parkinson-muizen. In plaats van slechter af te zijn in vergelijking met muizen met de ziekte maar met normale microglia, leefden de muizen die Axl en Mer misten langer. Dit kan zijn omdat Axl en Mer zieke, disfunctionele neuronen targeten en vernietigen. In de aanwezigheid van ziekte kunnen er meer disfunctionele neuronen zijn dan normaal, dus Axl en Mer kunnen de vernietiging van te veel neuronen veroorzaken, waardoor de ziekte in feite wordt versneld.
"Het lijkt erop dat we het verloop van de ziekte in een diermodel kunnen wijzigen door Axl en Mer te manipuleren", zegt Lawrence Fourgeaud, mede-eerste auteur van de krant en voormalig Salk-onderzoeksmedewerker. Het team waarschuwt dat er meer onderzoek moet worden gedaan om te bepalen of het moduleren van de TAM-receptoren een levensvatbare therapie zou kunnen zijn voor neurodegeneratieve ziekte waarbij microglia betrokken zijn.
Andere onderzoekers op het papier waren Yusuf Tufail, Humberto Leal-Bailey, Erin D. Lew, Patrick G. Burrola, Perri Callaway, Anna Zagórska en Axel Nimmerjahn van het Salk Institute; en Carla V. Rothlin van de Yale University School of Medicine.
Het werk werd ondersteund door de National Institutes of Health Leona M. en Harry B. Helmsley Charitable Trust Howard Hughes Medical Instituteen Nomis, HN en Frances C. Berger, Fritz B. Burns, HKT, Wacht, Rita Allenen Hearst stichtingen.
BLOG
NATUUR
AUTEURS
Lawrence Fourgeaud, Paqui G. Través, Yusuf Tufail, Humberto Leal-Bailey, Erin D. Lew, Patrick G. Burrola, Perri Callaway, Anna Zagórska, Carla V. Rothlin, Axel Nimmerjahn & Greg Lemke
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.