
December 5, 2016
Salk-wetenschappers vinden dat stamcellen alleen gezond zijn als de lengte van de telomeren precies goed is
Salk-wetenschappers vinden dat stamcellen alleen gezond zijn als de lengte van de telomeren precies goed is
LA JOLLA - Sinds onderzoekers de verkorting van telomeren - de beschermende structuren aan de uiteinden van chromosomen - in verband brachten met veroudering en ziekte, is de race bezig om de factoren te begrijpen die de lengte van telomeren bepalen. Nu hebben wetenschappers van het Salk Institute ontdekt dat een evenwicht tussen verlenging en trimmen van stamcellen resulteert in telomeren die, zoals Goudlokje zou zeggen, niet te kort en niet te lang zijn, maar precies goed.
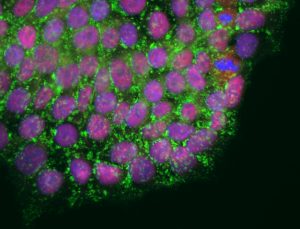
Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
De bevinding, die verschijnt in de uitgave van 5 december 2016 van Nature Structural & Molecular Biology, verdiept ons begrip van stamcelbiologie en zou kunnen helpen bij het bevorderen van op stamcellen gebaseerde therapieën, met name met betrekking tot veroudering en regeneratieve geneeskunde.
"Dit werk laat zien dat de optimale lengte voor telomeren een zorgvuldig gereguleerd bereik is tussen twee uitersten", zegt Jan Karlseder, een professor in Salk's Molecular and Cell Biology Laboratory en senior auteur van het werk. “Het was bekend dat zeer korte telomeren schade toebrengen aan een cel. Maar wat totaal onverwacht was, was onze bevinding dat er ook schade optreedt als telomeren erg lang zijn.”
Telomeren zijn repetitieve stukjes DNA aan de uiteinden van elk chromosoom waarvan de lengte kan worden vergroot door een enzym dat telomerase wordt genoemd. Onze cellulaire machinerie zorgt ervoor dat een klein stukje van de telomeer wordt afgehakt telkens wanneer cellen hun DNA repliceren en delen. Naarmate telomeren in de loop van de tijd korter worden, worden de chromosomen zelf kwetsbaar voor beschadiging. Uiteindelijk sterven de cellen af. De uitzondering zijn stamcellen, die telomerase gebruiken om hun telomeren opnieuw op te bouwen, waardoor ze hun vermogen om te delen behouden en zich kunnen ontwikkelen ("differentiëren") tot vrijwel elk celtype voor het specifieke weefsel of orgaan, of het nu gaat om huid, hart, lever of spieren - een eigenschap die bekend staat als pluripotentie. Deze eigenschappen maken stamcellen tot veelbelovende hulpmiddelen voor regeneratieve therapieën om leeftijdsgebonden cellulaire schade en ziekte te bestrijden.
"In onze experimenten bracht het beperken van de lengte van telomeren de pluripotentie in gevaar en resulteerde zelfs in stamceldood", zegt Teresa Rivera, een Salk-onderzoeksmedewerker en eerste auteur van het artikel. "Dus toen wilden we weten of toenemende telomeerlengte de pluripotente capaciteit verhoogde. Verrassend genoeg ontdekten we dat te langwerpige telomeren kwetsbaarder zijn en DNA-schade ophopen."
Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
Karlseder, Rivera en collega's begonnen met het onderzoeken van telomeeronderhoud in in het laboratorium gekweekte lijnen van menselijke embryonale stamcellen (ESC's). Met behulp van moleculaire technieken varieerden ze de telomerase-activiteit. Misschien niet verrassend, cellen met te weinig telomerase hadden zeer korte telomeren en uiteindelijk stierven de cellen. Omgekeerd hadden cellen met verhoogde niveaus van telomerase zeer lange telomeren. Maar in plaats van dat deze cellen gedijen, ontwikkelden hun telomeren instabiliteiten.
"We waren verrast toen we ontdekten dat het dwingen van cellen om echt lange telomeren te genereren, telomere fragiliteit veroorzaakte, wat kan leiden tot het ontstaan van kanker", zegt Karlseder, die ook de Donald en Darlene Shiley-leerstoel bekleedt. "Deze experimenten zetten vraagtekens bij het algemeen aanvaarde idee dat het kunstmatig verhogen van telomeren het leven kan verlengen of de gezondheid van een organisme kan verbeteren."
Het team merkte op dat zeer lange telomeren trimmechanismen activeerden die werden aangestuurd door een paar eiwitten genaamd XRCC3 en Nbs1. De experimenten van het laboratorium tonen aan dat verminderde expressie van deze eiwitten in ESC's het trimmen van telomeren verhinderde, wat bevestigt dat XRCC3 en Nbs1 inderdaad verantwoordelijk zijn voor die taak.
Vervolgens keek het team naar geïnduceerde pluripotente stamcellen (iPSC's), dit zijn gedifferentieerde cellen (bijvoorbeeld huidcellen) die opnieuw worden geprogrammeerd naar een stamcelachtige staat. iPSC's - omdat ze genetisch kunnen worden gekoppeld aan donoren en gemakkelijk verkrijgbaar zijn - zijn veelgebruikte en cruciale hulpmiddelen voor potentiële stamceltherapieën. De onderzoekers ontdekten dat iPSC's markers bevatten voor het trimmen van telomeren, waardoor hun aanwezigheid een nuttige graadmeter is voor hoe succesvol een cel is geherprogrammeerd.
“Het herprogrammeren van stamcellen is een grote wetenschappelijke doorbraak, maar de methoden worden nog steeds geperfectioneerd. Begrijpen hoe de lengte van telomeren wordt gereguleerd, is een belangrijke stap in de richting van het waarmaken van de belofte van stamceltherapieën en regeneratieve geneeskunde”, zegt Rivera.
Andere auteurs waren Candy Haggblom van het Salk Institute en Sandro Cosconati van de Tweede universiteit van Napels.
Het werk werd gefinancierd door de Californisch Instituut voor Regeneratieve Geneeskunde opleidingsbeurs TG2-01158, de Kankercentrum van het Salk Instituut Kernbeurs (P30CA014195), de National Institutes of Health (R01GM087476, R01CA174942), de Stichting Hooglandstraat, de Fritz B. Burns Foundation, de Emerald Foundation en de Glenn Centrum voor onderzoek naar veroudering.
BLOG
Nature Structural & Molecular Biology
TITEL
Een balans tussen telomeerverlenging en trimmen reguleert de telomeerstabiliteit in stamcellen
AUTEURS
Teresa Rivera, Candy Haggblom, Sandro Cosconati, Jan Karlseder
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.