
24 juni 2015
In een onverwachte bevinding laten het Salk Institute en medewerkers zien hoe het uitschakelen van telomeerbescherming tijdens celdeling leidt tot celdood
In een onverwachte bevinding laten het Salk Institute en medewerkers zien hoe het uitschakelen van telomeerbescherming tijdens celdeling leidt tot celdood
LA JOLLA – Telomeren, gespecialiseerde uiteinden van onze chromosomen die bepalen hoe lang cellen zichzelf kunnen blijven dupliceren, zijn al lang bestudeerd vanwege hun verband met het verouderingsproces en kanker. Nu toont een ontdekking aan het Salk Institute aan dat telomeren mogelijk meer centraal staan dan eerder werd gedacht in een zelfvernietigingsprogramma in cellen dat tumoren voorkomt, een functie die mogelijk kan worden benut om kankertherapieën te verbeteren.
Wanneer cellen repliceren in een proces dat mitose wordt genoemd, worden hun telomeren elke keer een beetje korter. Uiteindelijk, na vele celdelingen, worden telomeren kritiek kort, wat de cel signaleert om te stoppen met delen. Dit normale proces werkt als een barrière tegen kanker. Cellen met defecten in de signaalroute gaan echter door na dit stadium om zichzelf te vernietigen.
Dit proces van celvernietiging, crisis genaamd, voorkomt meestal dat genetisch onstabiele of beschadigde cellen zich vermenigvuldigen. Maar veel soorten kankercellen omzeilen een crisis door de telomeren te beschermen om het zelfvernietigingssignaal te belemmeren en cellen in staat te stellen zich te blijven vermenigvuldigen.
"We wilden het mechanisme van celdood in een crisis begrijpen en vonden een veel actievere rol van telomeren als barrières voor de ontwikkeling van tumoren dan eerder werd gedacht," zegt Jan Karlseder, Salk-professor in de Laboratorium voor moleculaire en celbiologie en senior auteur van het werk. "Het begon toen we zagen dat mitose langer duurt in cellen die een crisis naderen." Het werk was gedetailleerd in NATUUR juni 24, 2015.
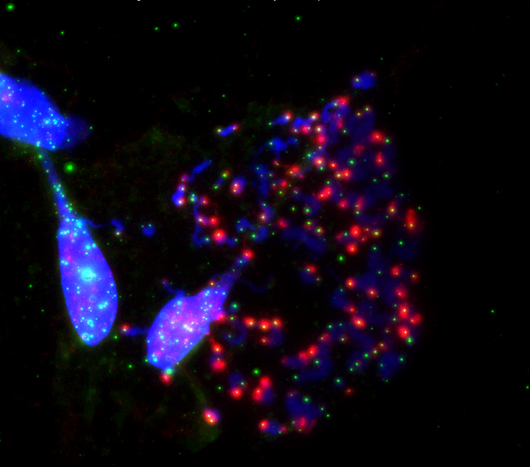
Salk-onderzoekers laten zien hoe de uitgeschakelde bescherming van uiteinden van chromosomen (blauw) genaamd telomeren (groen) tijdens celdeling (mitose) celdood veroorzaakt. Dit gebeurt wanneer het telomeerbeschermende eiwit TRF2 wordt geremd. Deze afbeelding toont een verergering van telomere ontscherming (rood) tijdens mitotische arrestatie door kunstmatige manipulatie van TRF2.
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
Terwijl normale mitose doorgaans ongeveer 30-45 minuten duurt, hebben cellen die op het punt staan in crisis te raken een mitose die 2-20 uur of langer duurt. Het observeren hiervan deed de onderzoekers denken aan a 2012 ontdekking waar ze het mitoseproces kunstmatig verlengden. Doorgaans hebben telomeren een eiwit dat hen beschermt tegen identificatie door de cel als beschadigd DNA en zo verhindert dat ze overgaan tot celdood. Maar tijdens kunstmatig verlengde mitose verloren telomeren het eiwit, wat leidde tot een DNA-schadesignaal dat de cellen ertoe aanzette zichzelf te vernietigen.
Tot hun verbazing ontdekten de wetenschappers dat precies hetzelfde gebeurde in de natuurlijke crisistoestand. In dit nieuwe werk maakten de onderzoekers real-time beeldvorming van cellen in een schaal om het lot van de cellen te volgen door een of meer mitotische cycli. Ze ontdekten dat een soort cellulaire stress, telomeerfusie genaamd, een langdurige mitose en uiteindelijk een crisis kan veroorzaken. Cellen in deze toestand verloren hun telomeerbeschermende eiwit en activeerden de zelfvernietigingssequentie.
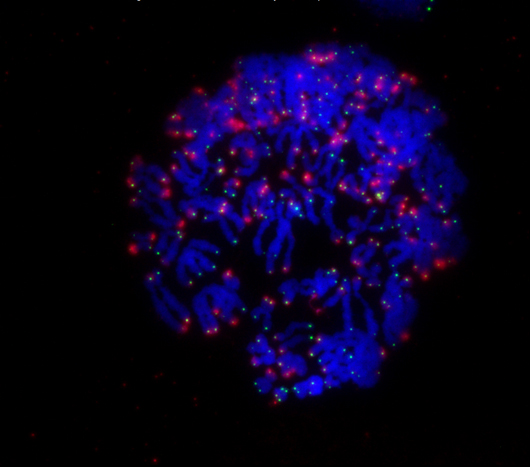
Tijdens mitose delen de chromosomen (blauw) van een cel zich snel. Wanneer de uiteinden van chromosomen die telomeren (groen) worden genoemd niet langer worden beschermd door het eiwit TRF2, krijgt de cel een signaal (rood) om celdood te ondergaan.
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
"Er was een lang bestaande hypothese die onjuist bleek te zijn: dat cellen gewoon beginnen met het samensmelten van chromosomen en uiteenvallen, waardoor instabiliteit en celdood ontstaan", zegt Karlseder, die ook de houder is van de Donald en Darlene Shiley-leerstoel van Salk. "Wat we in plaats daarvan laten zien, is dat het een veel gerichter pad is dat eigenlijk maar één celcyclus nodig heeft om een crisis te veroorzaken - het heeft niets te maken met de langzame en gestage accumulatie van genomische instabiliteit."
Anthony Cesare, hoofd van de Genome Integrity Group bij Medisch Onderzoeksinstituut voor Kinderen in Australië en een medewerker aan het werk, zei dat de bevinding erg opwindend was en dat het onverwacht was om te zien hoe gebeurtenissen vroeg in de celcyclus, telomeerfusies, worden doorgegeven aan een later stadium van de celcyclus, mitose. "Dit opent nieuwe wegen om te begrijpen hoe telomeren de celgroei controleren en de implicaties van telomeerbiologie bij chemotherapie", zegt hij.
Verschillende chemotherapieën, zoals Taxol voor borstkanker, proberen kanker te stoppen door de mitose te onderbreken, zodat kankercellen zich niet langer kunnen delen. De onderzoekers veronderstellen dat ze deze mitotische remmers kunnen versterken door bijvoorbeeld eerst telomeren te deprotecteren om de cellen vatbaarder te maken voor medicijnen. Het zou ook mogelijk kunnen zijn om te zien of cellen van een bepaalde tumor kortere of onbeschermde telomeren hadden en, zo ja, te verwachten dat die tumor veel gevoeliger is voor mitotische remmers.
"Het pad dat we hebben gevonden daagt een lang gekoesterde hypothese over cellulair gedrag tijdens vroege tumorvorming uit", zegt Makoto Hayashi, een onderzoeker aan het Hakubi Center for Advanced Research aan de Universiteit van Kyoto en eerste auteur van het nieuwe werk. "Uitgebreid begrip van het pad zal ons hopelijk een nieuwe methode bieden voor vroege tumordiagnose en een therapeutische mogelijkheid voor een zeer vroeg stadium van kanker."
Het lab werkt momenteel samen met Deborah Kado, MD, MS, aan de Universiteit van Californië, San Diego om deze theorieën te testen bij patiënten met nieuw gediagnosticeerde borstkanker.
Auteurs van de studie zijn Makoto T. Hayashi van de Universiteit van Kyoto, Anthony J. Cesare van het Children's Medical Research Institute, en Teresa Rivera en Jan Karlseder van het Salk Institute.
Dit werk werd gefinancierd door de Human Frontier Science-programma en Japan Society for the Promotion of Science Postdoctorale beurzen voor onderzoek in het buitenland National Institutes of Health, de Donald en Darlene Shiley-stoel, de Stichting Hooglandstraat, de Fritz B. Burns Foundation, de Smaragd Stichtingen Glenn Centrum voor onderzoek naar veroudering.
BLOG
NATUUR
AUTEURS
Makoto T. Hayashi, Anthony J. Cesare, Teresa Rivera en Jan Karlseder
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.