
August 19, 2020
Salk-onderzoekers ontwikkelen transplanteerbare menselijke cellen die insuline maken en de bloedsuikerspiegel reguleren zonder immunosuppressiva in muismodellen
Salk-onderzoekers ontwikkelen transplanteerbare menselijke cellen die insuline maken en de bloedsuikerspiegel reguleren zonder immunosuppressiva in muismodellen
LA JOLLA - Wetenschappers van het Salk Institute hebben een grote stap gezet in het streven naar een veilige en effectieve behandeling van diabetes type 1, een ziekte die naar schatting 1.6 miljoen Amerikanen treft en jaarlijks 14.4 miljard dollar kost.
Met behulp van stamceltechnologie genereerden Salk-onderzoekers de eerste menselijke insulineproducerende pancreascelclusters die het immuunsysteem konden omzeilen, zoals beschreven in het tijdschrift NATUUR op 19 augustus 2020. Deze "immuun-afgeschermde" celclusters regelden de bloedglucose zonder immunosuppressiva bij muizen, eenmaal getransplanteerd in het lichaam.
"De meeste type 1-diabetici zijn kinderen en tieners", zegt professor Salk Ronald Evans, senior auteur en houder van de March of Dimes Chair in Molecular and Developmental Biology. “Dit is een ziekte die van oudsher moeilijk te behandelen is met medicijnen. We hopen dat regeneratieve geneeskunde in combinatie met immuunafscherming een echt verschil kan maken in het veld door beschadigde cellen te vervangen door in het laboratorium gegenereerde menselijke eilandjesachtige celclusters die op verzoek normale hoeveelheden insuline produceren.”
Type 1-diabetes is een levenslange aandoening die moeilijk te behandelen is, zelfs met geautomatiseerde apparaten die insuline toedienen om de bloedsuikerspiegel te reguleren. Transplantaties van alvleesklier-bèta-eilandjes - clusters van cellen die insuline en andere hormonen maken - uit donorweefsel kunnen genezing bieden, maar vereisen dat patiënten levenslang immunosuppressieve medicijnen gebruiken, die ernstige risico's met zich meebrengen. Decennia lang hebben onderzoekers gezocht naar een betere manier om verloren pancreascellen aan te vullen. Nu brengt apparaatloze transplantatie van insulineproducerende cellen zoals deze ons een stap dichter bij het genezen van de ziekte, aldus het laboratorium.
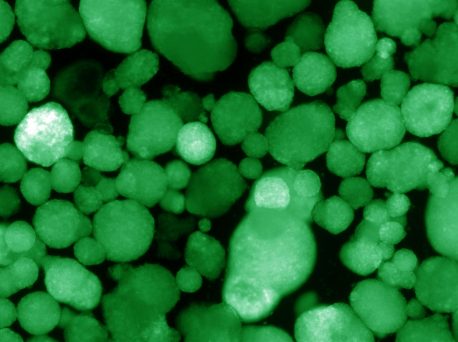
Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
In een eerdere studie, overwon het Evans-lab een belemmering in het veld, waarbij van stamcellen afgeleide bèta-achtige cellen insuline produceerden, maar niet functioneel waren. Volgens Evans gaven de cellen geen insuline af als reactie op glucose, omdat ze simpelweg te weinig stroom hadden. Zijn team ontdekte een genetische schakelaar genaamd ERR-gamma die, wanneer deze wordt omgedraaid, de cellen "turbo-oplaadt".
"Als we ERR-gamma toevoegen, hebben de cellen de energie die ze nodig hebben om hun werk te doen", zegt Michael Downes, senior stafwetenschapper bij Salk en co-auteur van beide onderzoeken. "Deze cellen zijn gezond en robuust en kunnen insuline toedienen wanneer ze hoge glucosespiegels waarnemen."
Een cruciaal onderdeel van de nieuwe studie was het ontwikkelen van een manier om bèta-achtige cellen te laten groeien in een driedimensionale omgeving die de menselijke alvleesklier benadert. Dit gaf de cellen een eilandje-achtige eigenschap. Belangrijk is dat het team ontdekte dat een eiwit genaamd WNT4 in staat was om de ERR-gamma-gestuurde rijpingsschakelaar aan te zetten. Deze combinatie van stappen genereerde functionele celclusters die menselijke eilandjes nabootsen: zogenaamde human islet-like organoids (HILO's).
Vervolgens pakte het team het complexe probleem van immuunafstoting aan. Normale weefseltransplantaties vereisen levenslange immuunonderdrukkende therapieën om het weefsel te beschermen tegen aanvallen door het immuunsysteem; deze therapieën verhogen echter ook het risico op infecties. Geïnspireerd door de successen van immunotherapiemedicijnen voor kanker, toonde het team aanvankelijk aan dat het checkpoint-eiwit PD-L1 de getransplanteerde cellen beschermde. "Door PD-L1 tot expressie te brengen, dat werkt als een immuunblokker, kunnen de getransplanteerde organoïden zich verbergen voor het immuunsysteem", zegt eerste auteur Eiji Yoshihara, een voormalig stafwetenschapper in het laboratorium.

Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
Yoshihara ontwikkelde vervolgens een methode om PD-L1 in HILO's te induceren met korte pulsen van het eiwit interferon-gamma. Wanneer ze werden getransplanteerd in diabetische muizen, zorgden deze immuunontwijkende HILO's voor een langdurige controle van de bloedglucose bij diabetische muizen met een gezond immuunsysteem.
"Dit is de eerste studie die aantoont dat je HILO's kunt beschermen tegen het immuunsysteem zonder genetische manipulatie", legt Downes uit. "Als we dit als therapie kunnen ontwikkelen, hoeven patiënten geen immuunonderdrukkende medicijnen te nemen."
Er moet meer onderzoek worden gedaan voordat dit systeem kan worden gebruikt voor klinische proeven. De getransplanteerde organoïden moeten gedurende langere tijd in muizen worden getest om te bevestigen dat hun effecten langdurig zijn. Er moet meer werk worden verzet om ervoor te zorgen dat ze ook veilig kunnen worden gebruikt bij mensen. "We hebben nu een product dat mogelijk bij patiënten kan worden gebruikt zonder dat er een apparaat voor nodig is", concludeert Evans.
Andere onderzoekers op het papier waren Carolyn O'Connor, Emanuel Gasser, Zong Wei, Tae Gyu Oh, Tiffany W. Tseng, Dan Wang, Fritz Cayabyab, Yang Dai, Ruth T. Yu en Annette R. Atkins van Salk en Christopher Liddle van het Westmead Institute for Medical Research en de Sydney Medical School in Australië.
Dit werk werd ondersteund door subsidies van het California Institute of Regenerative Medicine subsidie DISC2-11175, National Institutes of Health subsidie 1RO1DK120480-01, de Leona M. en Harry B. Helmsley Charitable Trust, aan Evans. Liddle en Downes werden gefinancierd door subsidies van het National Health and Medical Research Council of Australia Project. Yoshihara werd ondersteund door een P&F-beurs van de DRC. Dank ook aan Steven en Lisa Altman voor hun steun aan het lab.
DOI: 10.1038 / s41586-020-2631-z
Voor een FAQ over dit werk, Klik hier..
BLOG
NATUUR
AUTEURS
Eiji Yoshihara, Carolyn O'Connor, Emanuel Gasser, Zong Wei, Tae Gyu Oh, Tiffany W. Tseng, Dan Wang, Fritz Cayabyab, Yang Dai, Ruth T. Yu, Christopher Liddle, Annette R. Atkins, Michael Downes, Ronald M Evans
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.