
August 23, 2019
Salk-wetenschappers ontwikkelen een nieuwe tool voor het bewerken van het genoom die kan helpen bij de behandeling van veel aandoeningen die worden veroorzaakt door genmutaties
Salk-wetenschappers ontwikkelen een nieuwe tool voor het bewerken van het genoom die kan helpen bij de behandeling van veel aandoeningen die worden veroorzaakt door genmutaties
LA JOLLA—Het vermogen om genen in levende organismen te bewerken, biedt de mogelijkheid om een overvloed aan erfelijke ziekten te behandelen. Veel soorten hulpmiddelen voor het bewerken van genen zijn echter niet in staat zich op kritieke delen van het DNA te richten, en het creëren van een dergelijke technologie was moeilijk omdat levend weefsel verschillende soorten cellen bevat.
Nu hebben onderzoekers van het Salk Institute een nieuwe tool ontwikkeld, genaamd SATI, om het muizengenoom te bewerken, waardoor het team zich kan richten op een breed scala aan mutaties en celtypen. De nieuwe technologie voor genoombewerking, beschreven in Celonderzoek op 23 augustus 2019, zou kunnen worden uitgebreid voor gebruik bij een breed scala aan genmutatieaandoeningen, zoals de ziekte van Huntington en het zeldzame progeria-syndroom.
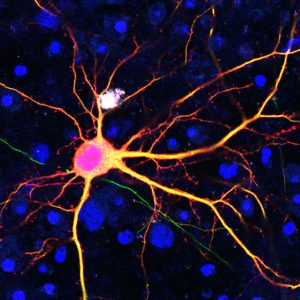
Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
"Deze studie heeft aangetoond dat SATI een krachtig hulpmiddel is voor genoombewerking", zegt Juan Carlos Izpisua Belmonte, een professor in het Gene Expression Laboratory van Salk en senior auteur van het artikel. "Het zou een belangrijke rol kunnen spelen bij het ontwikkelen van effectieve strategieën voor het vervangen van doelgenen van veel verschillende soorten mutaties, en het opent de deur voor het gebruik van hulpmiddelen voor het bewerken van het genoom om mogelijk een breed scala aan genetische ziekten te genezen."
Technieken die DNA wijzigen - met name het CRISPR-Cas9-systeem - zijn over het algemeen het meest effectief geweest bij het delen van cellen, zoals die in de huid of de darmen, met behulp van de normale DNA-herstelmechanismen van de cellen. Het Izpisua Belmonte-laboratorium eerder getoond dat hun op CRISPR/Cas9 gebaseerde technologie voor het bewerken van genen, HITI genaamd (voor homologie-onafhankelijke gerichte integratie), zich zowel op delende als niet-delende cellen kan richten. Eiwitcoderende regio's functioneren als recepten voor het maken van eiwitten, terwijl gebieden die niet-coderende regio's worden genoemd, fungeren als chef-koks die beslissen hoeveel voedsel ze moeten maken. Deze niet-coderende regio's vormen de overgrote meerderheid van het DNA (~ 98%) en reguleren veel cellulaire functies, waaronder het in- en uitschakelen van genen, en kunnen dus een waardevol doelwit zijn voor toekomstige gentherapieën.
"We probeerden een veelzijdige tool te creëren om deze niet-coderende delen van het DNA aan te pakken, die de functie van het gen niet zouden beïnvloeden, en het mogelijk maken om een breed scala aan mutaties en celtypen te targeten", zegt Mako Yamamoto, co- eerste auteur op het papier en een postdoctoraal onderzoeker in het Izpisua Belmonte lab. "Als proof-of-concept hebben we ons gericht op een muismodel van vroegtijdige veroudering veroorzaakt door een mutatie die moeilijk te herstellen is met behulp van bestaande hulpmiddelen voor het bewerken van het genoom."
De nieuwe gen-knock-in-methode, die de wetenschappers SATI noemen (afkorting van intercellulair gelineariseerd Senkele homologie Arm donor gemedieerde intron-Truzie maken Iintegratie) is een verbetering van de vorige HITI-methode om het mogelijk te maken zich op andere delen van het genoom te richten. SATI werkt door een normale kopie van het problematische gen in het niet-coderende gebied van het DNA vóór de mutatieplaats te plaatsen. Dit nieuwe gen wordt vervolgens geïntegreerd in het genoom naast het oude gen via een van de verschillende DNA-reparatieroutes, waardoor het organisme wordt verlost van de schadelijke effecten van het oorspronkelijke, gemuteerde gen, zonder het risico te lopen op schade die gepaard gaat met volledige vervanging ervan.
De wetenschappers testten de SATI-technologie in levende muizen met progeria, die wordt veroorzaakt door een mutatie in het LMNA-gen. Zowel mensen als muizen met progeria vertonen tekenen van vroegtijdige veroudering, hartdisfunctie en een drastisch verkorte levensduur als gevolg van de ophoping van een eiwit dat progerine wordt genoemd. Door SATI te gebruiken, werd een normale kopie van het LMNA-gen in de progeria-muizen ingebracht. De onderzoekers waren in staat om verminderde tekenen van veroudering waar te nemen in verschillende weefsels, waaronder de huid en milt, samen met een verlenging van de levensduur (45% toename in vergelijking met onbehandelde progeria-muizen). Een vergelijkbare verlenging van de levensduur, vertaald naar mensen, zou meer dan een decennium zijn. Het SATI-systeem vertegenwoordigt dus het eerste in vivo gencorrectietechnologie die zich kan richten op niet-coderende DNA-gebieden in meerdere weefseltypen.

Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
Vervolgens wil het team de efficiëntie van SATI verbeteren door het aantal cellen dat het nieuwe DNA bevat te vergroten.
"We zullen met name de details onderzoeken van de cellulaire systemen die betrokken zijn bij DNA-reparatie om de SATI-technologie nog verder te verfijnen voor betere DNA-correctie", zegt Reyna Hernandez-Benitez, mede-eerste auteur van het artikel en een postdoctoraal onderzoeker in de Izpisua Belmonte laboratorium.
Andere auteurs waren onder meer Keiichiro Suzuki, Rupa Devi Soligalla, Emi Aizawa, Fumiyuki Hatanaka, Masakazu Kurita, Pradeep Reddy, Alejandro Ocampo, Tomoaki Hishida, Masahiro Sakurai, Amy N. Nemeth, Concepcion Rodriguez Esteban van Salk; Zhe Li, Christopher Wei en Kun Zhang van de Universiteit van Californië in San Diego; Estrella Nuñez Delicado van Universidad Catolica San Antonio de Murcia; Jun Wu van het Southwestern Medical Center van de Universiteit van Texas; Josep M. Campistol van de ziekenhuiskliniek van Barcelona in Spanje; Pierre Magistretti van de King Abdullah University of Science and Technology in Saoedi-Arabië; Pedro Guillen van de Clinica CEMTRO in Spanje; Jianhui Gong, Yilin Yuan en Ying Gu van de BGI-Shenzhen in China; Guang-Hui Liu van de Chinese Academie van Wetenschappen; en Carlos López-Otín van de Universidad de Oviedo in Spanje.
Het werk werd gefinancierd door de Salk Women & Science Special Award 2016, de JSPS KAKENHI (15K21762 en 18H04036), de Takeda Science Foundation, de Uehara Memorial Foundation, de National Institutes of Natural Sciences (BS291007), The Sumitomo Foundation (170220), The Naito Foundation, The Kurata Grants (1350), de Mochida Memorial Foundation, The Inamori Foundation, het Guangdong Provincial Key Laboratory of Genome Read and Write (nr. 2017B030301011), Guangdong Provincial Academician Workstation van BGI Synthetic Genomics (nr. 2017B090904014), het Shenzhen Peacock Plan (nr. KQTD20150330171505310), de Leona M. en Harry B. Helmsley Charitable Trust (2012-PG-MED002), de G. Harold en Leila Y. Mathers Charitable Foundation, de National Institutes of Health (R01HL123755 en 5 DP1 DK113616), The Progeria Research Foundation, The Glenn Foundation, KAUST, The Moxie Foundation, de Fundación Dr. Pedro Guillen, de Asociación de Futbolistas Españoles en Universidad Católica San Antonio de Murcia (UCAM).
DOI: 10.1038/s41422-019-0213-0
BLOG
Celonderzoek
AUTEURS
Keiichiro Suzuki, Mako Yamamoto, Reyna Hernandez-Benitez, Zhe Li, Christopher Wei, Rupa Devi Soligalla, Emi Aizawa, Fumiyuki Hatanaka, Masakazu Kurita, Pradeep Reddy, Alejandro Ocampo, Tomoaki Hishida, Masahiro Sakurai, Amy N. Nemeth, Estrella Nuñez Delicado , Josep M. Campistol, Pierre Magistretti, Pedro Guillen, Concepcion Rodriguez Esteban, Jianhui Gong, Yilin Yuan, Ying Gu, Guang-Hui Liu, Carlos López-Otín, Jun Wu, Kun Zhang en Juan Carlos Izpisua Belmonte
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.