
30 januari 2020
De bevindingen van het Salk Institute zullen helpen bij de ontwikkeling van nieuwe en verbeterde behandelingen voor hiv
De bevindingen van het Salk Institute zullen helpen bij de ontwikkeling van nieuwe en verbeterde behandelingen voor hiv
LA JOLLA - Wetenschappers van Salk hebben ontdekt hoe een krachtige klasse hiv-medicijnen zich bindt aan een belangrijk onderdeel van hiv-machines. Door voor het eerst driedimensionale structuren van dit complex op te lossen terwijl er verschillende medicijnen aan vastzaten, lieten de onderzoekers zien wat de therapie zo krachtig maakt. Het werk, verschenen in Wetenschap op 30 januari 2020, biedt inzichten die kunnen helpen bij het ontwerpen of verbeteren van nieuwe behandelingen voor hiv.
“De medicijnen die we hebben bestudeerd, zijn de nieuwste verbindingen die vandaag in de kliniek beschikbaar zijn, evenals verschillende belangrijke preklinische moleculen. Tot nu toe wist niemand precies hoe ze zich aan dit hiv-complex bonden', zegt de hoofdauteur van het onderzoek Dmitri Lyumkis, een assistent-professor in Salk's Laboratory of Genetics. "Een beter begrip van hoe de medicijnen werken, zal ons helpen ze te verbeteren en nieuwe therapeutische verbindingen te ontwerpen."
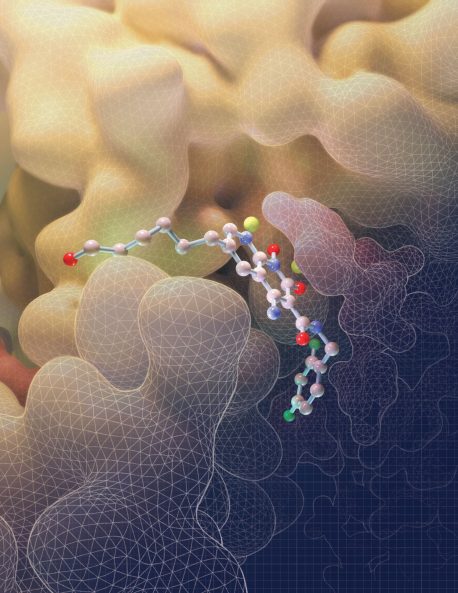
Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
Het intasoom is een cruciale structuur van het virus die infectie mogelijk maakt, samengesteld uit het HIV-eiwitintegrase en strengen van viraal DNA die ontstaan wanneer het virus menselijke cellen binnendringt. Het intasoom beweegt zich in elke menselijke cel en voert vervolgens de chemische reacties uit die nodig zijn om het genetisch materiaal van het virus in het menselijk DNA te integreren.
Sommige medicijnen, genaamd integrase strand transfer inhibitors (INSTI's), zijn erin geslaagd het intasoom te blokkeren; HIV kan geen menselijke cellen infecteren als het complex geen viraal DNA in het menselijk genoom kan integreren. Er zijn momenteel vier INSTI's goedgekeurd door de Amerikaanse Food and Drug Administration, evenals andere in ontwikkeling.
Ondanks het succes van deze moleculen, hebben onderzoekers moeite gehad om te bestuderen hoe ze het hiv-intasoom remmen, grotendeels vanwege de moeilijkheid om intasomen te isoleren voor structurele studies. In het verleden werd het meeste onderzoek naar het intasoom en INSTI's uitgevoerd op een ander retrovirus, het prototype foamy virus of PFV. In 2017 waren Lyumkis en zijn collega's de eersten die dit vaststelden de structuur van gezuiverde HIV-intasomen.
In het nieuwe werk ging het team van Lyumkis nog een stap verder: ze verkregen de structuur van HIV-intasomen terwijl ze actief werden geblokkeerd door een van de vier INSTI's - het in de handel verkrijgbare medicijn bictegravir of drie experimentele verbindingen bekend als 4f, 4d en 4c. Het team gebruikte gekantelde single-particle cryo-elektronenmicroscopie (cryo-EM), een beeldvormende techniek ze hebben geholpen met optimaliseren, om de structuur van elk intasoom-medicijncomplex te onthullen.
De eerste observatie die Lyumkis maakte, was hoe anders de medicijnen zich aan het HIV-intasoom hechtten dan wat was gezien met het PFV-intasoom. De verbinding die bekend staat als 4f, bijvoorbeeld, loopt achterwaarts op zichzelf terwijl het bindt aan het PFV-intasoom, maar blijft relatief vlak omdat het hecht aan de HIV-versie van het complex, details die onderzoekers kunnen helpen de bindingseigenschappen van potentiële toekomstige moleculen te verbeteren.
"Tot op de dag van vandaag gebruikt iedereen nog steeds de PFV-intasoomstructuur om het werkingsmechanisme van deze medicijnen te rationaliseren en te begrijpen", zegt Dario Passos, de co-eerste auteur van de studie en een stafwetenschapper in het laboratorium van Lyumkis. "Maar we hebben laten zien dat het veld echt moet verhuizen en de hiv-structuur moet bestuderen als we verdere vooruitgang willen boeken."

Klik hier voor een afbeelding met een hoge resolutie
Krediet: Salk Institute
"Wij en vele anderen werken al tientallen jaren aan dit doel en het is opwindend dat we nu eindelijk in detail kunnen begrijpen hoe hiv-remmers werken en de ontwikkeling van nieuwe medicijnen kunnen helpen." zegt Min Li, co-eerste auteur en stafwetenschapper bij het National Institute of Diabetes and Digestive and Kidney Diseases.
De structuren onthulden ook waarom de medicijnen zo krachtig zijn en waarom ze zo goed zijn in het voorkomen van resistentie tegen medicijnen. De INSTI's, vonden Lyumkis en zijn collega's, vullen de hele ruimte die normaal wordt ingenomen door DNA. Dat betekent dat als het HIV-intasoom een mutatie ontwikkelt die de binding van de INSTI-geneesmiddelen blokkeert, het ook de hechting van het DNA blokkeert, waardoor het complex onbruikbaar wordt voor het binnendringen van menselijke cellen.
Ten slotte laat de extreem hoge resolutie van de structuur verkregen door de Salk-onderzoekers hen details zien over hoe de medicijnen chemisch interageerden met deze bindende pocket, en hoe INSTI's watermoleculen verplaatsten om dit te doen, wat het team nog meer informatie gaf over wat INSTI's maakt zo succesvol in de kliniek.
"In eerdere structuren leerden we over intasome biologie", zegt Lyumkis. "Maar hier zijn we echt begonnen inzicht te krijgen in de therapeutische invalshoek van hoe medicijnen deze belangrijke virale assemblages kunnen aanvallen."
De onderzoekers plannen extra werk aan de experimentele medicijnen, met de nadruk op de verbinding die bekend staat als 4d, die, gebaseerd op zowel preklinische tests als het nieuwe structurele inzicht, veelbelovender is tegen hiv dan andere verbindingen. Ze willen ook beter begrijpen wat er gebeurt met de structuur van het intasoom in gevallen waarin het resistentie ontwikkelt tegen INSTI's. Dit zou hen kunnen helpen om in de toekomst efficiëntere medicijnen te ontwerpen, zegt Lyumkis.
Andere onderzoekers van het onderzoek waren Ilona Jóźwik en Youngmin Jeon van Salk; Renbin Yang en Robert Craigie van het National Institute of Diabetes and Digestive Diseases; Xue Zhi Zhao, Steven Smith, Stephen Hughes en Terrence Burke Jr. van het National Cancer Institute; en Diogo Santos-Martins en Stefano Forli van The Scripps Research Institute.
Het werk en de betrokken onderzoekers werden ondersteund door subsidies van de National Institutes of Health, de intramurale programma's van het National Institute of Diabetes and Digestive Diseases, de intramurale programma's van het National Cancer Institute en het intramurale AIDS-gerichte antivirale programma van de Nationale gezondheidsinstituten.
DOI: 10.1126/wetenschap.aay8015
BLOG
Wetenschap
AUTEURS
Dario Oliveira Passos, Min Li, Ilona K. Jóźwik, Xue Zhi Zhao, Diogo Santos-Martins, Renbin Yang, Steven J. Smith, Youngmin Jeon, Stefano Forli, Stephen H. Hughes, Terrence R. Burke, Jr., Robert Craigie , Dmitry Lyumkis
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.