
July 6, 2022
Gedetailleerde weergaven van het HIV-eiwit kunnen leiden tot nieuwe behandelingen tegen het virus
Gedetailleerde weergaven van het HIV-eiwit kunnen leiden tot nieuwe behandelingen tegen het virus
LA JOLLA - Begrijpen hoe hiv zich in cellen vermenigvuldigt, is essentieel voor het ontwikkelen van nieuwe therapieën die wereldwijd bijna 40 miljoen mensen met hiv kunnen helpen. Nu heeft een team van wetenschappers van het Salk Institute en Rutgers University voor het eerst de moleculaire structuur bepaald van HIV Pol, een eiwit dat een sleutelrol speelt in de late stadia van HIV-replicatie, of het proces waardoor het virus zich voortplant. en verspreidt zich door het lichaam. Belangrijk is dat het bepalen van de structuur van het molecuul helpt bij het beantwoorden van al lang bestaande vragen over hoe het eiwit zichzelf uit elkaar haalt om het replicatieproces te bevorderen. De ontdekking, gepubliceerd in Wetenschap Advances op 6 juli 2022 onthult een nieuwe kwetsbaarheid in het virus waarop drugs kunnen worden ingezet.
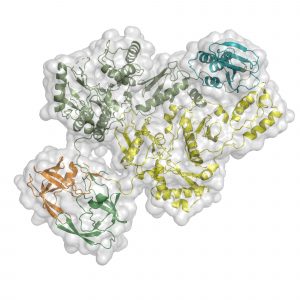
"Structuur informeert de functie, en de inzichten die we hebben verkregen door de moleculaire architectuur van Pol te visualiseren, geven ons een nieuw begrip van het mechanisme waarmee hiv repliceert", zegt co-senior auteur Dmitri Lyumkis, assistent-professor in het Laboratorium voor Genetica en Hearst Foundation Developmental Chair in Salk.
Wetenschappers wisten eerder dat HIV Pol, een polyproteïne, uiteenvalt in drie enzymen - een protease, reverse transcriptase en integrase - die samenwerken om de volwassen vorm van het virus samen te stellen. De protease speelt een cruciale rol bij het initiëren van dit proces door het molecuul in stukken te hakken om de andere componenten te scheiden. Het was echter voorheen niet bekend hoe het protease zich losmaakt, eerst van het grotere polyproteïne HIV Gag-Pol en vervolgens van HIV Pol, om deze taak te volbrengen. Het nieuwe artikel suggereert dat het protease het proces initieert door zichzelf te splitsen of zichzelf los te snijden van de rest van het molecuul, geholpen door reverse transcriptase en mogelijk integrase.
“Het was bekend (maar niet begrepen) dat er een koppeling is tussen deze enzymen voordat HIV Pol uiteenvalt. Het visualiseren van de HIV Pol-structuur verklaart de basis voor dit complexe mechanisme”, zegt co-senior auteur Eddy Arnold, professor aan de raad van bestuur en vooraanstaande professor in het Center for Advanced Biotechnology and Medicine aan de Rutgers University.
"De eerste uitdaging was het produceren van een stabiele versie van HIV Pol, zodat de structuur kon worden geanalyseerd, wat nog nooit eerder was gerapporteerd", zegt co-eerste auteur Jerry Joe Harrison, hoofddocent aan de Universiteit van Ghana.

"Dit was een belangrijk ontbrekend stukje van de structurele hiv-puzzel", voegt Arnold eraan toe.
Het team gebruikte cryogene elektronenmicroscopie, een beeldvormingstechniek waaraan Lyumkis belangrijke bijdragen heeft geleverd, om de driedimensionale structuur van het HIV pol-eiwitmolecuul te onthullen. Dit leidde tot de ontdekking dat Pol een dimeer is, wat betekent dat het wordt gevormd door twee aan elkaar gebonden eiwitten. De bevinding was een verrassing omdat andere vergelijkbare virale eiwitten uit één eiwit bestaan.
De groep toonde aan dat in deze tweezijdige structuur de proteasecomponent van Pol "losjes vastgebonden" is aan de reverse transcriptasecomponent in een bindingsconfiguratie die de protease enigszins flexibel houdt.
"Het houdt de protease op armlengte, losjes, en we denken dat dit de protease een beetje beweging geeft, waardoor het op zijn beurt het knippen van polyproteïnen kan initiëren, wat een voorwaarde is voor virale rijping", zegt co-eerste auteur Dario Passos, een voormalig onderzoeker in het laboratorium van Lyumkis in Salk. "De huidige hiv-behandelingen omvatten meerdere klassen remmers voor alle drie de enzymen, en de ontdekking onthult ook een nieuwe kwetsbaarheid die met medicijnen kan worden bestreden."
De auteurs zeggen dat de ontdekking de deur opent voor belangrijk vervolgonderzoek, waaronder studies naar de structuur van het grotere en complexere polyproteïne Gag-Pol, ook betrokken bij virale assemblage, evenals het nader bekijken van de rol van integrase in het assembleren van de volwassen vorm van het HIV-virus tijdens replicatie.
Andere auteurs waren onder meer Jessica F. Bruhn van Salk; Joseph Bauman, Lynda Tuberty en Francesc Xavier Ruiz van Rutgers; en Jeffrey DeStefano van de Universiteit van Maryland.
Het werk werd gefinancierd door de National Institutes of Health, International Institute of Education, Fulbright-programma, Margaret T. Morris Foundation en Hearst Foundations.
DOI: 10.1126/sciadv.abn9874
BLOG
Wetenschap Advances
AUTEURS
Jerry Joe EK Harrison, Dario Oliveira Passos, Jessica F. Bruhn, Joseph D. Bauman, Lynda Tuberty, Jeffrey J. DeStefano, Francesc Xavier Ruiz, Dmitry Lyumkis, Eddy Arnold
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.