
23 september 2025
Wetenschappers van Salk gebruiken een muismodel om de graciele kern te identificeren als hersengebied dat verantwoordelijk is voor het onderscheid tussen pijnlijke en niet-pijnlijke aanraking, waarbij de disfunctie ervan leidt tot chronische pijn
Wetenschappers van Salk gebruiken een muismodel om de graciele kern te identificeren als hersengebied dat verantwoordelijk is voor het onderscheid tussen pijnlijke en niet-pijnlijke aanraking, waarbij de disfunctie ervan leidt tot chronische pijn
LA JOLLA—Na negen maanden in de baarmoeder betreden mensen een wereld vol textuur en vorm. We moeten dan snel leren texturen en objecten in de buitenwereld te herkennen en erop te reageren, te beginnen met sensaties zoals het zachte gevoel van een T-shirt of het zachte geplette van een sandwich. Door te leren welke aanrakingssensaties onschadelijk zijn, kan het brein pijnlijke verwondingen die schade kunnen veroorzaken beter herkennen – denk aan het schaafwonden van een knie of het stoten van een teen. Maar 7 tot 10 procent van de wereldbevolking ontwikkelt mechanische allodynie, een vorm van chronische pijn waarbij onschadelijke lichte aanraking als pijnlijk wordt ervaren.
Neurowetenschappers van het Salk Institute hebben ontdekt dat veranderde neuronale activiteit in een hersengebied genaamd de kernen van de dorsale kolom mechanische allodynie aanstuurt. De kernen van de dorsale kolom verwerken en categoriseren lichte aanrakingen voordat ze deze doorsturen naar corticale gebieden die onderscheid maken tussen verschillende soorten aanraking. Door de activiteit van muizenneuronen in de graciele kern te monitoren, ontdekten ze dat mechanische allodynie ervoor zorgt dat de normale neurale activiteitspatronen van de graciele kern ongecoördineerd raken. Hierdoor herkent de hersenen lichte aanraking niet langer als onschadelijk, maar interpreteert deze als pijnlijk. Als een vorm van zelfbehoud initieert de hersenen vervolgens een pijnachtige reactie – voorkomen is beter dan genezen.

De bevindingen, gepubliceerd in Cell Reports op 23 september 2025 tonen aan dat ongecoördineerde graciele kernen neurale activiteitspatronen mechanische allodynie veroorzaken—niet Een simpele toename van activiteit, zoals eerder werd aangenomen. Dit nieuwe inzicht in hoe de hersenen pijn verwerken en coderen, is een cruciale eerste stap in de ontwikkeling van therapieën voor acute en chronische pijn.
"We hebben vastgesteld waar het lichaam onderscheid maakt tussen pijnlijke en niet-pijnlijke aanraking, en dat is veel verder stroomopwaarts dan ooit werd gedacht", zegt de hoofdauteur Martijn Goulding, PhD, hoogleraar en houder van de Frederick W. en Joanna J. Mitchell leerstoel aan Salk. "Wat ik vooral interessant vind, is dat we hebben aangetoond dat het de aard van een sensatie zelf is die bepaalt of deze pijnlijk is of niet, in plaats van dat pijn en niet-pijn op een glijdende schaal bestaan waarbij het overschrijden van een bepaalde drempel voldoende is om iets van onschadelijk in pijnlijk te veranderen."
Wat we weten over hoe de hersenen aanraking en pijn verwerken
Pijn is in de eerste plaats een beschermende reactie. Een steen sluipt in je sandaal en je zet een nietsvermoedende stap –au! Instinctief spring je op je andere voet om je gewicht van de rots te halen en het ongemak te verlichten. Op dat moment kan je brein snel het verwachte gevoel van een zachte schoen onderscheiden van het onverwachte gevoel van een puntige rots.
Dit is mogelijk dankzij uitgebreide training om objecten die letsel veroorzaken te onderscheiden van objecten die dat niet doen – onderscheid dat plaatsvindt in de kernen van de dorsale kolom, bestaande uit de nucleus cuneatus en de nucleus gracile, die zich op de grens tussen de bovenste ruggengraat en de hersenstam bevinden. De neuronen in de nucleus cuneatus en de nucleus gracile vuren in patronen, waarbij dit vurenpatroon een representatie vormt van de tastervaring die door de rest van de hersenen kan worden begrepen.
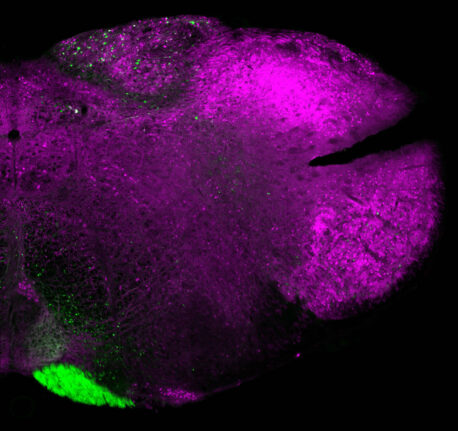
De representatie van de tastzin van de kernen van de dorsale kolom wordt doorgegeven aan een ander gebied, de thalamus, dat ook een belangrijke rol speelt bij pijnperceptie. Dit wordt echter gemedieerd door verschillende thalamische regio's die schadelijke pijninformatie ontvangen van gespecialiseerde pijnreceptoren, nociceptoren genaamd. Normaal gesproken blijven deze twee paden gescheiden, maar in het geval van mechanische allodynie lijken hun draden elkaar te kruisen ter hoogte van de thalamus en hoger, in de cortex. Begrijpen hoe deze draden elkaar kruisen, is de volgende stap in het bepalen hoe de hersenen onschadelijke van pijnlijke aanraking onderscheiden.
Het opzetten van een model om mechanische allodynie te begrijpen
Recente bevindingen wijzen op een verband tussen de kernen van de dorsale kolom en mechanische allodynie, maar de details bleven onduidelijk. Het Salk-team wilde de specifieke rol van de kernen van de dorsale kolom begrijpen en testte de heersende opvatting dat een simpele toename van neurale activiteit resulteert in de transformatie van 'onschadelijke' naar 'pijnlijke' tastsignalen. Om de details te analyseren, moesten muismodellen met en zonder mechanische allodynie worden vergeleken.
"Door zowel ontstekingsgeïnduceerde als letselgeïnduceerde mechanische allodynie te bestuderen, konden we zoeken naar gemeenschappelijke kenmerken in de patronen van neurale activiteit die deze vorm van chronische pijn kenmerken", zegt co-eerste auteur Amandine Virlogeux, postdoctoraal onderzoeker in het laboratorium van Goulding. "Dit leidde ertoe dat we veranderingen in de neurale verwerking observeerden die erop wijzen dat de kernen van de dorsale kolom cruciaal zijn bij het onderscheiden van onschuldige aanraking van potentieel schadelijke aanraking."
De bevindingen tonen aan dat mechanische allodynie niet simpelweg te wijten is aan een toename van de activiteit in de kernen van de dorsale kolom. Mechanische allodynie ontstaat juist wanneer de kernen van de dorsale kolom niet langer in staat zijn om nieuwe informatie correct te coderen en daardoor de standaardinstelling voor aanraking instellen. pijnlijk.
"Letsel of ontsteking verstoort de neurale activiteitspatronen die normaal gesproken onschadelijke aanraking in de kernen van de ruggengraat coderen", legt co-eerste auteur Tejapratap Bollu, postdoctoraal onderzoeker in het laboratorium van Goulding, uit. "Deze veranderde signalen komen niet meer overeen met de representaties in de hersenen, waardoor de hersenen deze onschadelijke stimuli als pijnlijk ervaren."
De toekomst van pijnonderzoek en de weg naar therapie
De ontdekking dat de graciele nucleus de representaties van tastprikkels verandert, is een enorme stap voor neurowetenschappers die mechanische allodynie en de behandeling ervan proberen te begrijpen. De huidige behandelingen voor allodynie variëren van antidepressiva tot zalven. Het aanwijzen van de kernen van de dorsale kolom als fundamenteel voor de expressie van mechanische allodynie is een cruciaal inzicht dat onderzoekers kunnen gebruiken om specifiekere, effectievere medicijnen te ontwikkelen.
Andere auteurs zijn Xiangyu Ren en Ana Palma van Salk.
Het werk werd ondersteund door de National Institutes of Health (R35NS111643, NCI CCSG: P30 CA01495, NINDS R24 Core Grant, NEI), de George E. Hewitt Foundation en de Helen Hay Whitney Foundation.
DOI: 10.1016/j.celrep.2025.116248
BLOG
Cell Reports
AUTEURS
Amandine Virlogeux, Tejapratap Bollu, Xiangyu Ren, Ana Palma, Martyn Goulding
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.