
8 februari 2024
Wetenschappers van Salk schetsen het ontstekingstraject van muizencellen, van mitochondriale stress tot lekkende endosomen en de initiatie van het immuunsysteem, waardoor nieuwe potentiële therapeutische doelen worden onthuld om ontstekingen bij veroudering en ziekte te verminderen
Wetenschappers van Salk schetsen het ontstekingstraject van muizencellen, van mitochondriale stress tot lekkende endosomen en de initiatie van het immuunsysteem, waardoor nieuwe potentiële therapeutische doelen worden onthuld om ontstekingen bij veroudering en ziekte te verminderen
LA JOLLA – Cellen in het menselijk lichaam bevatten energiegenererende mitochondriën, elk met hun eigen mtDNA – een unieke reeks genetische instructies die volledig los staan van het nucleaire DNA van de cel dat mitochondriën gebruiken om levengevende energie te creëren. Wanneer mtDNA blijft waar het thuishoort (in de mitochondriën), ondersteunt het zowel de mitochondriale als de cellulaire gezondheid. Maar als het terechtkomt op een plek waar het niet thuishoort, kan het een immuunreactie op gang brengen die ontstekingen bevordert.

Nu hebben Salk-wetenschappers en medewerkers van UC San Diego een nieuw mechanisme ontdekt dat wordt gebruikt om onjuist functionerend mtDNA van binnen naar buiten de mitochondriën te verwijderen. Wanneer dit gebeurt, wordt het mtDNA gemarkeerd als vreemd DNA en activeert het een cellulair pad dat normaal gesproken wordt gebruikt om ontstekingen te bevorderen om de cel te ontdoen van ziekteverwekkers, zoals virussen.
De bevindingen, gepubliceerd in Natuur celbiologie op 8 februari 2024 bieden veel nieuwe doelen voor therapieën om de ontstekingsroute te verstoren en daardoor ontstekingen tijdens veroudering en ziekten, zoals lupus of reumatoïde artritis, te verminderen.
“We wisten dat mtDNA aan de mitochondriën ontsnapte, maar hoe was nog steeds onduidelijk”, zegt senior en co-corresponderend auteur professor Gerald Schadel, directeur van het San Diego-Nathan Shock Center of Excellence in the Basic Biology of Aging en houder van de Audrey Geisel Chair in Biomedical Science in Salk. "Met behulp van beeldvorming en celbiologische benaderingen kunnen we de stappen volgen van het pad voor het verplaatsen van mtDNA uit de mitochondriën, die we nu kunnen proberen te bereiken met therapeutische interventies om hopelijk de resulterende ontsteking te voorkomen."
Een van de manieren waarop onze cellen reageren op schade en infectie is met wat bekend staat als het aangeboren immuunsysteem. Hoewel de aangeboren immuunrespons de eerste verdedigingslinie tegen virussen is, kan deze ook reageren op moleculen die het lichaam maakt en die eenvoudigweg op ziekteverwekkers lijken, inclusief misplaatst mtDNA. Deze reactie kan leiden tot chronische ontstekingen en bijdragen aan ziekten en veroudering bij de mens.
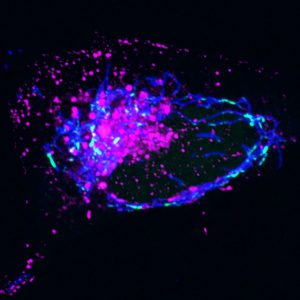
Wetenschappers hebben geprobeerd te ontdekken hoe mtDNA de mitochondriën verlaat en de aangeboren immuunrespons in gang zet, maar de eerder gekarakteriseerde routes waren niet van toepassing op de unieke mtDNA-stressomstandigheden die het Salk-team aan het onderzoeken was. Dus wendden ze zich tot geavanceerde beeldvormingstechnieken om aanwijzingen te verzamelen over waar en wanneer het mis ging in die mitochondriën.
"We hadden een enorme doorbraak toen we zagen dat mtDNA zich in een mysterieuze membraanstructuur bevond zodra het de mitochondriën verliet. Nadat we alle puzzelstukjes hadden samengevoegd, realiseerden we ons dat die structuur een endosoom was", zegt de eerste auteur. Laura Nieuwman, voormalig postdoctoraal onderzoeker in het laboratorium van Shadel en huidig assistent-professor aan de Universiteit van Virginia. “Die ontdekking leidde ons uiteindelijk tot het besef dat het mtDNA werd weggegooid en dat daarbij een deel ervan uitlekte.”
Het team ontdekte een proces dat begon met een storing in de mtDNA-replicatie, waardoor mtDNA-bevattende eiwitmassa's, nucleoïden genaamd, zich opstapelden in de mitochondriën. De cel merkt deze storing op en begint vervolgens de replicatie-remmende nucleoïden te verwijderen door ze naar endosomen te transporteren, een verzameling organellen die celmateriaal sorteren en verzenden voor permanente verwijdering. Het endosoom raakt overbelast met deze nucleoïden, er ontstaat een lek en mtDNA komt plotseling los in de cel. De cel markeert dat mtDNA als vreemd DNA – op dezelfde manier waarop hij het DNA van een virus markeert – en initieert de DNA-detecterende cGAS-STING-route om ontstekingen te veroorzaken.
“Met behulp van onze geavanceerde beeldvormingshulpmiddelen voor het onderzoeken van de dynamiek van de mitochondriën en de afgifte van mtDNA hebben we een geheel nieuw afgiftemechanisme voor mtDNA ontdekt”, zegt co-corresponderende auteur Uri Manor, voormalig directeur van de Waitt Advanced Biophotonics Core bij Salk en huidig assistent-professor. bij UC San Diego. “Er zijn zoveel vervolgvragen die we niet kunnen wachten om te stellen, zoals hoe andere interacties tussen organellen de aangeboren immuunroutes controleren, hoe verschillende celtypen mtDNA vrijgeven, en hoe we ons op deze nieuwe route kunnen richten om ontstekingen tijdens ziekte en veroudering te verminderen.”
De onderzoekers hopen meer van deze ingewikkelde mtDNA-verwijderings- en immuunactivatieroute in kaart te brengen, inclusief welke biologische omstandigheden – zoals mtDNA-replicatiedisfunctie en virale infectie – nodig zijn om de route te initiëren en welke stroomafwaartse effecten er kunnen zijn op de menselijke gezondheid. Ze zien ook een kans voor therapeutische innovatie met behulp van deze route, die een nieuw cellulair doelwit vertegenwoordigt om ontstekingen te verminderen.
Andere auteurs zijn onder meer Sammy Weiser Novak, Gladys Rojas, Nimesha Tadepalle, Cara Schiavon, Christina Towers, Matthew Donnelly, Sagnika Ghosh, Sienna Rocha en Ricardo Rodriguez-Enriquez van Salk; Danielle Grotjahn en Michaela Medina van het Scripps Research Institute; Marie-Ève Tremblay van de Universiteit van Victoria in Canada; Joshua Chevez van UC San Diego; en Ian Lemersal van het La Jolla Instituut voor Immunologie.
Het werk werd ondersteund door de National Institutes of Health (R01 AR069876, P30AG068635, 1K99GM141482, 1F32GM137580, T32GM007198, 5R00CA245187 en 5R00CA245187-04S1), een prijs van het Allen-AHA Initiative in Brain Health and Cognitive Impairment (19 PABH134610000H), een Nationale Wetenschapsstichting NeuroNex Award (2014862), Chan-Zuckerberg Initiative Imaging Scientist Award, de LIFE Foundation, een George E. Hewitt Foundation for Medical Research Postdoctoral Fellowship, Paul F. Glenn Foundation for Medical Research Postdoctoral Fellowship, Salk Pioneer Fund Postdoctoral Scholar Award, de Waitt Foundation, Yale University School of Medicine Center for Cellular and Molecular Imaging, een Canada Research Chair (Tier 2) in Neurobiology of Aging and Cognition, en een Canada Foundation for Innovation John R. Evans Leaders Fund (subsidie 39965).
DOI: 10.1038/s41556-023-01343-1
BLOG
Natuur celbiologie
AUTEURS
Laura E. Newman, Sammy Weiser Novak, Gladys R. Rojas, Nimesha Tadepalle, Cara R. Schiavon, Danielle A. Grotjahn, Christina G. Towers, Marie-Ève Tremblay, Matthew P. Donnelly, Sagnika Ghosh, Michaela Medina, Sienna Rocha , Ricardo Rodriguez-Enriquez, Joshua A. Chevez, Ian Lemersal, Uri Manor en Gerald S. Shadel
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.