
8 januari 2016
Factor in hoe kwaadaardige tumoren zich verspreiden, kan ook een sleutel tot behandeling zijn
Factor in hoe kwaadaardige tumoren zich verspreiden, kan ook een sleutel tot behandeling zijn
LA JOLLA - Glioblastoma multiforme is een bijzonder dodelijk kanker. Een persoon met de diagnose van dit type hersentumor overleeft doorgaans 15 maanden, mits hij de beste zorg krijgt. Wijlen senator Ted Kennedy bezweek in iets meer dan een jaar aan deze ziekte.
Maar wetenschappers van het Salk Institute hebben een sleutel ontdekt voor hoe deze tumorcellen zich zo snel vermenigvuldigen - en manieren om deze motor van tumorgroei om te zetten in een doelwit voor kankerbehandeling.
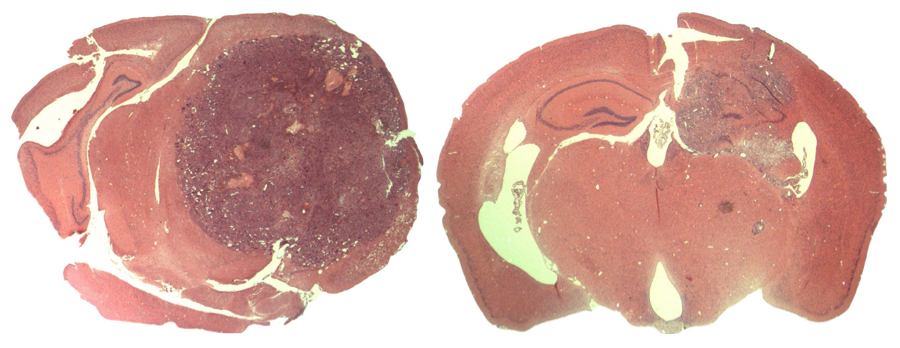
Klik hier om een afbeelding in hoge resolutie te downloaden.
Afbeelding: met dank aan het Salk Institute for Biological Studies
"Dit is een ziekte waarvoor er al jaren praktisch geen verbetering in de behandeling is opgetreden", zei hij Onder Verma, professor in het Laboratorium voor Genetica van het Salk Institute en senior auteur van het artikel dat op 8 januari 2016 in het tijdschrift is gepubliceerd Wetenschap Advances. "Het is duidelijk dat zelfs als een chirurg 99.99 procent van een glioblastoma multiforme tumor verwijdert, wat achterblijft terug zal komen en zal uitgroeien tot meer tumor."
Om te bestuderen hoe glioblastoma multiforme zich verspreidt, concentreerde het team van Verma zich op een transcriptiefactor genaamd nucleaire factor kB (of NF-kB). Een transcriptiefactor is een eiwit dat zich bindt aan DNA en het lot van genexpressie regelt voor een bepaalde reeks genen. Verschillende bekende factoren kunnen NF-kB-activiteit in een cel veroorzaken, waaronder ultraviolette en ioniserende straling, immuuneiwitten (cytokines) en DNA-schade.
In het geval van glioblastoma multiforme voerden Verma en collega's een reeks tests uit om te laten zien hoe overijverige NF-kB-activiteit de kankercellen ertoe aanzette zich te vermenigvuldigen, en hoe het stoppen van NF-kB de groei van kanker vertraagde en de overleving bij muizen verhoogde.
"Onze experimenten hebben bevestigd dat NF-kB nodig is voor de proliferatie van de kankercel", zegt Dinorah Friedmann-Morvinski, eerste auteur van het artikel en momenteel onderzoeker bij de afdeling biochemie en moleculaire biologie aan de Universiteit van Tel Aviv in Israël. "Maar nu hebben we eindelijk een manier gevonden om de tumor te verbeteren en de levensduur te verlengen."
Verma's team begon met een muismodel van glioblastoma multiforme en gebruikte genetische hulpmiddelen om cellen te manipuleren om de NF-kB-activiteit op twee manieren af te sluiten. Het team verhoogde de aanwezigheid van een eiwit genaamd IkBaM, dat de NF-kB-activiteit remt. Ze elimineerden ook een enzym dat de NF-kB-activiteit verhoogt. Met minder NF-kB-activiteit vertraagde de tumorgroei en leefden muizen aanzienlijk langer dan muizen waarvan de NF-kB-activiteit met rust werd gelaten. Maar hoewel deze genetische experimenten de rol van NF-kB in glioblastoma multiforme hebben aangetoond, zijn ze geen haalbare behandeling bij mensen.
"Dus vroegen we hoe we het systeem konden manipuleren met behulp van farmacologie in plaats van genetica", zegt Verma.
Wetenschappers vermoeden al lang dat een van de redenen waarom glioblastoma multiforme zo snel na de operatie terugkomt, de zogenaamde tumor-micro-omgeving is. Met andere woorden, een tumor verandert de omgeving van zijn omgeving (nabijgelegen weefsels) om het voor kankercellen gemakkelijker te maken om te gedijen, legt Verma uit.

Klik hier om een afbeelding in hoge resolutie te downloaden.
Afbeelding: met dank aan het Salk Institute for Biological Studies
In plaats van genetische hulpmiddelen te gebruiken, probeerden Verma en collega's de hersentumoren te behandelen op een manier die ook de micro-omgeving van de tumor veranderde. De wetenschappers voedden muizen met een peptide (NBD genaamd) waarvan bekend is dat het de NF-kB-activiteit blokkeert wanneer NF-kB wordt geactiveerd door cytokines (eiwitten geproduceerd door het immuunsysteem). Het NBD-peptide reist gemakkelijk door het centrale zenuwstelsel en kan met succes glioblastoma-tumorcellen binnendringen. Het behandelen van muizen met het NBD-peptide verdubbelde hun typische overlevingstijd in vergelijking met muizen die het NBD-peptide niet kregen.
"We zouden de overlevingstijd kunnen verlengen van een maand zonder behandeling tot drie maanden met behandeling", zegt Verma. "Dat is een forse stijging van de levensverwachting, vooral als je bedenkt dat een muis maar twee jaar leeft." Maar terwijl het NBD-peptide de tumoren op afstand hield, veroorzaakt de peptidebehandeling uiteindelijk toxiciteit, hoogstwaarschijnlijk in de lever. Dus onderzoekers verkenden een andere tactiek om de NF-kB-activiteit te vertragen.
Het terugdringen van de activiteit van NF-kB kan lastig zijn omdat NF-kB veel belangrijke rollen vervult: het helpt bij het reguleren van celoverleving, ontsteking en immuniteit naast vele andere functies in de cel.
"Het uiteindelijke doel is om NF-kB te blokkeren, maar omdat het veel genen activeert - minstens 100 - werd ons doel het vinden van een handvol genen die rechtstreeks van invloed zijn op de tumorgroei", zegt Verma. "Dan kunnen we selectiever zijn in de behandeling."
Salk-wetenschappers volgden welke genen werden beïnvloed door NF-kB en vonden er een, Timp1, dat eerder betrokken was bij longkanker. Het richten op het Timp1-gen in de behandeling vertraagde ook de tumorgroei en verhoogde de overlevingstijd bij muizen met een paar maanden.
"In de toekomst willen we ons concentreren op manieren om de toxiciteit van anti-NF-kB-geneesmiddelen te verminderen", zei Friedmann-Morvinski. "We kunnen dit doen door deze medicijnen specifiek op de tumor te richten, of door stroomafwaartse doelen van de NF-kB-route te identificeren, zoals Timp1, die ook de overleving verlengen." Verdere experimenten kunnen behandelingen identificeren die op een veilige, maar effectieve manier gericht zijn op NF-kB-activiteit.
Andere auteurs op het papier waren Rajesh Narasimamurthy, Yifeng Xia, Chad Myskiw en Yasushi Soda van het Salk Institute for Biological Studies.
Het werk werd gefinancierd door de National Institutes of Health HN en Frances C. Berger Foundationen Leona M. en Harry B. Helmsley Charitable Trust.
BLOG
Wetenschap Advances
AUTEURS
Dinorah Friedmann-Morvinski, Rajesh Narasimamurthy, Yifeng Xia, Chad Myskiw, Yasushi Soda, Inder M. Verma
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.