
17 februari 2016
Salk Institute en medewerkers tonen belangrijke moleculaire verschillen tussen virussen wanneer ze interageren met gastheer-DNA
Salk Institute en medewerkers tonen belangrijke moleculaire verschillen tussen virussen wanneer ze interageren met gastheer-DNA
LA JOLLA—Gebruikmakend van geavanceerde beeldvormingstechnologie, Salk Institute en Harvard Medical School onderzoekers hebben de structuur bepaald van een eiwitcomplex dat virussen laat lijken op de human immunodeficiency virus (hiv) vestigen permanente infecties binnen hun gastheren.
In tegenstelling tot eerdere aannames, geeft de nieuw gedetailleerde virale eiwitcomplexstructuur aan dat dit type moleculaire architectuur verschilt tussen retrovirussen. Deze informatie helpt te onthullen hoe retrovirussen hun genomische informatie in menselijke cellen inbrengen en kan implicaties hebben, niet alleen voor de behandeling van ziekten zoals HIV, maar ook voor het verbeteren van gentherapiemethoden om nieuw DNA te leveren aan patiënten met genetische mutaties.
"De details van hoe retrovirussen integreren verschillen veel meer dan eerder werd gedacht en leiden tot totaal verschillende infectiepatronen", zegt Dmitry Lyumkis, een Salk kameraad en co-senior auteur van het nieuwe artikel, gepubliceerd in NATUUR op februari 18, 2016.
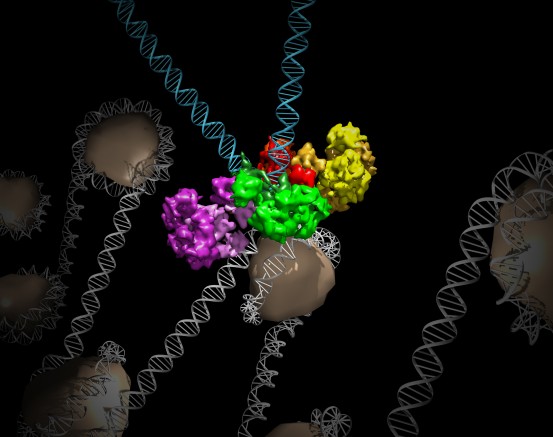
Klik hier voor een afbeelding met hoge resolutie.
Krediet: Salk Institute
Een retrovirus voegt zijn genetische informatie in het eigen genoom van de gastheer in, waardoor de cellen van de gastheer in wezen worden omgezet in fabrieken voor het maken van virussen. In het geval van het bekende retrovirus HIV integreren die virale genen in menselijke immuuncellen en doden ze uiteindelijk. Een al lang bestaand mysterie - deels veroorzaakt door het gebrek aan kennis over de structuur van het eiwitcomplex - bepaalt waar viraal DNA in het menselijk genoom wordt ingebracht.
Een eiwitcomplex, een intasoom genaamd, is verantwoordelijk voor het onomkeerbaar inbrengen van viraal DNA in menselijk DNA, een essentiële stap om retrovirussen in staat te stellen ziekten te veroorzaken. Omdat het intasoom van hiv zelf lastig te bestuderen is, is het meeste van wat er bekend is over intasomen gebaseerd op werk van een ander retrovirus, het prototype foamy virus of PFV. In het licht van monstergerelateerde uitdagingen met betrekking tot HIV-intasomen, gingen Lyumkis en Engelman, samen met hun collega Peter Cherepanov van het Francis Crick Institute, op zoek naar de structuur van het intasoom van het muizenborsttumorvirus (MMTV), dat in sommige opzichten is nauwer verwant aan hiv dan aan PFV.
"De MMTV-intasoomstructuur definieert een onverwacht nieuw paradigma voor de structurele basis van retrovirale DNA-integratie", zegt co-senior auteur Alan Engelman, hoogleraar geneeskunde aan het Dana-Farber Cancer Institute en de Harvard Medical School.
Om de moleculaire structuur van MMTV te bepalen, gebruikte het team een opkomende techniek genaamd cryo-elektronenmicroscopie (cryoEM), een benadering die verschillende voordelen heeft ten opzichte van traditionele beeldvormingstechnieken. Onderzoekers hoeven bijvoorbeeld geen eiwitten over te halen tot kristalvormen om ze in beeld te brengen, een wisselvallig proces dat vereist is voor de meer gebruikelijke techniek van röntgenkristallografie. In cryoEM worden eiwitten in plaats daarvan direct ingevroren in een vloeibare oplossing. Door vervolgens te meten hoe elektronenbundels van de bevroren monsters worden afgebogen, kunnen wetenschappers de structuur van de eiwitten bepalen.
Lyumkis gebruikte deze geavanceerde technologie om de structuur van MMTV-intasomen te beschrijven die zijn gebonden aan strengen van viraal DNA (de manier waarop de structuur eruit zou zien als deze een gastheercel zou binnendringen). Het team ontdekte dat hoewel het PFV-complex is samengesteld uit vier eiwitcomponenten, integrasen genaamd, gebonden aan twee strengen viraal DNA, de MMTV-assemblage acht integrasemoleculen per twee stukjes viraal DNA heeft.
Dit belangrijke structurele verschil, zegt Lyumkis, betekent dat de complexen anders interageren met het gastheer-DNA wanneer ze klaar zijn om viraal DNA in het genoom te brengen. PFV geeft de voorkeur aan plekken in het gastheergenoom die sterk gebogen zijn, terwijl MMTV rechte stukken DNA kiest. De voorkeur voor hiv blijft een mysterie, maar de nieuwe waarnemingen bieden een onverwacht moleculair raamwerk waarbinnen vroegere en toekomstige gegevens over hiv en andere retrovirussen kunnen worden geïnterpreteerd.
De teams van Lyumkis en Engelman werken nu aan het begrijpen van de reeks gebeurtenissen die het MMTV-intasoomcomplex doormaakt tijdens de stappen van virale integratie, van het binden van viraal DNA tot het vastleggen van gastheer-DNA en het katalyseren van de insertie van viraal DNA in het genoom van de gastheer. Lyumkis is ook van plan om cryoEM-technieken toe te passen om het HIV-intasoom-molecuulcomplex zelf te bestuderen. "De technologische infrastructuur is aanwezig, dus nu denk ik dat we deze lastige en slecht gedragende exemplaren kunnen aanpakken met behulp van cryoEM", voegt Lyumkis toe.
Andere onderzoekers van het onderzoek waren Allison Ballandras-Colas en Tamaria G. Dewdney van de Dana-Farber Kankerinstituut en de Medische School van Harvard; Monica Brown van het Salk Instituut; Nicola J. Cook en Peter Cherepanov van de Francis Crick Instituut; en Borries Demeler van de Centrum voor Gezondheidswetenschappen van de Universiteit van Texas.
Het werk en de betrokken onderzoekers werden ondersteund door subsidies van de National Institutes of Health Leona M. en Harry B. Helmsley Charitable Trust National Science Foundation en het San Antonio Kankerinstituut.
BLOG
NATUUR
AUTEURS
Allison Ballandras-Colas, Tamaria G. Dewdney en Alan Engelman van de Harvard Medical School; Monica Brown en Dmitry Lyumkis van het Salk Institute; Nicola J. Cook en Peter Cherepanov van het Francis Crick Institute; en Borries Demeler van het Health Sciences Center van de Universiteit van Texas
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.