
17 maart 2023
Twee therapeutische geneesmiddelen, één door de FDA goedgekeurd en één in klinische onderzoeken, komen ten goede aan muizen met LKB1-gemuteerde, niet-kleincellige longkanker, wat mogelijk de weg vrijmaakt voor klinische proeven bij mensen
Twee therapeutische geneesmiddelen, één door de FDA goedgekeurd en één in klinische onderzoeken, komen ten goede aan muizen met LKB1-gemuteerde, niet-kleincellige longkanker, wat mogelijk de weg vrijmaakt voor klinische proeven bij mensen
LA JOLLA—Kankerbehandelingen gaan al lang in de richting van personalisatie—het vinden van de juiste medicijnen die werken voor de unieke tumor van een patiënt, op basis van specifieke genetische en moleculaire patronen. Veel van deze gerichte therapieën zijn zeer effectief, maar zijn niet beschikbaar voor alle kankers, inclusief niet-kleincellige longkankers (NSCLC's) met een LKB1-genetische mutatie. Een nieuwe studie onder leiding van Salk Institute Professor Ruben Shaw en voormalig postdoctoraal onderzoeker Lillian Eichner, nu assistent-professor aan de Northwestern University, onthulde dat door de FDA goedgekeurde trametinib en entinostat (die momenteel in klinische onderzoeken zijn) samen kunnen worden gegeven om minder en kleinere tumoren te produceren bij muizen met LKB1-gemuteerde NSCLC.
De bevindingen werden gepubliceerd in Wetenschap Advances in maart 17, 2023.
"Voor gevallen van niet-kleincellige longkanker met de LKB1-mutatie zijn standaard chemotherapie- en immunotherapiebehandelingen niet effectief", zegt Shaw, senior en co-corresponderende auteur van de studie, en directeur van Salk's Cancer Center. "Onze bevindingen tonen aan dat er een manier is om deze gevallen aan te pakken met medicijnen die door de FDA zijn goedgekeurd of die al in klinische onderzoeken zijn, dus dit werk kan gemakkelijk worden gebruikt voor een klinische proef bij mensen."
Ongeveer 20 procent van alle NSCLC's heeft de LKB1-genetische mutatie, wat betekent dat er momenteel geen effectieve gerichte therapieën op de markt zijn voor patiënten met dit type kanker. Om een therapie te creëren die zich op de LKB1-mutatie zou kunnen richten, wendden de onderzoekers zich tot histondeacetylasen (HDAC's). HDAC's zijn eiwitten die geassocieerd zijn met tumorgroei en metastase van kanker, met kenmerkende overexpressie in solide tumoren. Verschillende HDAC-remmers zijn al door de FDA goedgekeurd (veilig voor menselijk gebruik) voor specifieke vormen van lymfoom, maar gegevens over hun werkzaamheid bij solide tumoren of dat tumoren met specifieke genetische veranderingen een verhoogd therapeutisch potentieel kunnen vertonen, ontbreken.
Op basis van eerdere bevindingen die het LKB1-gen verbinden met drie andere HDAC's die allemaal afhankelijk zijn van HDAC3, begon het team met het uitvoeren van een genetische analyse van HDAC3 in muismodellen van NSCLC, waarbij een onverwacht cruciale rol voor HDAC3 in meerdere modellen werd ontdekt. Nadat ze hadden vastgesteld dat HDAC3 van cruciaal belang was voor de groei van de moeilijk te behandelen LKB1-gemuteerde tumoren, onderzochten de onderzoekers of het farmacologisch blokkeren van HDAC3 een vergelijkbaar krachtig effect zou kunnen geven.

Het team was nieuwsgierig naar het testen van twee medicijnen, entinostat (een HDAC-remmer in klinische onderzoeken waarvan bekend is dat ze zich richten op HDAC1 en HDAC3) en door de FDA goedgekeurde trametinib (een remmer voor een andere klasse van enzymen die verband houden met kanker). Tumoren worden vaak snel resistent tegen trametinib, maar gelijktijdige behandeling met een geneesmiddel dat een eiwit stroomafwaarts van HDAC3 remt, helpt deze resistentie te verminderen. Omdat dat eiwit afhankelijk is van HDAC3, geloofden de onderzoekers dat een geneesmiddel dat gericht is op HDAC3, zoals entinostat, ook zou helpen om de resistentie tegen trametinib te beheersen.
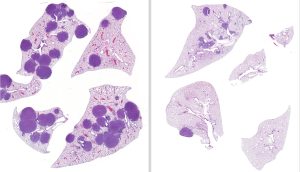
Na 1 dagen behandeling van muizen met LKB42-gemuteerde longkanker met variabele behandelingsregimes, ontdekte het team dat muizen die zowel entinostat als trametinib kregen 79 procent minder tumorvolume en 63 procent minder tumoren in hun longen hadden dan de onbehandelde muizen. Bovendien bevestigde het team dat entinostat een levensvatbare behandelingsoptie was in gevallen waarin een tumor resistent was tegen trametinib.
“We dachten dat de hele HDAC-enzymklasse rechtstreeks verband hield met de oorzaak van LKB1-gemuteerde longkanker. Maar we kenden de specifieke rol van HDAC3 bij de groei van longtumoren niet', zegt eerste en co-corresponderende auteur Eichner. "We hebben nu aangetoond dat HDAC3 essentieel is bij longkanker, en dat het een kwetsbaarheid is voor therapeutische resistentie."
De bevindingen kunnen leiden tot klinische proeven om het nieuwe regime bij mensen te testen, aangezien entinostat al in klinische proeven is en trametinib door de FDA is goedgekeurd. Belangrijk is dat Shaw deze ontdekking ziet als transformatief voor kankers buiten NSCLC, met mogelijke toepassingen bij lymfoom, melanoom en pancreaskanker.
"Ons lab heeft zich jaren aan dit project gewijd en heeft kleine en zinvolle stappen gezet in de richting van deze bevindingen", zegt Shaw, houder van de William R. Brody-leerstoel. "Dit is echt een succesverhaal voor hoe fundamentele ontdekkingswetenschap kan leiden tot therapeutische oplossingen in de niet zo verre toekomst."
“Mijn onafhankelijk laboratorium heeft het geluk deel uit te maken van het Lurie Cancer Center aan de Feinberg School of Medicine aan de Northwestern University, dat translationeel onderzoek zeer ondersteunt. We hopen dat deze omgeving de start van een klinische proef op basis van deze bevindingen zal vergemakkelijken, "zegt Eichner.
Andere auteurs zijn Stephanie D. Curtis, Sonja N. Brun, Joshua T. Baumgart, Elijah Trefts, Debbie S. Ross en Tammy J. Rymoff van Salk; en Caroline K. McGuire en Irena Gushterova van Northwestern University.
Het werk werd ondersteund door de National Institutes of Health (R35CA220538, P01CA120964, K22CA251636, 5T32CA009370, 5F32CA206400, CCSG P30CA014195 en CCSG P30CA23100), Leona M. en Harry B. Helmsley Charitable Trust (#2012-PG- MED002), Amerikaanse kanker Maatschappij (PF-15-037-01-DMC) en Chapman Foundation.
DOI: 10.1126/sciadv.add3243
BLOG
Wetenschap Advances
TITEL
HDAC3 is van cruciaal belang bij de ontwikkeling van tumoren en therapeutische resistentie bij Kras-mutante niet-kleincellige longkanker
AUTEURS
Lillian J. Eichner, Stephanie D. Curtis, Sonja N. Brun, Caroline K. McGuire, Irena Gushterova, Joshua T. Baumgart, Elijah Trefts, Debbie S. Ross, Tammy J. Rymoff, Reuben J. Shaw
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.