
2024 年 2 月 28 日
ソークの科学者は、アルツハイマー病などの神経疾患におけるストレスと炎症を研究するために、豊富なアストロサイトを含む人間の脳オルガノイドモデルを作成
ソークの科学者は、アルツハイマー病などの神経疾患におけるストレスと炎症を研究するために、豊富なアストロサイトを含む人間の脳オルガノイドモデルを作成
ラホヤ—脳は通常、メッセージを送受信するニューロンの複雑な網として描かれています。しかし、ニューロンは人間の脳の半分しか構成していません。残りの半分、約 85 億個の細胞は、グリアと呼ばれる非神経細胞です。最も一般的な種類のグリア細胞はアストロサイトであり、ニューロンの健康と活動をサポートするために重要です。それにもかかわらず、人間の脳の既存の実験室モデルのほとんどには、アストロサイトが十分なレベルで含まれていない、またはまったく含まれていないため、脳の健康と病気を研究するためのモデルの有用性が制限されています。
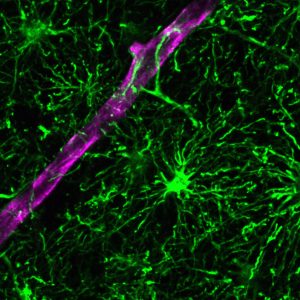
今回、ソークの科学者らは、成熟した機能的な星状膠細胞を含む、人間の組織の特徴を模倣した細胞の三次元集合体である人間の脳の新しいオルガノイドモデルを作成した。このアストロサイトが豊富なモデルを使用することで、研究者は老化やアルツハイマー病などの疾患における炎症やストレスをこれまでよりも明確かつ深く研究できるようになります。すでに研究者らはこのモデルを使用して、星状膠細胞の機能不全と炎症との関係、およびその関係を破壊するための創薬可能性のある標的を明らかにしている。
調査結果はに掲載されました ネイチャー·バイオテクノロジー 2月28、2024に。
「アストロサイトは、脳内で最も豊富に存在する種類のグリア細胞ですが、脳オルガノイドモデルでは過小評価されてきました」と上級著者は述べています。 ラスティ・ゲージ、教授であり、ソーク大学の加齢に伴う神経変性疾患研究のヴィ・アンド・ジョン・アドラー議長。 「私たちのモデルはこの欠陥を修正し、アストロサイトが脳機能に不可欠であるさまざまな方法や、さまざまな神経学的状態におけるストレスや炎症にアストロサイトがどのように反応するかを調査するために使用できる、グリアが豊富なヒト脳オルガノイドを提供します。」
過去 10 年間で、オルガノイドは、細胞研究と人間の研究の間のギャップを埋めるための普及したツールとして登場しました。オルガノイドは、他の実験システムよりも人間の発生や器官生成を模倣することができるため、研究者はより現実的な環境で薬物や病気が人間の細胞にどのような影響を与えるかを研究することができます。脳オルガノイドは通常、培養皿で培養されますが、アストロサイトなどの特定の脳細胞を効率的に生産する能力が限られていることが依然として問題となっています。
アストロサイトはニューロンと同じ経路で発生し、最初はニューロン幹細胞として始まり、分子スイッチが切り替わって細胞の運命がニューロンからアストロサイトに変わるまで続きます。アストロサイトが豊富に存在する脳オルガノイドを作成するために、研究チームはこのスイッチを引き起こす方法を探しました。
これを行うために、研究者らは特定のグリオ生成化合物をオルガノイドに送達し、それらがアストロサイトの形成を促進するかどうかを調べた。その後、チームはアストロサイトが発達しているかどうか、発達している場合はその数とどの程度成熟したかを確認するためのテストを開始しました。
皿の中で培養された脳オルガノイドには、人間の脳の微小環境や神経構造の配置がまだ欠けていました。より人間の脳に似た環境を作り出すために、研究者らはオルガノイドをマウスモデルに移植し、数か月かけてさらに発達できるようにした。

「私たちの移植オルガノイドモデルは、古いモデルで可能であったものよりも、より洗練され、分化した星状細胞集団を生成しました」と、共同筆頭著者であり、ゲージの研究室の元博士研究員である Lei Zhang 氏は述べています。人間の脳における機能的な細胞グループの組織化を実験室で模倣することは非常に困難ですが、私たちのオルガノイドモデルのこれらのアストロサイトはまさにそれを行っていました。」
移植されたオルガノイドにおけるアストロサイトのサブタイプの発生と成熟を観察した後、研究者らは神経炎症の過程におけるアストロサイトの役割を調査することを目的とした。老化および加齢に関連した神経疾患は、免疫系および炎症と強い関係があり、アストロサイトもこの関係に関与しているかどうかは、神経科学者にとって長年の疑問でした。
これをテストするために、研究者らは移植されたオルガノイドに炎症誘発性化合物を導入し、アストロサイトのサブタイプが活性化され、さらなる炎症誘発性経路を促進することを発見した。さらに、CD38と呼ばれる分子が、反応性アストロサイトの代謝ストレスやエネルギーストレスの媒介に重要であることも発見した。 CD38シグナル伝達がこの重要な役割を果たしているということは、CD38阻害剤がこれらの反応性アストロサイトによって引き起こされる神経炎症および関連ストレスを軽減できる可能性があることを示唆している、とGage氏は言う。

「私たちは、これまで以上に現実の脳モデルに似た研究用の人間の脳モデルを作成しました。これには、人間の皮質に見られる主要な星状細胞のサブクラスがすべて含まれています」と、共同筆頭著者で博士研究員のメイヤン・ワン氏は言う。ゲイジの研究室。 「このモデルにより、我々はすでに炎症とアストロサイトの機能不全との関連性を発見しており、その過程でCD38がその関連性を破壊するための潜在的な創薬可能性のある標的であることを明らかにしました。」
彼らの発見は以下に基づいています 研究室で開発された別の最近のモデル それは、ミクログリアと呼ばれる異なる種類のグリア細胞を特徴としていました。このアストロサイトが豊富なモデルはこれまでで最も先進的ですが、研究チームはすでに、追加の脳細胞タイプを組み込み、さらなる細胞成熟を促進することにより、オルガノイド モデルの改良と拡張を目指しています。その間、彼らはこの洗練されたモデルを使用して脳の機能と機能不全を新たに詳細に調査することを目指しており、その発見がアルツハイマー病のような神経疾患に対する新たな介入や治療法につながることを期待している。
他の著者には、サミー・ワイザー・ノバク、ジンティン・ユー、イリーナ・ガリーナ、リン・シュー、クリスティーナ・リム、サラ・フェルナンデス、マキシム・ショヒレフ、エイプリル・ウィリアムズ、モニシャ・サクセナ、シャシャンク・クーラパティ、サラ・パリラック、クリスティアン・キンテロ、エルサ・モリーナ、ソークのレオナルド・アンドラーデが含まれる。そして研究当時ソーク研究の教授だったウリ・マナー氏。
この研究は、米国心臓協会、ポール・G・アレン・フロンティアーズ・グループ助成金(#19PABHI34610000)、JPB財団、アネット・C・マール・スミス、リン&エドワード・ストレイム、ミルキー・ウェイ財団、レイ&ダグマー・ドルビー・ファミリー基金によって支援された。 、国立衛生研究所 (R37 AG072502-03、P30 AG062429-05、P30 AG068635-04、R01 AG070154-04、AG056306-07、P01 AG051449-08、NCI CCSG: P30 014195、NINDS R24 Core Grant、National Eye)研究所) 、NGSコア施設、GT3コア施設、ラザヴィ・ニューマン統合ゲノミクスおよびバイオインフォマティクス・コア施設、チャップマン財団、ウェイト財団、脳・行動研究財団NARSAD若手研究者助成金、およびパイオニア基金博士研究員賞。
DOI: 10.1038/s41587-024-02157-8
ジャーナル
ネイチャー·バイオテクノロジー
作者
Meiyan Wang、Lei Zhang、Sammy Weiser Novak、Jingting Yu、Iryna S. Gallina、Lynne L. Xu、Christina K. Lim、Sarah Fernandes、Maxim N. Shokhirev、April E. Williams、Monisha D. Saxena、Shashank Coorapati、Sarah L. パリラック、クリスティアン キンテロ、エルサ モリーナ、レオナルド R. アンドラーデ、ウリ マナー、フレッド H. ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。