
2023 年 5 月 11 日
ソークの科学者は、脳の免疫細胞が自閉症スペクトラム障害やアルツハイマー病などの脳の状態にどのような影響を与えるかを理解するためのオルガノイドモデルを確立
ソークの科学者は、脳の免疫細胞が自閉症スペクトラム障害やアルツハイマー病などの脳の状態にどのような影響を与えるかを理解するためのオルガノイドモデルを確立
ラホーヤ—人間の免疫系と脳の交差点には、発達と疾患において重要な役割を果たす特殊な脳免疫細胞であるミクログリアが存在します。 ミクログリアの重要性には議論の余地がありませんが、ミクログリアのモデル化と研究は依然として困難な課題です。
体外やヒト以外のモデルで研究できる一部のヒト細胞とは異なり、ヒトのミクログリアは、人間の脳に似た環境から離れると研究が困難になります。 この障壁を克服するために、ソークの科学者はオルガノイド モデル、つまり人間の組織の特徴を模倣した細胞の三次元集合体を開発しました。 このモデルにより、研究者は生きたヒト由来の組織で初めてヒトのミクログリアの発生と機能を研究することができます。 さらに科学者らは、脳環境がより反応性の高いミクログリアの発達に影響を与えるかどうかを判断するために、大頭型自閉症スペクトラム障害(乳児の頭囲が他の乳児の97パーセントよりも大きい状態)を持つ小児の患者由来のミクログリアを検査した。
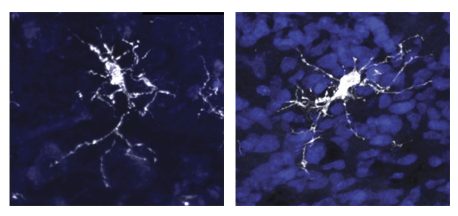
に発表された調査結果、 セル 11 年 2023 月 XNUMX 日に、免疫細胞と脳の相互作用の重要性を強調し、自閉症スペクトラム障害やアルツハイマー病などの神経変性疾患や発達疾患への理解を深めます。
「脳環境の外では、ミクログリアはほぼすべての機能と意味を失います」と教授は言います。 ラスティ・ゲージ、上級著者であり、加齢に伴う神経変性疾患研究のヴィ・アンド・ジョン・アルダー委員長の保持者。 「ヒトのミクログリアを研究するためにオルガノイドで人間の脳環境を再現する方法を見つければ、健康な脳と病気の脳がミクログリアにどのような影響を与えるのか、そして逆に健康な脳と病気の脳がどのように影響するのかを調べるためのツールが最終的に得られることはわかっていました。ミクログリアは脳に影響を与えます。」
約 10 年前に登場したオルガノイドは、細胞研究とヒト研究の間のギャップを埋めるための普及したツールとなっています。 オルガノイドは、他の実験システムよりも人間の発生や器官生成を模倣することができるため、研究者はより現実的な環境で薬物や病気が人間の細胞にどのような影響を与えるかを研究することができます。 脳オルガノイドは通常、培養皿で培養されますが、血管の欠如、生存期間の短さ、多様な細胞型(ミクログリアなど)の維持不能などにより、構造的および機能的に制限されています。

「成熟したミクログリアを含み、それらの研究を可能にする脳オルガノイドモデルを作成するために、私たちは人間の脳に似た環境を作り出す新しい移植技術を使用しました」と共同筆頭著者のアベド・マンスール氏は言う。現在はエルサレムのヘブライ大学で助教授を務めている。 「これにより、ヒトのミクログリアの成長、行動、機能を調整するために必要な機能をすべて備えたヒトの脳オルガノイドをついに作ることができました。」
以前のモデルとは異なり、研究者らはミクログリアを持った人間の脳オルガノイドを作成しました。 の三脚と 人間の脳に似た環境により、最終的に脳の発達全体を通してミクログリアに対する環境の影響を調べることが可能になりました。 彼らは、SALL1と呼ばれる特徴的なタンパク質が発生開始から119週間という早い段階で出現し、ミクログリアの同一性を確認し、成熟した機能を促進するのに役立つことを発見した。 さらに、タンパク質TMEM2やP12RYXNUMXなどの脳環境特異的因子がミクログリアの機能に必要であることも発見した。
「人間の脳環境を効果的に再現できる人間の脳モデルを作成することは、非常に興味深いことです」と准教授は言います。 アクセル・ニンマーヤーン、研究の別の著者。 「このモデルを使用すると、人間のミクログリアが人間の脳環境内でどのように機能するかをついに調べることができます。」

研究チームがミクログリアについてさらに学ぶにつれて、特に病気のシナリオにおいて、脳環境とミクログリアの関係の重要性が明らかになりました。 研究所 以前に調べた 自閉症スペクトラム障害を持つ人々に由来するニューロンを調査したところ、彼らのニューロンは定型発達のニューロンよりも成長が速く、より複雑な分岐を持っていることがわかりました。 新しいオルガノイドモデルを使えば、研究チームは、これらの神経細胞の違いが脳環境を変え、ミクログリアの発達に影響を与えるかどうかを問うことができるだろう。
そうするために、彼らは、大頭症の自閉症スペクトラム障害を持つ XNUMX 人の個人と大頭症の XNUMX 人の定型発達者の皮膚サンプルに由来するミクログリアを比較しました。 研究者らは、自閉症スペクトラム障害を持つ個人が、研究チームが以前に指摘していた神経細胞の違いを示しており、ミクログリアが生育環境におけるそれらの違いの影響を受けていることを発見した。 このニューロン依存の環境変化により、ミクログリアは損傷や侵入者に対してより反応しやすくなりました。この発見は、一部の自閉症スペクトラム障害患者に観察される脳の炎症を説明できる可能性があります。
これはサンプルサイズが小さい予備研究であったため、研究チームは今後さらに多くの人々からミクログリアを調べてその結果を検証する予定です。 彼らはまた、ミクログリアが病気の発症にどのように寄与しているかを調べるために、他の発生疾患や神経変性疾患の研究にも研究を拡大することを目指しています。
「脳を解体するのではなく、私たちは脳を自分たちで構築することにしました」と共同筆頭著者のサイモン・シェーファー氏は言う。彼はゲージ氏の研究室の元博士研究員で、現在はミュンヘン工科大学の助教授である。 「独自の脳モデルを構築することで、ボトムアップで作業を進め、トップダウンでは不可能な解決策を見つけることができます。 私たちはモデルを改良し続け、脳と免疫系の関係を解明していきたいと考えています。」
他の著者には、Monique Pena、Saeed Ghassemzadeh、Lisa Mitchell、Amanda Mar、Daphne Quang、Sarah Stumpf、およびソーク研究所の Clara Baek が含まれます。 カリフォルニア大学サンディエゴ校のヨハネス・CM・シュラチェツキ氏、アディソン・J・ラナ氏、クリストファー・K・グラス氏。 ミュンヘン工科大学のイレーネ・サンティステバン氏。 エルサレムのヘブライ大学のラガッド・ザガル氏。
この研究は、国立衛生研究所 (R01 AG056306、R01 AG057706、R01 AG056511、R01 AG061060、R01 NS108034、U19 NS123719、NCI CCSG: P30 014195、NCI CCSG: P30 014195)、米国心臓協会、およびポール G.アレン・フロンティアーズ・グループ (助成金 19PABHI34610000)、脳・行動研究財団 (27685 および 30421)、ドイツ研究財団 (500300695)、ミルキーウェイ研究財団、アネット・C・マール・スミスおよびロバート・アンド・メアリー・ジェーン・エングマン財団、欧州分子生物学機関 (ALTF 1214-2014)、ヒューマンフロンティアサイエンスプログラム (LT001074/2015)、欧州研究評議会、チャップマン財団、JBP 財団、およびヘルムスリー慈善信託。
DOI: 10.1016 / j.cell.2023.04.022
ジャーナル
セル
作者
サイモン・T・シェーファー、アベド・A・マンスール、ヨハネス・CM・シュラチェツキ、モニク・ペーニャ、サイード・ガセムザデ、リサ・ミッチェル、アマンダ・マー、ダフネ・クアン、サラ・スタンプフ、アイリーン・サンティステバン・オルティス、アディソン・J・ラナ、クララ・ベク、ラガッド・ザガール、クリストファー・K.グラス、アクセル・ニンマーヤーン、フレッド・H・ゲージ
通信局
電話:(858)453-4100
press@salk.edu
ソーク研究所は、1960年に世界初の安全かつ効果的なポリオワクチンを開発したジョナス・ソーク博士によって設立された、独立した非営利研究機関です。研究所の使命は、がん、アルツハイマー病、農業の脆弱性といった社会が直面する最も差し迫った課題に対処するため、基礎的かつ協調的でリスクを伴う研究を推進することです。この基礎科学はあらゆるトランスレーショナルリサーチの基盤となり、世界中の新薬やイノベーションを可能にする知見を生み出しています。